Diferencia entre revisiones de «Reactivo de Gilman»
correcciones menores |
|||
| (No se muestran 18 ediciones intermedias de 14 usuarios) | |||
| Línea 1: | Línea 1: | ||
Un '''reactivo de Gilman''', o '''diorganocuprato de litio''', es un [[compuesto de organocobre|compuesto organocúprico]] de fórmula R<sub>2</sub>[[Cobre|Cu]][[Litio|Li]], donde R puede ser un [[alquilo]], un [[vinilo]] o un [[Grupo arilo|arilo]]. Recibe su nombre por el químico |
Un '''reactivo de Gilman''', o '''diorganocuprato de litio''', es un [[compuesto de organocobre|compuesto organocúprico]] de fórmula R<sub>2</sub>[[Cobre|Cu]][[Litio|Li]], donde R puede ser un [[alquilo]], un [[Grupo vinilo|vinilo]] o un [[Grupo arilo|arilo]]. Recibe su nombre por el químico estadounidense [[Henry Gilman]]. |
||
== Síntesis == |
== Síntesis == |
||
Se preparan, |
Se preparan, dada su inestabilidad, por [[transmetalación]] a partir de un reactivo [[compuesto de organolitio|organolítico]] y una [[Sal (química)|sal]] cuprosa (cobre(I)): |
||
:RLi + CuX → RCu + LiX |
:RLi + CuX → RCu + LiX |
||
:RCu + RLi → R<sub>2</sub>CuLi |
:RCu + RLi → R<sub>2</sub>CuLi |
||
donde X = [[Yodo|I]]<sup>−</sup> |
donde X = [[Yodo|I]]<sup>−</sup> o [[Bromo|Br]]<sup>−</sup>. |
||
== Aplicaciones == |
== Aplicaciones == |
||
| Línea 14: | Línea 14: | ||
Tienen aplicaciones en [[síntesis orgánica]]. No son [[Base (química)|básicos]] y toleran la presencia de los grupos [[hidroxilo]] y [[carboxilo]], además de no reaccionar tampoco ni con [[Cetona (química)|cetonas]] ni [[éster]]es, aunque sí lo hacen con el grupo [[carbonilo]] de [[aldehído]]s no [[Sistema conjugado|conjugados]]. Su reactividad consiste en: |
Tienen aplicaciones en [[síntesis orgánica]]. No son [[Base (química)|básicos]] y toleran la presencia de los grupos [[hidroxilo]] y [[carboxilo]], además de no reaccionar tampoco ni con [[Cetona (química)|cetonas]] ni [[éster]]es, aunque sí lo hacen con el grupo [[carbonilo]] de [[aldehído]]s no [[Sistema conjugado|conjugados]]. Su reactividad consiste en: |
||
*Creación de enlaces C-C mediante procesos de sustitución. Por ejemplo, sustitución del átomo de [[halógeno]] por el grupo R en [[organohalógeno]]s: |
* Creación de enlaces C-C mediante procesos de sustitución. Por ejemplo, sustitución del átomo de [[halógeno]] por el grupo R en [[organohalógeno]]s: |
||
:R<sub>2</sub>CuLi + 2 R'X → R-R' + CuX + LiX |
:R<sub>2</sub>CuLi + 2 R'X → 2 R-R' + CuX + LiX |
||
donde R' puede ser un alquilo, un vinilo o un arilo. |
donde R' puede ser un alquilo, un vinilo o un arilo. |
||
*Sustitución S<sub>N</sub>2' formal sobre [[Sustrato (química)|sustratos]] [[Grupo alilo|alílicos]]. |
* Sustitución S<sub>N</sub>2' formal sobre [[Sustrato (química)|sustratos]] [[Grupo alilo|alílicos]]. |
||
:R<sub>2</sub>CuLi + 2 ''C''H<sub>2</sub>=CH-CH<sub>2</sub>X → 2 R-''C''H<sub>2</sub>-CH=CH<sub>2</sub> + CuX + LiX |
:R<sub>2</sub>CuLi + 2 ''C''H<sub>2</sub>=CH-CH<sub>2</sub>X → 2 R-''C''H<sub>2</sub>-CH=CH<sub>2</sub> + CuX + LiX |
||
*Apertura de [[epóxido]]s, para dar [[alcohol]]es. |
* Apertura de [[epóxido]]s, para dar [[alcohol]]es. |
||
*[[Sustitución nucleófila acílica]] sobre [[Haluro de acilo|haluros de acilo]] para dar cetonas. |
* [[Sustitución nucleófila acílica]] sobre [[Haluro de acilo|haluros de acilo]] para dar cetonas. |
||
*[[Adición conjugada|Adiciones conjugadas]], sobre aldehídos, cetonas y ésteres α,β-insaturados, y [[ciclopropano]]s activados ([[electrófilo]]s). |
* [[Adición conjugada|Adiciones conjugadas]], sobre aldehídos, cetonas y ésteres α,β-insaturados, y [[ciclopropano]]s activados ([[electrófilo]]s). |
||
[[ |
[[Archivo:1,4-Addition (Cuprat).svg|centrado|300px|Adición 1,4 de un dialquilcuprato de litio a una [[enona]]]] |
||
A menudo sólo reacciona un grupo orgánico R por cada molécula de diorganocuprato de litio. En estos casos, si el reactivo de partida es valioso, se recurre a cupratos mixtos R<sub>T</sub>R<sub>R</sub>CuLi, de tal forma que sólo se transfiere el grupo R<sub>T</sub> que nos interesa, sin desaprovechar reactivo de partida, mientras que el grupo R<sub>R</sub> queda retenido de forma selectiva, ya que interacciona fuertemente con el átomo de cobre. El grupo R<sub>R</sub> puede ser, por ejemplo, CN<sup>−</sup>, Ph-S<sup>−</sup>, R-C≡C<sup>−</sup>, <sup>t</ |
A menudo sólo reacciona un grupo orgánico R por cada molécula de diorganocuprato de litio. En estos casos, si el reactivo de partida es valioso, se recurre a cupratos mixtos R<sub>T</sub>R<sub>R</sub>CuLi, de tal forma que sólo se transfiere el grupo R<sub>T</sub> que nos interesa, sin desaprovechar reactivo de partida, mientras que el grupo R<sub>R</sub> queda retenido de forma selectiva, ya que interacciona fuertemente con el átomo de cobre. El grupo R<sub>R</sub> puede ser, por ejemplo, CN<sup>−</sup>, Ph-S<sup>−</sup>, R-C≡C<sup>−</sup>, <sup>t</sup>BuO<sup>−</sup>, etc. No todos presentan la misma selectividad, y reactividad, ante distintos sustratos, siendo según el caso unos más adecuados que otros. |
||
== Bibliografía == |
== Bibliografía == |
||
| Línea 39: | Línea 39: | ||
== Véase también == |
== Véase también == |
||
*[[Reactivo de Grignard|Reactivos de Grignard]] |
* [[Reactivo de Grignard|Reactivos de Grignard]] |
||
*[[ |
* [[Organolitio|Compuestos organolíticos]] |
||
{{Control de autoridades}} |
|||
[[Categoría:Química orgánica]] |
|||
[[Categoría:Compuestos organometálicos]] |
[[Categoría:Compuestos organometálicos]] |
||
[[Categoría:Compuestos de litio]] |
[[Categoría:Compuestos de litio]] |
||
[[Categoría:Compuestos de cobre]] |
[[Categoría:Compuestos de cobre]] |
||
[[Categoría:Epónimos relacionados con la química]] |
|||
[[en:Gilman reagent]] |
|||
[[ja:ギルマン試薬]] |
|||
[[pl:Odczynnik Gilmana]] |
|||
[[zh:吉爾曼試劑]] |
|||
Revisión actual - 17:53 25 oct 2021
Un reactivo de Gilman, o diorganocuprato de litio, es un compuesto organocúprico de fórmula R2CuLi, donde R puede ser un alquilo, un vinilo o un arilo. Recibe su nombre por el químico estadounidense Henry Gilman.
Síntesis
[editar]Se preparan, dada su inestabilidad, por transmetalación a partir de un reactivo organolítico y una sal cuprosa (cobre(I)):
- RLi + CuX → RCu + LiX
- RCu + RLi → R2CuLi
Aplicaciones
[editar]Tienen aplicaciones en síntesis orgánica. No son básicos y toleran la presencia de los grupos hidroxilo y carboxilo, además de no reaccionar tampoco ni con cetonas ni ésteres, aunque sí lo hacen con el grupo carbonilo de aldehídos no conjugados. Su reactividad consiste en:
- Creación de enlaces C-C mediante procesos de sustitución. Por ejemplo, sustitución del átomo de halógeno por el grupo R en organohalógenos:
- R2CuLi + 2 R'X → 2 R-R' + CuX + LiX
donde R' puede ser un alquilo, un vinilo o un arilo.
- R2CuLi + 2 CH2=CH-CH2X → 2 R-CH2-CH=CH2 + CuX + LiX
- Apertura de epóxidos, para dar alcoholes.
- Sustitución nucleófila acílica sobre haluros de acilo para dar cetonas.
- Adiciones conjugadas, sobre aldehídos, cetonas y ésteres α,β-insaturados, y ciclopropanos activados (electrófilos).
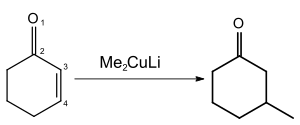
A menudo sólo reacciona un grupo orgánico R por cada molécula de diorganocuprato de litio. En estos casos, si el reactivo de partida es valioso, se recurre a cupratos mixtos RTRRCuLi, de tal forma que sólo se transfiere el grupo RT que nos interesa, sin desaprovechar reactivo de partida, mientras que el grupo RR queda retenido de forma selectiva, ya que interacciona fuertemente con el átomo de cobre. El grupo RR puede ser, por ejemplo, CN−, Ph-S−, R-C≡C−, tBuO−, etc. No todos presentan la misma selectividad, y reactividad, ante distintos sustratos, siendo según el caso unos más adecuados que otros.
Bibliografía
[editar]- K. Peter C. Vollhardt (1994). Química Orgánica. Barcelona: Ediciones Omega S.A. ISBN 84-282-0882-4.
