Diferencia entre revisiones de «Ácido orselínico»
mSin resumen de edición |
m web no disponible, cambiada a la versión que guarda TheWaybackMachine de archive.org |
||
| Línea 99: | Línea 99: | ||
== Bioquímica== |
== Bioquímica== |
||
En el ciclo metabólico, el producto se produce a través de la vía de biosíntesis de policétidos: una acil-coenzima A activada ([[acetil-CoA]] generalmente), forma un tetracétido y luego se cicla.<ref>{{cita publicación|apellido=Klaus Mosbach|título=Die Biosynthese der Orsellinsäure und Penicillinsäure (I)|publicación=Acta Chem. Scand.|año=1960|volumen=14|páginas=457–464|url=http://actachemscand.dk/pdf/acta_vol_14_p0457-0464.pdf PDF}}</ref> |
En el ciclo metabólico, el producto se produce a través de la vía de biosíntesis de policétidos: una acil-coenzima A activada ([[acetil-CoA]] generalmente), forma un tetracétido y luego se cicla.<ref>{{cita publicación|apellido=Klaus Mosbach|título=Die Biosynthese der Orsellinsäure und Penicillinsäure (I)|publicación=Acta Chem. Scand.|año=1960|volumen=14|páginas=457–464|url=https://web.archive.org/web/20160402233258/http://actachemscand.dk/pdf/acta_vol_14_p0457-0464.pdf PDF}}</ref> |
||
[[Archivo:Orsellinsäure is.svg|miniatura|derecha|400px|Biosíntesis de ácidos orselínicos a partir de [[policétido]]s]] |
[[Archivo:Orsellinsäure is.svg|miniatura|derecha|400px|Biosíntesis de ácidos orselínicos a partir de [[policétido]]s]] |
||
Revisión del 20:16 3 feb 2024
| ácido orselínico | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| ácido 2,4-dihidroxi-6-metilbenzoico | ||
| General | ||
| Otros nombres | ácido o-orselínico | |
| Fórmula molecular | C8H8O4 | |
| Identificadores | ||
| Número CAS | 480-64-8[1] | |
| ChEMBL | CHEMBL457583 | |
| KEGG | C01839 | |
| Propiedades físicas | ||
| Masa molar | 16 814 g/mol | |
| Punto de fusión | 175 °C (448 K) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ácido orselínico, o más concretamente ácido o-orselínico, es un ácido fenólico. Es de importancia en la bioquímica de los líquenes y de especies como Aspergillus y Penicillium[2] de los que se puede aislar. En estos organismos, la biosíntesis del ácido orselínico ocurre a través de la vía del policétido.[3]
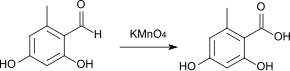
Química
Se puede preparar mediante la oxidación del aldehído correspondiente:[4]
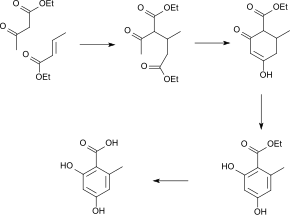
Otra síntesis, se consigue por adición de Michael de acetoacetato de etilo a crotonato de etilo (trans-2-butenoato de etilo) seguida de una condensación de Claisen intramolecular. Aquí, forma el éster de etilo del ácido orsenílico dihidrogenado. La deshidrogenación y escisión del éster da el ácido orselínico.
Bioquímica
En el ciclo metabólico, el producto se produce a través de la vía de biosíntesis de policétidos: una acil-coenzima A activada (acetil-CoA generalmente), forma un tetracétido y luego se cicla.[5]

Propiedades
El ácido orselínico forma cristales incoloros en forma de agujas. Se descompone por calentamiento a 176 °C y se descarboxila con ello dando lugar a orcinol.
Referencias
- ↑ Número CAS
- ↑ G. W. Eijk (1969). «Isolation and identification of orsellinic acid and penicillic acid produced by Penicillium fennelliae Stolk». Antonie van Leeuwenhoek 35: 497-504. doi:10.1007/BF02219167.
- ↑ Nolan, T. J.; Keane, J.; Davidson, V. E. (1940). «Chemical constituents of the lichen Parmelia latissima Fee». Scientific Proceedings of the Royal Dublin Society, Series A 22: 237-239.
- ↑ Kurt Hoesch (1913). «Synthese der Orsellinsäure und der Everninsäure». Berichte der deutschen chemischen Gesellschaft 46: 886-892. doi:10.1002/cber.191304601116.
- ↑ Klaus Mosbach (1960). PDF «Die Biosynthese der Orsellinsäure und Penicillinsäure (I)». Acta Chem. Scand. 14: 457-464.