Diferencia entre revisiones de «Carpaína»
Sin resumen de edición |
Sin resumen de edición |
||
| Línea 12: | Línea 12: | ||
}} |
}} |
||
[[Imagen:Koeh-029.jpg|izquierda|200px|thumb|Papaya (''[[Carica papaya]]'')]] |
|||
La '''carpaína''' es un [[alcaloide]] aislado de las hojas de papaya (''[[Carica papaya]]'')<ref>Greshoff, M.Ber., 1890, 23, 3537</ref>, las cuales han sido estudiadas por sus efectos cardiovasculares.<ref>Burdick, Everette M. "Carpaine. An alkaloid of Carica papaya. Chemistry and pharmacology." ''Economic Botany'' (1971), 25(4), 363-365.</ref> Es un homólogo de la [[azimina]]. Es un agente cardiotónico. [α]<small>D</small> = +21.65 (c, 1.0 en EtOH); es soluble en metanol y benceno. Probablemente se forma ''in vivo'' por la dimerización del [[ácido carpámico]]<ref>Coke, J.L. et al., JOC, 1965, 30, 3420</ref>. |
La '''carpaína''' es un [[alcaloide]] aislado de las hojas de papaya (''[[Carica papaya]]'')<ref>Greshoff, M.Ber., 1890, 23, 3537</ref>, las cuales han sido estudiadas por sus efectos cardiovasculares.<ref>Burdick, Everette M. "Carpaine. An alkaloid of Carica papaya. Chemistry and pharmacology." ''Economic Botany'' (1971), 25(4), 363-365.</ref> Es un homólogo de la [[azimina]]. Es un agente cardiotónico. [α]<small>D</small> = +21.65 (c, 1.0 en EtOH); es soluble en metanol y benceno. Probablemente se forma ''in vivo'' por la dimerización del [[ácido carpámico]]<ref>Coke, J.L. et al., JOC, 1965, 30, 3420</ref>. |
||
Revisión del 07:19 15 ene 2013
| Carpaína | ||
|---|---|---|
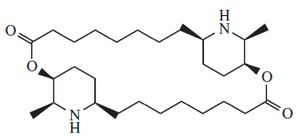 | ||
| Nombre IUPAC | ||
|
(1S,11R,13S,14S,24R,26S)-13,26-Dimetil-2,15-dioxa- 12,25-diazatriciclo[22.2.2.211,14]triacontano-3,16-diona | ||
| General | ||
| Fórmula estructural |
 | |
| Fórmula molecular | C28H50N2O4 | |
| Identificadores | ||
| Número CAS | 3463-92-1[1] | |
| ChEBI | 3433 | |
| ChemSpider | 390994 | |
| PubChem | 442630 | |
| UNII | VLR223H4QP | |
| KEGG | C10135 | |
| Propiedades físicas | ||
| Apariencia | Cubos (Éter)[2] | |
| Masa molar | 478,714 g/mol | |
| Punto de fusión | 119 °C (392 K) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||

La carpaína es un alcaloide aislado de las hojas de papaya (Carica papaya)[3], las cuales han sido estudiadas por sus efectos cardiovasculares.[4] Es un homólogo de la azimina. Es un agente cardiotónico. [α]D = +21.65 (c, 1.0 en EtOH); es soluble en metanol y benceno. Probablemente se forma in vivo por la dimerización del ácido carpámico[5].
Actividad biológica
Los efectos circulatorios de la carpaína fueron estudiados en ratas [6] Al incrementar las dosis de carpaina desde 0.5 mg/kg a 2.0 mg/kg se observó una disminución progresiva en las presiones arterial, diastólica y sistólica. El bloqueo selectivo de los nervios autónomos con sulfato de atropina (1 mg/kg) o con clorhidrato de propranolol (8 mg/kg) no alteró dla respuesta circulatoria de la carpaína. A una dosis de 2 mg/kg, la carpaína reduce el gasto cardiaco sin alterar la resistencia periférica. De estas observaciones se concluyó que la carpaína actúa directamente sobre el miocardio. Los efectos de la carpaína pueden estar relacionados con su estructura macrocíclica y con su capacidad para quelatar metales.
Derivados
Otros derivados de la carpaína han sido aislados de las hojas de papaya:
| Nombre | Estructura | Fórmula molecular | CAS | Masa molecular (g/mol) | Estado | Otras propiedades |
|---|---|---|---|---|---|---|
| Deshidrocarpaína I[7] |  |
C28H48N2O4 | 72362-02-8 | 476.698 | Aceite viscoso | |
| Deshidrocarpaína II [8] |  |
C28H46N2O4 | 72362-03-9 | 474.682 | Aceite viscoso | |
| Pseudocarpaína (ψ-Carpaína)[9] |  |
C28H50N2O4 | 3760-91-6 | 478.714 | Cristalino. PF = 65 - 68°C | [α]28D = +4.95 (c, 1.62 en EtOH) |
Referencias
- ↑ Número CAS
- ↑ Kabaleeswaran, V. et al., Acta Cryst. C, 1999, 55, 1935- 1937
- ↑ Greshoff, M.Ber., 1890, 23, 3537
- ↑ Burdick, Everette M. "Carpaine. An alkaloid of Carica papaya. Chemistry and pharmacology." Economic Botany (1971), 25(4), 363-365.
- ↑ Coke, J.L. et al., JOC, 1965, 30, 3420
- ↑ Hornick, C. A.; Sanders, L. I.; Lin, Y. C. "Effect of carpaine, a papaya alkaloid, on the circulatory function in the rat." Research Communications in Chemical Pathology and Pharmacology (1978), 22(2), 277-289.
- ↑ Topuriya, L.I. et al., Chem. Nat. Compd. (Engl. Transl.), 1978, 354
- ↑ Tang, C.-S.Phytochemistry, 1979, 18, 651
- ↑ Govindachari, T.R. et al., JCS, 1954, 1847; 1955, , 1563
