Diferencia entre revisiones de «Cannabinoide»
m Revertidos los cambios de 181.117.216.180 (disc.) a la última edición de 90.68.90.142 Etiqueta: Reversión |
Sin resumen de edición |
||
| Línea 134: | Línea 134: | ||
Muchos son almacenados en la grasa además de ser metabolizados en el hígado. |
Muchos son almacenados en la grasa además de ser metabolizados en el hígado. |
||
Δ-9-THC (neurotrasmisor delta 9 THC) es metabolizado a 11-hidroxi-Δ-9-THC para posteriormente convertirse en 9-carboxi-THC. Muchos metabolitos del cannabis pueden ser detectados en el organismo después de varias semanas. |
Δ-9-THC (neurotrasmisor delta 9 THC) es metabolizado a 11-hidroxi-Δ-9-THC para posteriormente convertirse en 9-carboxi-THC. Muchos metabolitos del cannabis pueden ser detectados en el organismo después de varias semanas. |
||
Tras los resultados obtenidos por investigadores como el Dr. Ben Shabat (1998) o Ethan Russo (2001, 2011), se cree que el efecto de los cannabinoides en el organismo puede ser modulado por otros compuestos también secretados por el cannabis - las moléculas aromáticas llamadas terpenos - en lo que se conoce como efecto séquito.<ref>SC Labs, [https://www.sclabs.com/beyond-aroma-terpenes-in-cannabis/ Beyond aroma: Terpenes in cannabis]</ref> |
|||
==== Síntesis de la planta ==== |
==== Síntesis de la planta ==== |
||
Revisión del 09:40 3 dic 2018
Un cannabinoide es un compuesto orgánico perteneciente al grupo de los terpenofenoles, activa los receptores cannabinoides en el organismo humano.[1] La forma plural cannabinoides originalmente aludía al particular grupo de metabolitos secundarios encontrados en la planta de cannabis, responsable de los efectos farmacológicos característicos de la planta.
Tipos
Actualmente, se reconocen tres tipos generales de cannabinoides: los cannabinoides herbarios o fitocannabinoides sintetizados naturalmente por la planta de cannabis; los cannabinoides endógenos, producidos por organismos animales y por el cuerpo humano (e.g., anandamidas.); y los cannabinoides sintéticos, compuestos similares generados en laboratorio.
Uno de los cannabinoides más conocidos es el THC (tetrahidrocannabinol), ingrediente psicoactivo de la marihuana. Sin embargo, la medicina institucional se ha interesado últimamente por otros cannabinoides menos renombrados, dotados de propiedades analgésicas únicas, que están siendo intensamente investigados.
Los cannabinoides actúan a través de dos tipos de receptores, los CB1 que se encuentran en el sistema nervioso central y en los sistemas reproductivo, digestivo e inmune y los CB2 que se encuentran en tejidos periféricos como pulmón, bazo y testículos, así como en algunas células del sistema inmune como los monocitos y los macrófagos. El receptor transmembrana CB1 estaría asociado a las GPi (proteínas G inhibitorias) y al activarse se produciría un bloqueo de la entrada de calcio hacia las células así como la inhibición de la adenilato ciclasa con la consecuente disminución de la concentración intracelular de AMPc (una molécula que funciona como señalizadora o segundo mensajero en distintas vías enzimáticas intracelulares). Los receptores CB2 aparentemente actúan de forma muy parecida a los CB1.
Usos terapéuticos
Entre los usos terapéuticos de los cannabinoides se mencionan el tratamiento del dolor neuropático en pacientes terminales como en el cáncer metastásico, de los vómitos inducidos por quimioterapia y en el síntoma de la espasticidad de la esclerosis múltiple, y en las nauseas y vómitos intratables post quimioterapia del cáncer. Otros usos se encuentran actualmente en investigación clínica (Ej: convulsiones refractarias en niños, glaucoma)
Receptores de cannabinoides
Antes de 1980, hubo mucha especulación sobre los efectos producidos sobre el físico y la psique a través de vía inespecífica en las membranas celulares por parte de los cannabinoides. El descubrimiento del primer receptor de cannabinoides en los años ochenta ayudó a resolver este debate. Estos receptores eran comunes en animales y fueron encontrados en mamíferos, aves, peces y reptiles. Actualmente hay dos tipos conocidos de receptores: el CB1 y el CB2.[2]
Receptores de cannabinoides tipo 1 (CB1)
Los receptores CB1 fueron encontrados por primera vez en el cerebro, específicamente en los ganglios basales y en el sistema límbico. También fueron encontrados en el cerebelo y en los sistemas de reproducción de machos y hembras. Los receptores de CB1 están ausentes en la parte del tallo cerebral responsable de las funciones cardiovasculares y respiratorias. En consecuencia no hay riesgo de fallo cardiorrespiratorio como sucede con otras drogas. Los CB1 aparecen como responsables de la euforia y de los efectos anticonvulsivos del cannabis.
Receptores de cannabinoides tipo 2 (CB2)
Los receptores de tipo 2 (CB2) se encuentran casi exclusivamente en el sistema inmunitario, con una gran cantidad en el bazo. Los CB2 son los responsables de la acción antiinflamatoria.
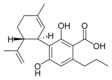
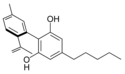
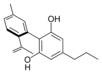
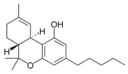
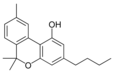
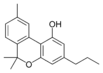
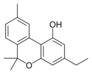
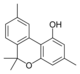
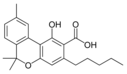
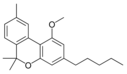
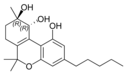
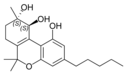
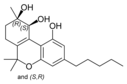
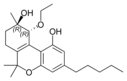
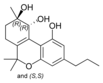
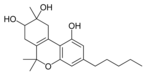
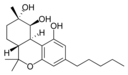
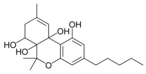
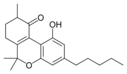
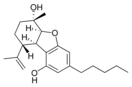
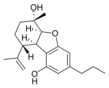
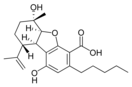
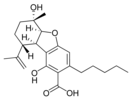
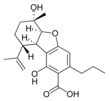
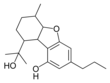
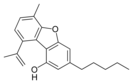
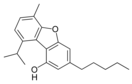
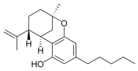
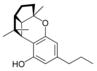
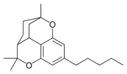
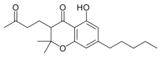
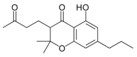
Fitocannabinoides
| Tipo | Estructura | Forma Ciclada |
|---|---|---|
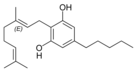
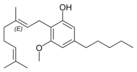
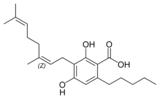
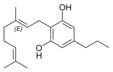
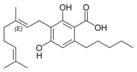
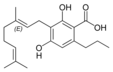
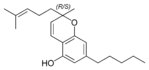
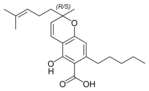
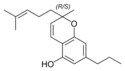
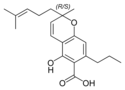
| Cannabigerol-type CBG |

|

|
| Cannabichromene-type CBC |

|

|
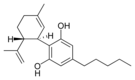
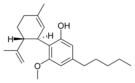
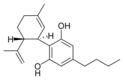
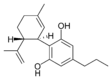
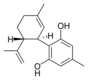
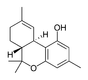
| Cannabidiol-type CBD |

|

|
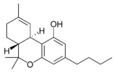
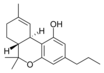
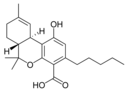
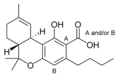
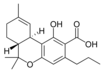
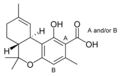
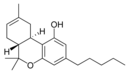
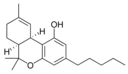
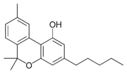
| Tetrahydrocannabinol- and Cannabinol-type THC, CBN |

|

|
| Cannabielsoin-type CBE |

|

|
| iso- Tetrahydrocannabinol- type iso-THC |

|

|
| Cannabicyclol-type CBL |

|

|
| Cannabicitran-type CBT |

|

|
| Principales de cannabinoides naturales | ||
También se les llama cannabinoides naturales, cannabinoides herbáceos o cannabinoides clásicos. Son conocidos únicamente porque se producen en una cantidad significativa en la planta de cannabis y están concentrados en una savia viscosa que se produce en estructuras glandulares conocidas como tricomas. Además la savia es rica en terpenos, los cuales son responsables del aroma de la planta. Los fitocannabinoides son bastante insolubles en agua pero muy solubles en lípidos, alcoholes y otros disolventes orgánicos apolares.
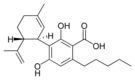
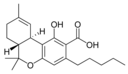
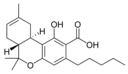
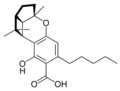
Todos los cannabinoides naturales son derivados de sus respectivos 2-acidocarboxílico(2-COOH) por descarboxilación (catalizada por calor, luz y condiciones alcalinas).
Tipos
Hasta el momento se han identificado al menos 113 cannabinoides procedentes de la planta de cannabis.[3] Todas las clases derivan de compuestos del tipo cannabigerol y difieren principalmente en el proceso mediante el cual el precursor es ciclado.
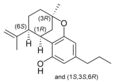
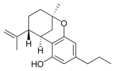
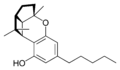
Tetrahidrocannabinol(THC), cannabidiol (CBD) y cannabinol(CBN) son los cannabinoides más frecuentes y los que han sido objetivo de más estudios. Hay más cannabinoides que han sido estudiados:
- CBG Cannabigerol
- CBC Cannabichromene
- CBL Cannabiciclol
- CBV Cannabidivarin
- CBCV Cannabichromevarin
- CBGV Cannabigerovarin
- CBGM Cannabigerol Monoetil éter
Tetrahidrocannabinol
El THC es el componente psicoactivo primario de la planta. Desde un punto de vista clínico, es útil para aliviar el dolor moderado pues posee un efecto analgésico además de ser neuroprotector. El tetrahidrocannabinol tiene aproximadamente la misma afinidad por el CB1 que por el CB2.[4]
Δ-9-tetrahidrocannabinol y Δ-8-tetrahidrocannabinol, imitan la acción de la anandamida, un neurotransmisor producido de forma natural en el organismo. El THC produce el “subidón” asociado al cannabis a causa del enlace con el receptor CB1 del cerebro.
Diversos estudios han propuesto los posibles efectos beneficiosos del THC en la enfermedad de Alzheimer, declarando que el THC puede reducir la actividad de la enzima acetilcolinesterasa, mejorando la transición colinérgica e impidiendo el desarrollo de la enfermedad. [5]
Cannabidiol
El cannabidiol es un narcótico o estupefaciente, pero no se considera un psicoactivo y se cree que no afecta a la actividad llevada a cabo por el THC.[6] Recientemente se han hallado evidencias que demuestran que los fumadores de cannabis con una alta proporción de CBD/THC poseen menos tendencia a sufrir los síntomas[7] de la esquizofrenia. Este hecho está apoyado por tests psicológicos en los cuales los participantes experimentan una pérdida de intensidad de los efectos psicóticos cuando se les administra THC junto a CBD. Esto nos conduce a la hipótesis que el CBD actúa como antagonista alostérico del CB1 y en consecuencia altera los efectos psicoactivos del THC. Médicamente, el CBD parece responsable del alivio de las convulsiones en epilepsias refractarias, inflamaciones, dolor crónico, ansiedad y náuseas.[8] Actualmente están realizándose varios estudios médicos donde se están encontrando resultados a favor del potencial terapéutico del cannabidiol.[9] El cannabidiol tiene una gran afinidad por el receptor de CB2, por el contrario por el CB1 no tanta. El cannabidiol comparte precursor con el THC.
Cannabinol
El cannabinol (CBN) es el producto primario de la degradación del THC y no se suele encontrar demasiado en la planta. El contenido en CBN va aumentando según la cantidad de THC que se degrada y por la exposición a la luz y al aire. Es un psicoactivo leve cuya afinidad es superior en el caso del receptor CB2 y baja en el CB1.[10]
Tetrahidrocannabivarina
La tetrahidrocannabivarina (THCV) es común en ciertas variedades de la planta de cannabis de Sudáfrica y del sudeste asiático. Es un antagonista del THC y en los receptores de CB1 atenúa el efecto psicoactivo del THC.[11]
Cannabicromeno
El cannabicromeno (CBC) no es un psicoactivo y no influye en el efecto del THC.[6]
Posición del doble enlace
Cada uno de estos compuestos puede tener distintas formas dependiendo de la posición del doble enlace en el anillo acíclico del carbono. Esto puede comportar confusión porque hay diferentes sistemas para numerar y describir la posición del doble enlace.
Longitud
Muchos compuestos formados de cannabinoides herbáceos están constituidos por 21 carbonos. Sin embargo, muchos no siguen esta regla a causa de la variación en la longitud de la cadena ligada al anillo aromático. En el caso del THC, CBD y del CBN esta cadena es un pentilo(5 carbonos). En la mayoría de los homólogos, la cadena pentilo es sustituida por un propilo (3 carbonos). A los cannabinoides con un propilo se les da nombre empleando el sufijo “varina”. Ejemplos: THCV, CBDV, CBNV. Estas cadenas son más estrechas pero aumentan la intensidad y disminuyen la duración de las actividades de las sustancias químicas.
Perfil de la planta

La planta de cannabis puede presentar grandes variaciones respecto al tipo y cantidad de cannabinoides que sintetiza. La mezcla de cannabinoides producidos por la planta también es conocida como: perfil de la planta de los cannabinoides. El cultivo selectivo ha sido utilizado para controlar la genética de las plantas y de esta forma modificar el perfil de los cannabinoides. Hay variedades utilizadas en medicina por su alto contenido en CBD como por ejemplo la Cannabis Sativa L, otras son utilizadas con propósitos recreativos en busca de un alto contenido en THC.
El análisis cuantitativo del perfil de una planta productora de cannabinoides se determina mediante una cromatografía gaseosa (CG). Se sabe que se combina con una espectrometría masiva. Las cromatografías liquidas también son posibles aunque normalmente son semi-cuantitativas y semi-cualitativas.
Farmacología
Los cannabinoides se pueden administrar fumándolos, por vaporización, ingestión oral, inyección intravenosa, absorción sublingual o con supositorios. Una vez dentro del organismo, muchos cannabinoides son metabolizados en el hígado. Muchos son almacenados en la grasa además de ser metabolizados en el hígado. Δ-9-THC (neurotrasmisor delta 9 THC) es metabolizado a 11-hidroxi-Δ-9-THC para posteriormente convertirse en 9-carboxi-THC. Muchos metabolitos del cannabis pueden ser detectados en el organismo después de varias semanas. Tras los resultados obtenidos por investigadores como el Dr. Ben Shabat (1998) o Ethan Russo (2001, 2011), se cree que el efecto de los cannabinoides en el organismo puede ser modulado por otros compuestos también secretados por el cannabis - las moléculas aromáticas llamadas terpenos - en lo que se conoce como efecto séquito.[12]
Síntesis de la planta
La producción de cannabinoides comienza cuando una enzima causa la combinación del geranil pirofosfato y ácido olivetolico para formar CBG. Después, el CBG se transforma de forma independiente en CBD o CBC por dos enzimas sintetasas que se hallan separados. Posteriormente el CBD se cicla por acción de enzimas. Para los homólogos del propilo (THCV, CBDV y CBNV) se lleva a cabo el mismo proceso pero basado en CBGV.
Separación
Los cannabinoides pueden ser separados de la planta por extracción con disolventes orgánicos. Los hidrocarburos y los alcoholes son muy utilizados como disolventes pero debemos tener en cuenta que son inflamables y muy tóxicos. La extracción supercrítica con dióxido de carbono es una técnica alternativa. Aunque este proceso requiera altas presiones (73 atmósferas), hay un mínimo riesgo de incendio o de toxicidad. La retirada del disolvente es simple y eficiente. Una vez extraído, la mezcla de cannabinoides puede ser separada en componentes individuales usando técnicas de destilación. Se ha de tener en cuenta que para producir cannabinoides es necesaria una síntesis química.
Historia
Los cannabinoides fueron descubiertos en la década de 1940, cuando CBD y CBN fueron identificados. La estructura del THC fue determinada por primera vez en 1964 por el profesor Raphael Mechoulam, sintetizando la molécula Δ9-tetrahidrocannabinol. Debido al parecido molecular y la facilidad de la conversión sintética, en un principio se pensó que el CBD era un precursor natural del THC. Sin embargo, hoy en día se sabe que el CBD y el THC son producidos de manera independiente en la planta del cannabis y que tienen un caracter antagónico.
Endocannabinoides

La anandamida es un ligando endógeno del CB1 y el CB2.
Los endocannabinoides son substancias que se producen en el interior del cuerpo, los cuales activan los receptores de cannabinoides. Tras el descubrimiento del primer receptor de cannabinoide en 1988, algunos científicos empezaron a buscar un ligando endógeno para el receptor.
Tipos de ligandos de endocannabinoides
- Araquidonoiletanolamina (Anandamida o AEA)
En 1992, el primer componente descubierto fue identificado como araquidonoiletanolamina y llamado anandamida, un nombre derivado de la palabra dicha en Sánscrito y –amida. Anandamida es un derivado del ácido graso esencial (separado en el link) araquidónico. Es farmacológicamente hablando similar al THC, aunque su estructura química es diferente. La anandamida se une al receptor de cannabinoides CB1 y, en menor grado al receptor CB2, dónde actúa como un agonista parcial. Es tan potente como el THC en el receptor CB1.[13]Se encuentra en la mayoría de tejidos de un amplio abanico de animales.[14]
Dos formas análogas de la anandamida, el 7,10,13,16-docosatetraenoiletanolamida y el homo-y-linolenoiletanolamina, tienen similar farmacología. Todos ellos son miembros de una familia de señales lipídicas llamadas N-aciletanolamidas, que también incluyen los no cannabi-miméticos palmitoiletanolamida y oleiletanolamina, los cuales poseen efectos antiinflamatorios y orexigénico, respectivamente. Muchas N-aciletanolaminas han sido identificadas también en semillas[15]y moluscos.[16]
- 2–Araquidonoilglicerol
Otro endocannabinoide, 2–Araquidonoilglicerol, se une a los receptores CB1 y CB2 con afinidad similar, actuando como un agonista total de ambos.[13][17] 2–AG está presente en concentraciones significativamente más altas en el cerebro que la anandamida, y existe cierta controversia en relación a si 2–AG, en lugar de anandamida, es el principal responsable de la señalización por endocannabinoides in vivo.[18] En particular, un estudio in Vitro sugiere que 2-AG es capaz de estimular la activación de la proteína G en mayor grado que la anandamida, aunque las implicaciones psicológicas de este hallazgo no son aún conocidas[19] .
- 2-Araquidonilgliceril eter (noladin éter)
En 2001 se aisló un tercer tipo de endocannabinoide, el 2-Araquidonil gliceril eter, de un cerebro porcino.[20] Antes de este descubrimiento, había sido sintetizado artificialmente como un análogo estable del 2-AG; es más, existe cierta controversia sobre una clasificación como un endocannabinoide, ya que se encontró una “cantidad inapreciable” de dicha sustancia en los cerebros de una gran cantidad de especies de mamíferos diferentes.[21]
Se une al receptor CB1 (Ki=21,2 nmol/L) y causa sedación, hipotermia, inmovilidad intestinal y un suave efecto antinociceptivo en ratones. Se une fuertemente al receptor CB1, y sólo débilmente al receptor CB2[13]
- N-Araquidonoil-dopamina (NADA)
Descubierto en el 2000, NADA se une preferentemente al receptor CB1.[22]Como la anandamida, NADA es también un agonista del subtipo 1 de receptor de vanilloides (TRPV1), un miembro de la familia de receptores vanilloides.[23][24]
- Virodamina
Un quinto cannabinoide, virodamina, o O-araquidonoil-etanolamina (OAE) fue descubierto en junio de 2002. Aunque es un agonista total del receptor CB2 y un agonista parcial del CB1, en el receptor CB1 se comporta como un antagonista si se encuentra en una situación in vivo. En ratas, virodhamina estaba presente en concentraciones ligeramente inferiores que la anandamida en el cerebro.[25]
Función
Los endocannabinoides funcionan como mensajeros intercelulares lipídicos, señalando moléculas que son secretadas en una célula y activando los receptores de cannabinoides presentes en otras células de alrededor. Aunque en este rol de señalización intercelular se comportan de manera similar a los ya conocidos neurotransmisores monoamina, como la dopamina o la acetilcolina, los endocannabinoides difieren de muchas maneras de ellos. Por ejemplo, utilizan señalización retrógrada. Además, los endocannabinoides son moléculas lipofílicas, por lo tanto no son demasiado solubles en agua. No se guardan en vesículas, y existen como componentes integrales de la bicapa lipídica que constituye la membrana de las células. Se cree que son sintetizados por demanda en vez de ser sintetizados y luego almacenados para un uso posterior. Los mecanismos y enzimas que hay bajo la biosíntesis de los endocannabinoides aun constituyen un área de investigación activa.
El endocannabinoide 2-AG ha sido encontrado en leche materna tanto humana como bovina.[26]
Señal retrógrada
Los neurotransmisores convencionales son liberados de una célula pre-sináptica, y activados por receptores apropiados en una célula post-sináptica, dónde pre-sináptico y post-sináptico designan las zonas de envío y recibo de la sinapsis, respectivamente. Los endocannabinoides, por otro lado, son descritos como transmisores retrógrados porque normalmente viajan “hacia atrás”, en contra de la corriente sináptica común. Ellos, en efecto, son liberados de la célula post-sináptica y activados en la célula pre-sináptica, donde los receptores señal se encuentran densamente concentrados en los terminales axónicos, en zonas desde las cuales los neurotransmisores convencionales son a su vez liberados. Este sistema de tráfico mediado por endocannabinoides permite a la célula post-sináptica controlar su propia entrada de tráfico sináptico. El efecto último en la célula liberadora de endocannabinoides depende de la naturaleza del transmisor convencional que está siendo controlado. Por ejemplo, cuando la liberación de un transmisor inhibidor, como GABA, es reducida, el efecto neto es un incremento de la excitabilidad de la célula liberadora de endocannabinoides. En contra, cuando la liberación de un neurotransmisor excitador, como el glutamato, es reducida, el efecto neto es la disminución de la excitabilidad de la célula liberadora de endocannabinoides.
Rango
Los endocannabinoides son moléculas hidrofóbicas: no pueden viajar sin ayuda largas distancias por el medio acuoso que envuelve las células de las cuales son liberadas, y por tanto actúan de forma local cerca de las células diana. Por esta razón, aunque emanen difusamente de las células fuente, tienen un área de influencia mucho más restringida que las hormonas, lo cual afecta a células por todo el cuerpo.
Curiosidades
Los endocannabinoides constituyen un sistema versátil para afectar las propiedades de la red neuronal en el sistema nervioso.
Scientific American publicó un artículo en diciembre de 2004, titulado “The Brain’s Own Marijuana” dónde se discutía el sistema endógeno cannabinoide.[27] El actual entendimiento reconoce el rol que los endocannabinoides juegan en prácticamente todas las funciones importantes del cuerpo humano.
Patente #6630507 U.S
En el año 2003, el gobierno de U.S. representado por el Departamento de Salud y Servicios Humanos (Department of Health and Human Services) presentó la solicitud de patente, la cual fue concedida para cannabinoides como antioxidantes y neuroprotectores. U.S. Patent 6630507.
Cannabinoides sintéticos y patentados
Históricamente, la síntesis de cannabinoides en los laboratorios se basaba usualmente en la estructura de los cannabinoides herbarios y un largo número de análogos que han sido producidos y testados, especialmente en un grupo liderado por Roger Adams desde 1941, y más tarde en un grupo liderado por Raphael Mechoulam. Los componentes más nuevos no se relacionan con los cannabinoides naturales ni están basados en la estructura de los cannabinoides endógenos.
Los cannabinoides sintéticos son particularmente útiles en experimentos para determinar la relación entre la estructura y la actividad de los componentes de los cannabinoides, haciendo sistemáticas e incrementales modificaciones en las moléculas de cannabinoides.
Medicamentos que contienen cannabinoides sintéticos, naturales o análogos de cannabinoides:
- Dronabinol (Marinol) es un (delta)9-tetrahidrocannabinol (THC), que se usa como un estimulante del apetito, analgésico y antiemético.
- Nabilone (Cesamet), un cannabinoide sintético y un análogo del Marinol.
- Sativex, un cannabinoide que se aplica en un spray que contiene THC; CBD y otros cannabinoides utilizados para el dolor neuropático y espástico en Canadá y España. Sativex crea todas la medicinas que proceden de la planta cannabinoide.
- Rimonabant (SR141716), un cannabinoide selectivo (CB1) receptor antagonista usado como una droga antiobesidad bajo el nombre de Acomplia. También se utiliza para los tratamientos para dejar de fumar.
Otros cannabinoides sintéticos remarcables incluyen:
- CP-55940, producido en 1974, un receptor agonista cannabinoide sintético que muchas veces es más potente que el THC.
- Dimetilheptilpirano
- HU-210, 100 veces más potente que el THC.[28]
- HU-331, una potente droga anticáncer derivada del cannabidiol que inhibe específicamente la tipoisomerasa II
- SR144528, un receptor antagonista de CB2
- WIN 55,212-2, un potente receptor agonista de cannabinoide.
- JWH-133, un potente receptor agonista selectivo de CB2
- Levonantradol (Nantrodolum), un antiemético y analgésico que ya no se encuentra vigente en el campo de la medicina.
Tabla de cannabinoides naturales
Véase también
- Cannabis
- Tetrahidrocannabinol
- Cannabinoides
- Cannabidiol
- Endocanabinoides
- Neurotransmisor
- Anandamida
- Psicoactivo
- Instituto Weizmann de Ciencias
- Raphael Mechoulam
Referencias
- ↑ Lambert DM, Fowler CJ (2005). «The endocannabinoid system: drug targets, lead compounds, and potential therapeutic applications». J. Med. Chem. 48 (16): 5059-87. PMID 16078824. doi:10.1021/jm058183t.
- ↑ Begg M, Pacher P, Bátkai S, Osei-Hyiaman D, Offertáler L, Mo FM, Liu J, Kunos G (2005). «Evidence for novel cannabinoid receptors». Pharmacol. Ther. 106 (2): 133-45. PMID 15866316. doi:10.1016/j.pharmthera.2004.11.005.
- ↑ Aizpurua-Olaizola, Oier; Soydaner, Umut; Öztürk, Ekin; Schibano, Daniele; Simsir, Yilmaz; Navarro, Patricia; Etxebarria, Nestor; Usobiaga, Aresatz (2 de febrero de 2016). «Evolution of the Cannabinoid and Terpene Content during the Growth of Cannabis sativa Plants from Different Chemotypes». Journal of Natural Products (en inglés). doi:10.1021/acs.jnatprod.5b00949. Consultado el 18 de febrero de 2016.
- ↑ Huffman JW (2000). «The search for selective ligands for the CB2 receptor». Curr. Pharm. Des. 6 (13): 1323-37. PMID 10903395. doi:10.2174/1381612003399347.
- ↑ Alchimia Blog, ¿Marihuana contra la enfermedad de Alzheimer?
- ↑ a b «Behavioural Pharmacology - Abstract: Volume 16(5-6) September 2005 p 487-496 Neurophysiological and subjective profile of marijuana with varying concentrations of cannabinoids.». Consultado el 24 de junio de 2007.
- ↑ Morgan CJ, Curran HV (abril de 2008). «Effects of cannabidiol on schizophrenia-like symptoms in people who use cannabis». The British journal of psychiatry : the journal of mental science 192 (4): 306-7. PMID 18378995. doi:10.1192/bjp.bp.107.046649.
- ↑ «Should I Smoke Dope?». Consultado el 24 de mayo de 2008.
- ↑ «Cannabidiol y sus usos terapéuticos | Kalapa Clinic». www.kalapa-clinic.com. Consultado el 21 de febrero de 2017.
- ↑ Mahadevan A, Siegel C, Martin BR, Abood ME, Beletskaya I, Razdan RK (octubre de 2000). «Novel cannabinol probes for CB1 and CB2 cannabinoid receptors». Journal of medicinal chemistry 43 (20): 3778-85. PMID 11020293. doi:10.1021/jm0001572.
- ↑ «British Journal of Pharmacology - Abstract of article: Evidence that the plant cannabinoid Δ9-tetrahydrocannabivarin is a cannabinoid CB1 and CB2 receptor antagonist». Consultado el 24 de junio de 2007.
- ↑ SC Labs, Beyond aroma: Terpenes in cannabis
- ↑ a b c Grotenhermen F. "Cannabinoids." Current Drug Targets - CNS & Neurological Disorders. 2005 Oct;4(5):507-30. PMID 16266285
- ↑ Martin BR, Mechoulam R, Razdan RK (1999). «Discovery and characterization of endogenous cannabinoids». Life sciences 65 (6-7): 573-95. PMID 10462059. doi:10.1016/S0024-3205(99)00281-7.
- ↑ «N-Acylethanolamines in Seeds. Quantification of Molecular Species and Their Degradation upon Imbibition -- Chapman et al. 120 (4): 1157 -- PLANT PHYSIOLOGY». Consultado el 24 de junio de 2007.
- ↑ «ScienceDirect - Biochimica et Biophysica Acta (BBA) - Lipids and Lipid Metabolism : Bioactive long chain N-acylethanolamines in five species of edible bivalve molluscs: Possible implications for mollusc physiology and sea food industry». doi:10.1016/S0005-2760(97)00132-X. Consultado el 24 de junio de 2007.
- ↑ Stella N, Schweitzer P, Piomelli D. "A second endogenous cannabinoid that modulates long-term potentiation." Nature. 1997 Aug 21; 388(6644):773-8. PMID 9285589
- ↑ reviewed in Pacher P, Batkai S, Kunos G. "The endocannabinoid system as an emerging target of pharmacotherapy." Pharmacological Reviews. 2006 Sep;58(3):389-462. PMID 16968947
- ↑ Savinainen JR, Jarvinen T, Laine K, Laitinen JT. "Despite substantial degradation, 2-arachidonoylglycerol is a potent full efficacy agonist mediating CB(1) receptor-dependent G-protein activation in rat cerebellar membranes." British Journal of Pharmacology. 2001 Oct; 134(3):664-72. PMID 11588122
- ↑ Hanuš L, Abu-Lafi S, Fride E, et al. (2001). «2-arachidonyl glyceryl ether, an endogenous agonist of the cannabinoid CB1 receptor». Proc. Natl. Acad. Sci. U.S.A. 98 (7): 3662-5. PMID 11259648. doi:10.1073/pnas.061029898.
- ↑ Oka S, Tsuchie A, Tokumura A, Muramatsu M, Suhara Y, Takayama H, Waku K, Sugiura T. "Ether-linked analogue of 2-arachidonoylglycerol (noladin ether) was not detected in the brains of various mammalian species." Journal of Neurochemistry. 2003 Jun;85(6):1374-81. PMID 12787057
- ↑ Bisogno, T., D. Melck, M. Bobrov, N. M. Gretskaya, V. V. Bezuglov, L. De Petrocellis, V. Di Marzo. "N-acyl-dopamines: novel synthetic CB1 cannabinoid-receptor ligands and inhibitors of anandamide inactivation with cannabimimetic activity in vitro and in vivo." The Biochemical Journal. 2000 Nov 1;351 Pt 3:817-24. PMID 11042139
- ↑ Bisogno T, Ligresti A, Di Marzo V. "The endocannabinoid signalling system: biochemical aspects." Pharmacology, Biochemistry, and Behavior. 2005 Jun;81(2):224-38. PMID 15935454
- ↑ Ralevic V. (julio de 2003). «Cannabinoid modulation of peripheral autonomic and sensory neurotransmission.». European journal of pharmacology 472 (1-2): 1-21. PMID 12860468. doi:10.1016/S0014-2999(03)01813-2.
- ↑ Porter AC, Sauer JM, Knierman MD, Becker GW, Berna MJ, Bao J, Nomikos GG, Carter P, Bymaster FP, Leese AB, Felder CC. (junio de 2002). «Characterization of a Novel Endocannabinoid, Virodhamine, with Antagonist Activity at the CB1 Receptor». The Journal of pharmacology and experimental therapeutics 301 (3): 1020-1024. PMID 12023533. doi:10.1124/jpet.301.3.1020.
- ↑ Fride E, Bregman T, Kirkham TC. (abril de 2005). «Endocannabinoids and food intake: newborn suckling and appetite regulation in adulthood.». Experimental Biology and Medicine 230 (4): 225-234. PMID 15792943. doi:10.1371/journal.pbio.0020286.
- ↑ Nicoll RA, Alger BE (2004). «The brain's own marijuana». Sci. Am. 291 (6): 68-75. PMID 15597982.
- ↑ https://web.archive.org/web/20070928104526/http://www.marijuana.org/mydna10-12-05.htm
- Murillo Rodríguez E. (2008). «Papel modulador de los endocanabinoides en el sueño». Revista de Neurología 46 (3): 160-166. PMID 18297624.
www.cultivamedicina.com
Notas
- Artículo traducido de la Wikipedia en inglés: http://en.wikipedia.org/wiki/Cannabinoid
- Elsohly MA, Slade D (2005). «Chemical constituents of marijuana: the complex mixture of natural cannabinoids». Life Sci. 78 (5): 539-48. PMID 16199061. doi:10.1016/j.lfs.2005.09.011.
- Hanuš L (1987). «Biogenesis of cannabinoid substances in the plant». Acta Universitatis Palackianae Olomucensis Facultatis Medicae 116: 47-53. PMID 2962461.
- Hanuš L., Krejčí Z. Isolation of two new cannabinoid acids from Cannabis sativa L. of Czechoslovak origin. Acta Univ. Olomuc., Fac. Med. 74, 161-166 (1975)
- Hanuš L., Krejčí Z., Hruban L. Isolation of cannabidiolic acid from Turkish variety of cannabis cultivated for fibre. Acta Univ. Olomuc., Fac. Med. 74, 167-172 (1975)
- Turner C. E., Mole M. L., Hanuš L., ElSohly H. N. Constituents of Cannabis sativa L. XIX. Isolation and structure elucidation of cannabiglendol. A novel cannabinoid from an Indian variant. J. Nat. Prod. - Lloydia 44 (1), 27-33 (1981)
- Devane WA, Hanuš L, Breuer A, et al. (1992). «Isolation and structure of a brain constituent that binds to the cannabinoid receptor». Science 258 (5090): 1946-9. PMID 1470919. doi:10.1126/science.1470919.
- Hanuš L, Gopher A, Almog S, Mechoulam R (1993). «Two new unsaturated fatty acid ethanolamides in brain that bind to the cannabinoid receptor». J. Med. Chem. 36 (20): 3032-4. PMID 8411021. doi:10.1021/jm00072a026.
- Mechoulam R, Ben-Shabat S, Hanuš L, et al. (1995). «Identification of an endogenous 2-monoglyceride, present in canine gut, that binds to cannabinoid receptors». Biochem. Pharmacol. 50 (1): 83-90. PMID 7605349. doi:10.1016/0006-2952(95)00109-D.
- Racz I, Nadal X, Alferink J, Baños JE, Rehnelt J, Martín M, Pintado B, Gutiérrez-Adán A, Sanguino E, Bellora N, Manzanares J, Zimmer A, Rafael Maldonado López (2008). «Interferon-γ is a critical modulator of CB2 cannabinoid receptor signaling during neuropathic pain». J. Neurosci. 28: 12136-12145.
- Racz I, Nadal X, Alferink J, Baños JE, Rehnelt J, Martín M, Pintado B, Gutiérrez-Adán A, Sanguino E, Manzanares J, Zimmer A, Rafael Maldonado López, (2008). «Crucial role of CB2 cannabinoid receptor in the regulation of central immune responses during neuropathic pain». J. Neurosci. 28: 12125-12135,.
Enlaces externos
 Wikimedia Commons alberga una categoría multimedia sobre Cannabinoide.
Wikimedia Commons alberga una categoría multimedia sobre Cannabinoide.