Diferencia entre revisiones de «Pirimidina»
| Línea 48: | Línea 48: | ||
Las pirimidinas se hallan asociadas en su mayoría a [[monosacáridos]] de cinco carbonos ([[pentosa]]s) unidos en N<sub>1</sub> para formar [[nucleósido]]s que, a su vez, se unen a un grupo fosfato (ácido fosfórico) para formar los [[nucleótido]]s. |
Las pirimidinas se hallan asociadas en su mayoría a [[monosacáridos]] de cinco carbonos ([[pentosa]]s) unidos en N<sub>1</sub> para formar [[nucleósido]]s que, a su vez, se unen a un grupo fosfato (ácido fosfórico) para formar los [[nucleótido]]s. |
||
En el [[Ácido desoxirribonucleico|ADN]] y el [[Ácido ribonucleico|ARN]], estas bases forman [[Fuerza por puente de hidrógeno|enlaces de hidrógeno]] con sus [[Purina|purinas]] complementarias. Así, en el ADN, las purinas [[adenina]] (A) y [[guanina]] (G) se emparejan con las pirimidinas [[timina]] (T) y [[citosina]] (C), respectivamente. |
En el [[Ácido desoxirribonucleico|ADN]] y el [[Ácido ribonucleico|ARN]], estas bases forman [[Fuerza por puente de hidrógeno|enlaces de hidrógeno]] con sus [[Purina|purinas]] [[Complementariedad (biología molecular)|complementarias]]. Así, en el ADN, las purinas [[adenina]] (A) y [[guanina]] (G) se emparejan con las pirimidinas [[timina]] (T) y [[citosina]] (C), respectivamente. |
||
En ARN, el complemento de adenina (A) es [[uracilo]] (U) en lugar de timina (T), por lo que los pares que se forman son adenina: uracilo y guanina: citosina. |
En ARN, el complemento de adenina (A) es [[uracilo]] (U) en lugar de timina (T), por lo que los pares que se forman son adenina: uracilo y guanina: citosina. |
||
Revisión del 23:17 19 may 2017
| Pirimidina | |
|---|---|
| IUPAC | Pirimidina |
| Fórmula química | C4H4N2 |
| Masa molecular | 80.09 g/mol |
| Densidad | 1.016 g/ml |
| Punto de fusión | 20 - 22 °C |
| Punto de ebullición | 123 - 124 °C |
| Número CAS | 289-95-2 |
| SMILES | C1=NC=NC=C1 |

| |
La pirimidina es un compuesto orgánico, similar al benceno, y a la piridina pero con dos átomos de nitrógeno que sustituyen al carbono en las posiciones 1 y 3 (ver tabla). Se degrada en sustancias muy solubles como alanina beta y aminoisobutirato beta, precursores de acetil-CoA y succinil-CoA.
Derivados
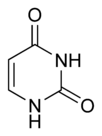
La pirimidina tiene tres derivados muy importantes para la vida, ya que forman parte de los ácidos nucleicos: la timina, la citosina y el uracilo; las tres tienen un grupo carbonilo (C=O) en el carbono 2; las dos primeras forman parte del ADN donde se aparean con sus purinas complementarias, mientras que la última está presente solo en el ARN.
| Timina | Citosina | Uracilo |

|

|
|
En las pirimidinas, una molécula de carbamoilfosfato en la que la glutamina es la donadora del grupo amino, se une a una molécula de ácido aspártico. El ácido orótico, producto de estas reacciones, es transferido a una molécula de fosfo-ribosil pirofosfato para dar origen al ácido uridílico.
Nucleósidos y nucleótidos

Las pirimidinas se hallan asociadas en su mayoría a monosacáridos de cinco carbonos (pentosas) unidos en N1 para formar nucleósidos que, a su vez, se unen a un grupo fosfato (ácido fosfórico) para formar los nucleótidos.
En el ADN y el ARN, estas bases forman enlaces de hidrógeno con sus purinas complementarias. Así, en el ADN, las purinas adenina (A) y guanina (G) se emparejan con las pirimidinas timina (T) y citosina (C), respectivamente.
En ARN, el complemento de adenina (A) es uracilo (U) en lugar de timina (T), por lo que los pares que se forman son adenina: uracilo y guanina: citosina.
Muy raramente, la timina puede aparecer en el ARN, o uracilo en el ADN, pero cuando las otras tres principales bases pirimidinas están representadas, algunas bases menores de pirimidina también pueden ocurrir en ácidos nucleicos. Estas pirimidinas menores son usualmente versiones metiladas de las principales y se postula que tienen funciones reguladoras. [1]
Estos modos de enlace de hidrógeno son para el emparejamiento clásico de la base de Watson-Crick. Otros modos de enlace de hidrógeno ("emparejamiento de oscilación") están disponibles tanto en ADN como en ARN, aunque el grupo 2'-hidroxilo adicional de ARN expande las configuraciones, a través de las cuales el ARN puede formar enlaces de hidrógeno
Referencias
- ↑ Nelson, David L.; Cox, Michael M. (2008). Principles of Biochemistry (5th edición). W. H. Freeman. pp. 272-274. ISBN 1429208929.
