Hipoclorito de sodio
| Hipoclorito de sodio | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Hipoclorito de sodio | ||
| General | ||
| Otros nombres | Hipoclorito sódico | |
| Fórmula estructural |
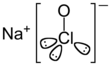 | |
| Fórmula molecular | NaClO | |
| Identificadores | ||
| Número CAS | 7681-52-9[1] | |
| ChEBI | 32146 | |
| ChEMBL | CHEMBL1334078 | |
| ChemSpider | 22756 | |
| PubChem | 24340 | |
| UNII | DY38VHM5OD | |
| KEGG | D01711 | |
| Propiedades físicas | ||
| Apariencia | Verde (líquido, diluido). Sólido (blanco) | |
| Densidad | 1110 kg/m³; 1,11 g/cm³ | |
| Masa molar | 74,44 g/mol | |
| Punto de fusión | 291 K (18 °C) | |
| Punto de ebullición | 374 K (101 °C) | |
| Propiedades químicas | ||
| Acidez | >7 (base) pKa | |
| Solubilidad en agua | 29.3 g/100mL (0 °C) | |
| Peligrosidad | ||
| Frases R |
Error en la cita: Etiqueta <ref> no válida; el nombre no puede ser un número entero. Usa un título descriptivo, Error en la cita: Etiqueta <ref> no válida; el nombre no puede ser un número entero. Usa un título descriptivo, Error en la cita: Etiqueta <ref> no válida; el nombre no puede ser un número entero. Usa un título descriptivo | |
| Frases S | S1/2, S28, S45, S50, S61 | |
| Riesgos | ||
| Riesgos principales | Hazardous Chemical Database (en inglés) | |
| Ingestión | Peligroso en grandes concentraciones. | |
| Inhalación | Peligroso en grandes concentraciones. | |
| Piel | Causa quemaduras químicas y cáncer de piel en grandes cantidades. | |
| Ojos | Causa quemaduras químicas. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El hipoclorito de sodio (cuya disolución en agua es conocida como lejía) es un compuesto químico, fuertemente oxidante de fórmula NaClO.
Contiene cloro en estado de oxidación +1, es un oxidante fuerte y económico. Debido a esta característica se utiliza como desinfectante, además destruye muchos colorantes por lo que se utiliza como blanqueador.[cita requerida]
En disolución acuosa sólo es estable en pH básico. Al acidular en presencia de cloruro libera cloro elemental, que en condiciones normales se combina para formar el gas dicloro, tóxico. Por esto debe almacenarse alejado de cualquier ácido. Tampoco debe mezclarse con amoníaco, ya que puede formar cloramina, un gas muy tóxico.[cita requerida]
Historia
Su uso industrial va unido a su uso como blanqueador. Derry (1977:783) afirma que el uso del cloro como blanqueante fue utilizado primero por Claude Louis Berthollet (1785), cuya agua de Javel se obtenía haciendo pasar cloro a través de potasa (sin embargo, Carl Wilhelm Scheele, descubridor del cloro, ya había notado estas propiedades). Posteriormente, Charles Tennant (1799) utilizaría el cloro que se obtenía como subproducto en la fabricación de sosa; el producto de Tennant era un hipoclorito de calcio en polvo.
Desde finales del siglo XVIII, además, se fueron encontrando usos al hipoclorito como desinfectante; los pioneros fueron el médico francés Pierre-François Percy (1793; la reducción de mortalidad sería de alrededor del 50%[2]) y el farmacéutico Antoine Germain Labarraque (1825), a quien se atribuye la sustitución del potasio por sodio.
En México, Francisco Montes de Oca, hacia 11 de julio de 1860 inició la escuela entre los cirujanos militares de: lavar los campos quirúrgicos y camas de los heridos de guerra, lavar las manos antes, durante la cirugía y al concluir las amputaciones, lavar las heridas con el licor de Labarraque (con un sistema que usaría Alexis Carrel en la Primera Guerra Mundial), por lo que fue el iniciador empírico de la antisepsia, esto demostrado por las múltiples tesis de la Facultad de Medicina de la UNAM y los trabajos de Quijano[3] y Soriano[4]), quienes reafirman esta primacía y extenso uso del referido licor desde 1860 hasta 1900.
Forma
El hipoclorito de sodio existe sólido en forma de sal pentahidratada NaClO * 5 H2O y con 2,5 moléculas de agua de hidratación por molécula: NaOCl * 2,5 H2O. La primera forma es la más conocida. A 0 °C se disuelven 29,3 g de la sal en 100 g de agua y a 23 °C ya son 94,2 g/100.
Reacciones
El hipoclorito se dismuta a temperaturas elevadas para dar clorato y cloruro:
- 3 NaClO → 2 NaCl + NaClO3
A veces se aprovecha esta reacción para la síntesis del clorato. Con aminas se forman las cloraminas. Estos compuestos suelen ser tóxicos y pueden ser explosivos. No es inflamable, pero con el fuego reacciona.
Usos
La lejía (popularmente conocido como cloro, agua lavandina, agua Jane, entre otros), un disolución acuosa de hipoclorito de sodio, es usado frecuentemente en hogares, como oxidante en el proceso de potabilización del agua, a dosis ligeramente superiores al punto crítico (punto en que empieza a aparecer cloro residual libre).[cita requerida]
En cuanto al tratamiento del agua, las preocupaciones con seguridad de transporte y manipulación tienen influencia directa cuanto el uso de hipoclorito de sodio en lugar de gas cloro, lo que representa un mercado de importante expansión potencial.[5] El hipoclorito de sodio se utiliza también como desinfectante en piscinas, ya sea por aplicación directa en forma de líquido (125 mL diarios por cada 10 m3 de agua), pastillas concentradas o en polvo, o a través de un aparato de electrólisis salina por el que se hace circular el agua de la piscina. Para que la electrólisis tenga lugar se debe salar ligeramente la piscina (necesitaremos 4 g de sal por litro de agua). El aparato de electrólisis, mediante descargas eléctricas trasforma la sal (NaCl) en hipoclorito de sodio consiguiendo desinfectar el agua.[cita requerida]
También se usa en el proceso de identificación de especies de los distintos filos de animales que poseen espículas o escleritos, como poríferos o equinodermos (holoturoideos). El hipoclorito de sodio disuelve la materia orgánica dejando al descubierto estas estructuras (únicas en cada especie), que son de carbonato de calcio (calcáreas) o dióxido de silicio (silíceas) y, por tanto, no se disuelven.
Este producto químico se puede también utilizar como blanqueador para las fibras textiles, así como para desinfectar los lavabos gracias a su poder fungicida y bactericida.
En parasitología puede ser utilizado para la esporulación invitro de Ooquistes de protozoos del phylum apicomplexa en el método denominado de Cawthorn.
Fórmula de dilución
Ejemplo:
Cantidad de líquido deseado: 15 L Concentración del producto comercial: 10%
En la práctica totalidad de los casos de desinfección de superficies se manejan cantidades de 5000 ppm (o lo que es lo mismo, 5000 mg/L, o 5 g/L).
Solución
Se necesitarían para obtener 15500 mg/L de disolución.
Referencias
- Derry, T. K.; y Trevor I. WILLIAMS (1977). Historia de la tecnología. 3. Desde 1750 hasta 1900 (II). Madrid/México: Siglo XXI. 84-323-0281-3.
- ↑ Número CAS
- ↑ Stéphanie LE QUELLEC: Histoire des urgences a Paris de 1770 a nos jours (tesis). Université Paris 7, 2000.
- ↑ Fernando QUIJANO-PIMAN: «El inicio de la antisepsia en México (1872)», en Gaceta Médica de México, 123 (11-12): pág. 289; 1987.
- ↑ M. F. Soriano: «Contibuciones a la cirugía militar en México», en Gaceta Médica de México, 21: pág. 158; 1886.
- ↑ «Sodium Hypochlorite Chemical Production». Intratec. ISBN 978-0-615-70217-9.
Enlaces externos
 Wikimedia Commons alberga una categoría multimedia sobre Hipoclorito de sodio.
Wikimedia Commons alberga una categoría multimedia sobre Hipoclorito de sodio.- ATSDR en Español - ToxFAQs: hipoclorito de calcio/hipoclorito de sodio
- Instituto Nacional de Seguridad e Higiene en el Trabajo de España: Ficha internacional de seguridad química del hipoclorito de sodio (disolución >5%).
- Cómo fabricar lejía casera con una pila y agua con sal

