Ацетат бария: различия между версиями
Перейти к навигации
Перейти к поиску
| [непроверенная версия] | [непроверенная версия] |
Содержимое удалено Содержимое добавлено
→Химические свойства: При разложении сильными кислотами не был указан коеффицент для уксусной кислоты |
Автодевикификация Шаблон:Ацетаты. |
||
| (не показана 1 промежуточная версия 1 участника) | |||
| Строка 127: | Строка 127: | ||
{{organic-compound-stub}} |
{{organic-compound-stub}} |
||
[[Категория:Ацетаты (соли)|бария]] |
[[Категория:Ацетаты (соли)|бария]] |
||
[[Категория:Соединения бария по алфавиту]] |
[[Категория:Соединения бария по алфавиту]] |
||
Текущая версия от 12:56, 5 октября 2021
| Ацетат бария | |
|---|---|
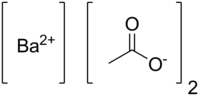 | |
| Общие | |
| Систематическое наименование |
Ацетат бария |
| Традиционные названия | барий уксуснокислый |
| Хим. формула | C4H6BaO4 |
| Рац. формула | Ba(CH3COO)2 |
| Физические свойства | |
| Молярная масса | 255,43 г/моль |
| Плотность | 2,468 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | с разл. ~450 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 58,70; 75100 г/100 мл |
| Классификация | |
| Рег. номер CAS | 543-80-6 |
| PubChem | 10980 и 521500 |
| Рег. номер EINECS | 208-849-0 |
| SMILES | |
| InChI | |
| RTECS | AF4550000 |
| ChEBI | 190441 |
| ChemSpider | 10515 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацета́т ба́рия (уксуснокислый барий) — органическое соединение, соль щелочноземельного металла бария и уксусной кислоты. Бесцветные кристаллы, образует кристаллогидраты.
Получение
[править | править код]- Получают действием уксусной кислоты на оксид бария, гидроксид бария или карбонат бария:
Физические свойства
[править | править код]Ацетат бария образует бесцветные кристаллы тетрагональной сингонии, пространственная группа I 41/a, параметры ячейки a = 0,9901 нм, c = 2,7362 нм, Z = 16.
При кристаллизации из водных растворов образует кристаллогидраты:
- при температуре ниже 25 °C — тригидрат Ba(CH3COO)2•3H2O
- при температуре 25÷41 °C — моногидрат Ba(CH3COO)2•H2O
- при температуре выше 41 °C — безводный Ba(CH3COO)2
Химические свойства
[править | править код]- При нагревании разлагается на карбонат бария и ацетон:
- Разлагается сильными кислотами:
Применение
[править | править код]- Как протраву при крашении шерсти и ситца.
См. также
[править | править код]Литература
[править | править код]- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |




