О-Ксилол: различия между версиями
| [отпатрулированная версия] | [непроверенная версия] |
Нет описания правки |
Спасено источников — 1, отмечено мёртвыми — 0. Сообщить об ошибке. См. FAQ.) #IABot (v2.0.8.6 |
||
| (не показано 25 промежуточных версий 20 участников) | |||
| Строка 1: | Строка 1: | ||
{{DISPLAYTITLE:''о''-Ксилол}} |
|||
| ⚫ | |||
{{Вещество |
|||
| картинка = O-Xylene.png |
|||
| картинка2 = O-xylene-spaceFill.png |
|||
| хим. формула = C<sub>8</sub>H<sub>10</sub> |
|||
| молярная масса = 106.17 |
|||
| темп. плавления = -24 |
|||
| темп. кипения = 144 |
|||
| темп. вспышки = 32 |
|||
| CAS = 95-47-6 |
|||
| SMILES = CC1=C(C)C=CC=C1 |
|||
| СГС = {{СГС|Пламя|Восклицательный знак|Опасность для здоровья}} |
|||
}} |
|||
| ⚫ | '''Ортоксилол''' (''о''-ксилол, [[Номенклатура ИЮПАК|ИЮПАК]]: '''1,2-диметилбензол''', {{lang-en|o-xylene}}) — органическое вещество, ароматический углеводород. Это бесцветная жидкость с характерным запахом, смешивается с [[Этанол|этанолом]], [[Диэтиловый эфир|диэтиловым эфиром]], [[Ацетон|ацетоном]], [[Хлороформ|хлороформом]], [[Бензол|бензолом]]; растворимость в воде менее 0,015 %. |
||
== Получение == |
== Получение == |
||
| ⚫ | Для синтеза [[Диметилбензолы|ксилолов]] используются процессы каталитического [[риформинг]]а [[бензин]]а, а также [[Пиролиз|пиролиза]] бензина, подвергнутого [[Гидроочистка|гидроочистке]]. Для выделения ''о''-ксилола из образующейся смеси [[Изомерия|изомеров]] используют чёткую [[Ректификация|ректификацию]]. |
||
| ⚫ | |||
== Применение == |
== Применение == |
||
| ⚫ | Окислением ''о''-ксилола в паровой фазе при 450—600 °C ([[катализатор]] — V<sub>2</sub>O<sub>5</sub> на SiO<sub>2</sub>) получают [[фталевый ангидрид]]. Глубоким окислением ''о''-ксилола действием [[Азотная кислота|азотной кислоты]] или кислорода воздуха в жидкой фазе при 100—300 °C и 4 МПа (катализаторы — [[бромиды]] Мn или Со) получают [[Фталевая кислота|фталевую кислоту]]. |
||
| ⚫ | |||
| ⚫ | Окислением о-ксилола в паровой фазе при 450—600° |
||
Также ''о''-ксилол входит в состав некоторых жидкостей для снятия [[Иммерсия (микроскопия)|иммерсионного масла]] с объективов микроскопов. |
|||
| ⚫ | |||
== Примечания == |
|||
{{примечания}} |
|||
== Ссылки == |
== Ссылки == |
||
* [http://files.school-collection.edu.ru/dlrstore/a75b771f-579d-d1f5-1d32-f78eb57e6a85/00119627187239641.htm Химическая структура] |
* [http://files.school-collection.edu.ru/dlrstore/a75b771f-579d-d1f5-1d32-f78eb57e6a85/00119627187239641.htm Химическая структура] {{Wayback|url=http://files.school-collection.edu.ru/dlrstore/a75b771f-579d-d1f5-1d32-f78eb57e6a85/00119627187239641.htm |date=20090726072646 }} |
||
{{rq|img|infobox|iwiki}} |
|||
[[Категория: |
[[Категория:Алкилбензолы]] |
||
[[Категория:растворители]] |
[[Категория:растворители]] |
||
[[Категория:Продукция основного органического синтеза]] |
|||
Текущая версия от 12:19, 14 марта 2022
| О-Ксилол | |
|---|---|
  | |
| Общие | |
| Хим. формула | C8H10 |
| Физические свойства | |
| Молярная масса | 106.17 г/моль |
| Плотность | 0,88 ± 0,01 г/см³[1] |
| Энергия ионизации | 8,56 ± 0,01 эВ[1][2] |
| Термические свойства | |
| Температура | |
| • плавления | -24 °C |
| • кипения | 144 °C |
| • вспышки | 32 °C |
| Пределы взрываемости | 0,9 ± 0,1 об.%[1] |
| Давление пара | 7 ± 1 мм рт.ст.[1] |
| Структура | |
| Дипольный момент | 2,1E−30 Кл·м[2] |
| Классификация | |
| Рег. номер CAS | 95-47-6 |
| PubChem | 7237 |
| Рег. номер EINECS | 202-422-2 |
| SMILES | |
| InChI | |
| RTECS | ZE2450000 |
| ChEBI | 28063 |
| ChemSpider | 6967 |
| Безопасность | |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
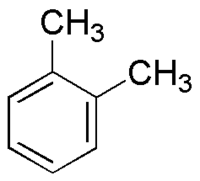
Ортоксилол (о-ксилол, ИЮПАК: 1,2-диметилбензол, англ. o-xylene) — органическое вещество, ароматический углеводород. Это бесцветная жидкость с характерным запахом, смешивается с этанолом, диэтиловым эфиром, ацетоном, хлороформом, бензолом; растворимость в воде менее 0,015 %.
Получение
[править | править код]Для синтеза ксилолов используются процессы каталитического риформинга бензина, а также пиролиза бензина, подвергнутого гидроочистке. Для выделения о-ксилола из образующейся смеси изомеров используют чёткую ректификацию.
Применение
[править | править код]Окислением о-ксилола в паровой фазе при 450—600 °C (катализатор — V2O5 на SiO2) получают фталевый ангидрид. Глубоким окислением о-ксилола действием азотной кислоты или кислорода воздуха в жидкой фазе при 100—300 °C и 4 МПа (катализаторы — бромиды Мn или Со) получают фталевую кислоту.
Кроме того, о-ксилол — растворитель лаков, красок, мастик, высокооктановая добавка к моторным топливам.
Также о-ксилол входит в состав некоторых жидкостей для снятия иммерсионного масла с объективов микроскопов.
Примечания
[править | править код]- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0668.html
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
Ссылки
[править | править код]- Химическая структура Архивная копия от 26 июля 2009 на Wayback Machine
