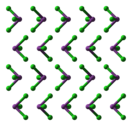Хлорид висмута(III): различия между версиями
| [отпатрулированная версия] | [непроверенная версия] |
м r2.7.1) (робот добавил: fa:بیسموت کلرید |
MBHbot (обсуждение | вклад) м →top: РДБ-запрос, replaced: еакционоспособност → еакционноспособност |
||
| (не показано 18 промежуточных версий 16 участников) | |||
| Строка 1: | Строка 1: | ||
<!-- http://en.wikipedia.org/wiki/File:Bismuth-trichloride-xtal-1982-Bi-coordination-A-3D-balls.png --> |
|||
{{Вещество |
{{Вещество |
||
| заголовок = Хлорид висмута(III) |
| заголовок = Хлорид висмута(III) |
||
| Строка 10: | Строка 9: | ||
| сокращения = |
| сокращения = |
||
| хим. формула = BiCl<sub>3</sub> |
| хим. формула = BiCl<sub>3</sub> |
||
| |
| рац. формула = BiCl<sub>3</sub> |
||
| отн. молек. масса = |
|||
| молярная масса = 315,34 |
| молярная масса = 315,34 |
||
| Строка 67: | Строка 65: | ||
| authorlink = |
| authorlink = |
||
| datepublished = |
| datepublished = |
||
| url = |
| url = www.xumuk.ru/spravochnik/418.html |
||
| title = Серебра хлорид |
| title = Серебра хлорид |
||
| format = |
| format = |
||
| Строка 74: | Строка 72: | ||
| accessdate = 2010-03-01 |
| accessdate = 2010-03-01 |
||
| lang = |
| lang = |
||
| description = |
| description = |
||
}}</ref> |
}}</ref> |
||
| теплоёмкость = 109<ref name="xumuk" /> |
| теплоёмкость = 109<ref name="xumuk" /> |
||
| Строка 116: | Строка 114: | ||
| ЛД50 = (крысы, орально) 3324 |
| ЛД50 = (крысы, орально) 3324 |
||
| |
| NFPA 704 = {{NFPA 704 |
||
| опасность для здоровья = 3 |
| опасность для здоровья = 3 |
||
| огнеопасность = 0 |
| огнеопасность = 0 |
||
| реакционноспособность = 2 |
|||
| реакционоспособность = 2 |
|||
| прочее = |
| прочее = |
||
}} |
}} |
||
| токсичность = |
|||
}} |
}} |
||
'''Хлори́д ви́смута(III)''' (''трихлорид висмута, хлористый висмут'') — BiCl<sub>3</sub>, [[ |
'''Хлори́д ви́смута(III)''' (''трихлорид висмута, хлористый висмут'') — BiCl<sub>3</sub>, [[бинарные соединения|бинарное]] неорганическое соединение металла [[висмут]]а с [[хлор]]ом, висмутовая [[соль]] [[хлороводород|хлороводородной кислоты]]. В [[нормальные условия|нормальных условиях]] представляет собой белое (бесцветное) или бледно-жёлтое кристаллическое, очень [[гигроскопичность|гигроскопичное]] вещество. |
||
== Молекулярная и кристаллическая структура == |
== Молекулярная и кристаллическая структура == |
||
[[Файл:Kristallstruktur Yttrium(III)-fluorid.png|200px|left|thumb|Кристаллическая структура хлорида висмута(III)]] |
[[Файл:Kristallstruktur Yttrium(III)-fluorid.png|200px|left|thumb|Кристаллическая структура хлорида висмута(III)]] |
||
Хлорид висмута имеет следующий элементный состав: Bi (66,27 |
Хлорид висмута имеет следующий элементный состав: Bi (66,27 %), Cl (33,73 %). [[Энергия разрыва химической связи|Энергия разрыва связи]] в соединении (''Е''<sub>св.</sub>): 275 кДж/моль, длина связи Bi—Cl: 0,248 нм, валентный угол Cl—Bi—Cl составляет 100°<ref>{{книга |
||
|автор = Лидин Р.А., Андреева Л.Л., Молочко В.А. |
|автор = Лидин Р.А., Андреева Л.Л., Молочко В.А. |
||
|часть = Часть III. Глава 5. Энергия и длина связи для двухатомных частиц |
|часть = Часть III. Глава 5. Энергия и длина связи для двухатомных частиц |
||
| Строка 162: | Строка 161: | ||
|isbn = 5-7107-8085-5 |
|isbn = 5-7107-8085-5 |
||
|тираж = |
|тираж = |
||
}}</ref>. Молекула соединения представляет собой тригональную пирамиду, у которой вершина — атом висмута — имеет неподелённую |
}}</ref>. Молекула соединения представляет собой тригональную пирамиду, у которой вершина — атом висмута — имеет неподелённую [[электронная пара|электронную пару]]. |
||
Кристаллическая структура BiCl<sub>3</sub> [[кубическая сингония|кубическая]]. |
Кристаллическая структура BiCl<sub>3</sub> [[кубическая сингония|кубическая]]. |
||
| Строка 193: | Строка 192: | ||
* [[Энергия Гиббса|стандартная энергия Гиббса]], ΔG<sup>o</sup><sub>298</sub>: −313 кДж/моль<ref name="const2" />. |
* [[Энергия Гиббса|стандартная энергия Гиббса]], ΔG<sup>o</sup><sub>298</sub>: −313 кДж/моль<ref name="const2" />. |
||
* стандартная мольная [[теплоемкость]], C<sub>p</sub><sup>o</sup><sub>298</sub>: 109 Дж/(моль·K)<ref name="xumuk" />; |
* стандартная мольная [[теплоемкость]], C<sub>p</sub><sup>o</sup><sub>298</sub>: 109 Дж/(моль·K)<ref name="xumuk" />; |
||
* энтальпия плавления, ΔH<sub>пл:</sub> 23,47 кДж/моль |
* энтальпия плавления, ΔH<sub>пл:</sub> 23,47 кДж/моль<ref name="const3">{{книга |
||
|автор = Лидин Р.А., Андреева Л.Л., Молочко В.А. |
|автор = Лидин Р.А., Андреева Л.Л., Молочко В.А. |
||
|часть = Часть IV. Глава 2. Энтальпия и энтропия фазовых переходов |
|часть = Часть IV. Глава 2. Энтальпия и энтропия фазовых переходов |
||
| Строка 211: | Строка 210: | ||
|тираж = |
|тираж = |
||
}}</ref>; |
}}</ref>; |
||
* энтальпия кипения, ΔH<sub>кип</sub>: 72,59 кДж/моль |
* энтальпия кипения, ΔH<sub>кип</sub>: 72,59 кДж/моль<ref name="const3" />. |
||
== Получение == |
== Получение == |
||
| Строка 220: | Строка 219: | ||
* Взаимодействие [[оксид висмута(III)|оксида висмута(III)]] с концентрированной [[соляная кислота|соляной кислотой]] при нагревании: |
* Взаимодействие [[оксид висмута(III)|оксида висмута(III)]] с концентрированной [[соляная кислота|соляной кислотой]] при нагревании: |
||
: Bi<sub>2</sub>O<sub>3</sub> + 6HCl = 2BiCl<sub>3</sub> + 3H<sub>2</sub>O. |
: Bi<sub>2</sub>O<sub>3</sub> + 6HCl = 2BiCl<sub>3</sub> + 3H<sub>2</sub>O. |
||
== Химические свойства == |
== Химические свойства == |
||
* Гидролизуется водой: |
* Гидролизуется водой: |
||
: BiCl<sub>3</sub> + H<sub>2</sub>O → |
: BiCl<sub>3</sub> + H<sub>2</sub>O → BiOCl + 2HCl. |
||
* В солянокислом растворе устойчив, склонен образовывать комплексы — хлорвисмутаты (III): |
* В солянокислом растворе устойчив, склонен образовывать комплексы — хлорвисмутаты (III): |
||
| Строка 235: | Строка 234: | ||
<center> |
<center> |
||
{|align="center" class="wikitable" |
{|align="center" class="wikitable" |
||
| |
|[[Файл:Tricaesium-hexachlorobismuthate-xtal-1986-3D-balls.png|center|200px]]||[[Файл:Tricaesium-hexachlorobismuthate-xtal-1986-3D-SF.png|center|200px]]||[[Файл:Hexachlorobismuthate-from-tricaesium-xtal-1986-3D-balls.png|center|130px]] |
||
|- |
|- |
||
|<center>Cs<sub>3</sub>[BiCl<sub>6</sub>]</center>||<center>Cs<sub>3</sub>[BiCl<sub>6</sub>]</center>||<center>[BiCl<sub>6</sub>]<sup>3−</sup></center> |
|<center>Cs<sub>3</sub>[BiCl<sub>6</sub>]</center>||<center>Cs<sub>3</sub>[BiCl<sub>6</sub>]</center>||<center>[BiCl<sub>6</sub>]<sup>3−</sup></center> |
||
| Строка 257: | Строка 256: | ||
* [[Хлорид висмута(II)]] |
* [[Хлорид висмута(II)]] |
||
== Безопасность == |
|||
== Примечания == |
== Примечания == |
||
{{Примечания}} |
{{Примечания}} |
||
{{Соединения висмута}} |
|||
== Литература == |
|||
== Ссылки == |
|||
[[Категория:Хлориды|Висмут]] |
[[Категория:Хлориды|Висмут]] |
||
[[Категория:Соединения висмута]] |
[[Категория:Соединения висмута]] |
||
[[Категория:Галогениды металлов]] |
[[Категория:Галогениды металлов]] |
||
{{спам-ссылки|1= |
|||
[[ar:كلوريد البزموت]] |
|||
* www.xumuk.ru/spravochnik/418.html |
|||
[[cs:Chlorid bismutitý]] |
|||
}} |
|||
[[de:Bismut(III)-chlorid]] |
|||
[[en:Bismuth chloride]] |
|||
[[fa:بیسموت کلرید]] |
|||
[[nl:Bismut(III)chloride]] |
|||
[[pl:Chlorek bizmutu(III)]] |
|||
[[simple:Bismuth(III) chloride]] |
|||
Текущая версия от 07:06, 5 мая 2023
| Хлорид висмута(III) | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Хлорид висмута(III) | ||
| Традиционные названия | Хлорид висмута, трихлорид висмута | ||
| Хим. формула | BiCl3 | ||
| Рац. формула | BiCl3 | ||
| Физические свойства | |||
| Состояние | твёрдое | ||
| Молярная масса | 315,34 г/моль | ||
| Плотность | 4,75[1] | ||
| Энергия ионизации | 10,4 эВ[5] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 234[2] | ||
| • кипения | 440[2] °C | ||
| Критическая точка | 905 °С, 11,97 МПа[3] | ||
| Мол. теплоёмк. | 109[3] Дж/(моль·К) | ||
| Энтальпия | |||
| • образования | −378[4] кДж/моль | ||
| Давление пара | (при 343 °С) 1,33⋅104[3] | ||
| Классификация | |||
| Рег. номер CAS | 7787-60-2 | ||
| PubChem | 24591 и 9839877 | ||
| Рег. номер EINECS | 232-123-2 | ||
| SMILES | |||
| InChI | |||
| RTECS | EB2690000 | ||
| ChemSpider | 22993 | ||
| Безопасность | |||
| ЛД50 | (крысы, орально) 3324 мг/кг | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Хлори́д ви́смута(III) (трихлорид висмута, хлористый висмут) — BiCl3, бинарное неорганическое соединение металла висмута с хлором, висмутовая соль хлороводородной кислоты. В нормальных условиях представляет собой белое (бесцветное) или бледно-жёлтое кристаллическое, очень гигроскопичное вещество.
Молекулярная и кристаллическая структура
[править | править код]
Хлорид висмута имеет следующий элементный состав: Bi (66,27 %), Cl (33,73 %). Энергия разрыва связи в соединении (Есв.): 275 кДж/моль, длина связи Bi—Cl: 0,248 нм, валентный угол Cl—Bi—Cl составляет 100°[6][7]. Молекула соединения представляет собой тригональную пирамиду, у которой вершина — атом висмута — имеет неподелённую электронную пару.
Кристаллическая структура BiCl3 кубическая.
Физические свойства
[править | править код]Хлорид висмута — белое или бледно-жёлтое, в кристаллическом виде — бесцветное вещество, плавящееся (T пл.= 234 °С) и кипящее без разложения (T кип.= 440 °С). Гигроскопичен, образует кристаллогидрат: BiCl3 • H2O[1].
Водой гидролизуется; растворим в метаноле, этаноле, ацетоне[1][3].
Термодинамические константы:
- стандартная энтальпия образования, ΔHo298: −378 кДж/моль[4];
- стандартная энтропия, So298: 172 Дж/(моль·K)[4];
- стандартная энергия Гиббса, ΔGo298: −313 кДж/моль[4].
- стандартная мольная теплоемкость, Cpo298: 109 Дж/(моль·K)[3];
- энтальпия плавления, ΔHпл: 23,47 кДж/моль[8];
- энтальпия кипения, ΔHкип: 72,59 кДж/моль[8].
Получение
[править | править код]- Прямая реакция элементов при 200 °С:
- 2Bi + 3Cl2 = 2BiCl3.
- Взаимодействие оксида висмута(III) с концентрированной соляной кислотой при нагревании:
- Bi2O3 + 6HCl = 2BiCl3 + 3H2O.
Химические свойства
[править | править код]- Гидролизуется водой:
- BiCl3 + H2O → BiOCl + 2HCl.
- В солянокислом растворе устойчив, склонен образовывать комплексы — хлорвисмутаты (III):
- BiCl3 + Cl− = [BiCl4]−.
- [BiCl4]− + Cl− = [BiCl5]2−.
- [BiCl5]2− + Cl− = [BiCl6]3−.
 |
 |
 |
- Реагирует с водными растворами щелочей с образованием гидроксида:
- BiCl3 + 3NaOH = Bi(OH)3↓ + 3NaCl.
- При сильном нагревании до 1000°С разлагается до хлорида висмута(I):
- BiCl3 → BiCl + Cl2
Применение
[править | править код]Висмут хлористый используется для получения других солей висмута, в качестве катализатора в органическом синтезе и как компонент пигментов и косметических средств[1].
См. также
[править | править код]
Примечания
[править | править код]- ↑ 1 2 3 4 Patnaik P. Handbook of Inorganic Chemicals. — McGraw-Hill, 2003. — P. 109—110. — ISBN 0-07-049439-8.
- ↑ 1 2 Лидин Р.А., Андреева Л.Л., Молочко В.А. Глава 3. Физические свойства // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 85. — ISBN 5-7107-8085-5.
- ↑ 1 2 3 4 5 [www.xumuk.ru/spravochnik/418.html Серебра хлорид]. Справочник по веществам. XuMuK.ru. Дата обращения: 1 марта 2010.
- ↑ 1 2 3 4 Лидин Р.А., Андреева Л.Л., Молочко В.А. Часть IV. Глава 1. Энтальпия образования, энтропия и энергия Гиббса образования веществ // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 452. — ISBN 5-7107-8085-5.
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Лидин Р.А., Андреева Л.Л., Молочко В.А. Часть III. Глава 5. Энергия и длина связи для двухатомных частиц // Константы неорганических веществ: справочник / Под редакцией проф. Р. А. Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 387. — ISBN 5-7107-8085-5.
- ↑ Лидин Р. А., Андреева Л. Л., Молочко В. А. Часть III. Глава 7.1. Геометрическая форма, длина связей и валентные углы в частицах с одним центральным атомом sp-элемента // Константы неорганических веществ: справочник / Под редакцией проф. Р. А. Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 396. — ISBN 5-7107-8085-5.
- ↑ 1 2 Лидин Р.А., Андреева Л.Л., Молочко В.А. Часть IV. Глава 2. Энтальпия и энтропия фазовых переходов // Константы неорганических веществ: справочник / Под редакцией проф. Р.А.Лидина. — 2-е изд., перераб. и доп.. — М.: «Дрофа», 2006. — С. 532. — ISBN 5-7107-8085-5.
Некоторые внешние ссылки в этой статье ведут на сайты, занесённые в спам-лист |