Гидроксид цинка: различия между версиями
Перейти к навигации
Перейти к поиску
| [отпатрулированная версия] | [непроверенная версия] |
Содержимое удалено Содержимое добавлено
м r2.7.1) (робот добавил: nl:Zinkhydroxide |
Нет описания правки Метки: ручная отмена через визуальный редактор |
||
| (не показано 47 промежуточных версий 38 участников) | |||
| Строка 1: | Строка 1: | ||
| ⚫ | |||
{{Вещество |
{{Вещество |
||
| картинка |
| картинка = |
||
| картинка3D = |
| картинка3D = Zn(OH)2 unit cell.png |
||
| изображение = Hydroxid zinečnatý.PNG |
|||
| картинка малая = |
|||
| наименование = Гидроксид цинка |
| наименование = Гидроксид цинка |
||
| сокращения = |
| сокращения = |
||
| традиционные названия = |
| традиционные названия = |
||
| хим. формула |
| хим. формула = Zn(OH)<sub>2</sub> |
||
| |
| рац. формула = Zn(OH)<sub>2</sub> |
||
| молярная масса = 99,38474 |
| молярная масса = 99,38474 |
||
| темп. плавления = 125 |
| темп. плавления = 125 |
||
| темп. кипения = |
| темп. кипения = |
||
| давление пара = <!-- при ?°C--> |
| давление пара = <!-- при ?°C--> |
||
| темп. разложения = |
| темп. разложения = |
||
| темп. вспышки = |
| темп. вспышки = |
||
| тройная точка = |
| тройная точка = |
||
| критическая точка = |
| критическая точка = |
||
| плотность = 3,053 |
| плотность = 3,053 |
||
| состояние = твёрдое |
| состояние = твёрдое |
||
| динамическая вязкость = |
| динамическая вязкость = |
||
| кинематическая вязкость = |
| кинематическая вязкость = |
||
| теплоёмкость = |
| теплоёмкость = |
||
| энтальпия образования = |
| энтальпия образования = |
||
| удельная теплота парообразования = |
| удельная теплота парообразования = |
||
| удельная теплота плавления = |
| удельная теплота плавления = |
||
| конст. диссоц. кислоты = |
| конст. диссоц. кислоты = |
||
| растворимость = <!--г/100 мл воды--> |
| растворимость = <!--г/100 мл воды--> |
||
| вещество1 = <!--(в) спирте--> |
| вещество1 = <!--(в) спирте--> |
||
| растворимость1 = |
| растворимость1 = |
||
| вращение = |
| вращение = |
||
| изоэлектрическая точка = |
| изоэлектрическая точка = |
||
| гибридизация = |
| гибридизация = |
||
| координационная геометрия = |
| координационная геометрия = |
||
| кристаллическая структура = |
| кристаллическая структура = |
||
| дипольный момент = |
| дипольный момент = |
||
| CAS = 20427-58-1 |
| CAS = 20427-58-1 |
||
| EINECS = |
| EINECS = |
||
| SMILES = |
| SMILES = |
||
| RTECS = |
|||
| Номер UN = |
|||
| ЕС = |
|||
| RTECS = |
|||
| ЛД50 = |
|||
| ЕС = |
|||
| ⚫ | |||
| ЛД50 = |
|||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
}} |
}} |
||
| ⚫ | |||
== Описание == |
== Описание == |
||
| ⚫ | Гидроксид цинка при [[стандартные условия|стандартных условиях]] представляет собой бесцветные [[кристаллы]], является [[аморфные тела|аморфным веществом]]. В настоящее время известно 5 [[Полиморфизм кристаллов|полиморфных модификаций]], из которых устойчивой является только модификация с ромбической [[сингония|сингонией]]. Гидроксид цинка практически [[растворимость|нерастворим]] в [[вода|воде]], проявляет [[амфотерность|амфотерные свойства]] (с преобладанием основных).<ref>{{Cite web|lang=ru-RU|url=https://xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai/gidroksid-tsinka-harakteristika-svoystva-i-poluchenie-himicheskie-reaktsii/|title=Гидроксид цинка, характеристика, свойства и получение, химические реакции|website=Вторая индустриализация России|date=2019-10-29|access-date=2022-09-27|archive-date=2022-09-27|archive-url=https://web.archive.org/web/20220927143511/https://xn--80aaafltebbc3auk2aepkhr3ewjpa.xn--p1ai/gidroksid-tsinka-harakteristika-svoystva-i-poluchenie-himicheskie-reaktsii/|deadlink=no}}</ref> |
||
| ⚫ | Гидроксид цинка при [[стандартные условия|стандартных условиях]] представляет собой бесцветные [[кристаллы]], является [[аморфные тела|аморфным веществом]]. В настоящее время известно 5 полиморфных модификаций, из которых устойчивой является только модификация с ромбической [[сингония|сингонией]]. Гидроксид цинка практически [[растворимость|нерастворим]] в [[вода|воде]], проявляет [[амфотерность|амфотерные свойства]] (с преобладанием основных). |
||
== Получение == |
== Получение == |
||
* Взаимодействие [[растворимость|растворимых]] [[соли|солей]] [[цинк]]а с [[щёлочи|щелочами]]: |
* Взаимодействие [[растворимость|растворимых]] [[соли|солей]] [[цинк]]а с [[щёлочи|щелочами]]: |
||
<math>\ |
<math>\mathsf{ZnCl_2 + 2 NaOH \text{(разб.)} \longrightarrow Zn(OH)_2 \downarrow + 2 NaCl}</math> |
||
<math>\ |
<math>\mathsf{Zn(NO_3)_2 + 2 KOH \longrightarrow Zn(OH)_2 \downarrow + 2 KNO_3}</math> |
||
== Химические свойства == |
== Химические свойства == |
||
* Взаимодействие с [[кислота]]ми с образованием [[соли]] и [[вода|воды]] ''([[нейтрализация|реакция нейтрализации]])'': |
* Взаимодействие с [[кислота]]ми с образованием [[соли]] и [[вода|воды]] ''([[нейтрализация|реакция нейтрализации]])'': |
||
<math>\ |
<math>\mathsf{Zn(OH)_2 + 2 HCl \longrightarrow ZnCl_2 + 2\ H_2O}</math> |
||
<math>\ |
<math>\mathsf{Zn(OH)_2 + H_2SO_4 \longrightarrow ZnSO_4 + 2\ H_2O}</math> |
||
* Взаимодействие с [[кислотные оксиды|кислотными оксидами]]: |
* Взаимодействие с [[кислотные оксиды|кислотными оксидами]]: |
||
<math>\ |
<math>\mathsf{Zn(OH)_2 + CO_2 \longrightarrow ZnCO_3 + H_2O}</math> |
||
* Взаимодействие с |
* Взаимодействие с избыткoм [[аммиак]]а: |
||
<math>\ |
<math>\mathsf{Zn(OH)_2 + 4 NH_3 \longrightarrow [Zn(NH_3)_4](OH)_2}</math>; |
||
* Взаимодействие со [[Щёлочи|щелочами]] с образованием |
* Взаимодействие со [[Щёлочи|щелочами]] с образованием: |
||
| ⚫ | |||
*# <math>\mathsf{Zn(OH)_2 + 2 NaOH \longrightarrow Na_2[Zn(OH)_4] }</math> — [[соли]] (тетрагидроксоцинката натрия) в [[раствор]]е |
|||
* Термическое разложение: |
|||
| ⚫ | |||
<math>\mathsf{Zn(OH)_2 \longrightarrow ZnO + H_2O}</math>; |
|||
== Применение == |
== Применение == |
||
Гидроксид цинка применяют для [[синтез]]а различных соединений [[цинк]]а, в основном, [[соли|солей]]. |
Гидроксид цинка применяют для [[синтез]]а различных соединений [[цинк]]а, в основном, [[соли|солей]]. |
||
| Строка 96: | Строка 94: | ||
{{Примечания}} |
{{Примечания}} |
||
| ⚫ | |||
{{Растворимость кислот, оснований и солей в воде}} |
|||
{{Соединения цинка}} |
|||
{{inorganic-compound-stub}} |
|||
[[Категория:Гидроксиды]] |
|||
| ⚫ | |||
[[Категория:Соединения цинка]] |
[[Категория:Соединения цинка]] |
||
[[Категория:Соединения кислорода]] |
|||
[[Категория:Соединения водорода]] |
|||
[[ar:هيدروكسيد الزنك]] |
|||
[[bg:Цинков дихидроксид]] |
|||
[[de:Zinkhydroxid]] |
|||
[[en:Zinc hydroxide]] |
|||
[[ja:水酸化亜鉛]] |
|||
[[nl:Zinkhydroxide]] |
|||
[[pl:Wodorotlenek cynku]] |
|||
[[pt:Hidróxido de zinco]] |
|||
[[simple:Zinc hydroxide]] |
|||
Текущая версия от 18:32, 13 ноября 2024
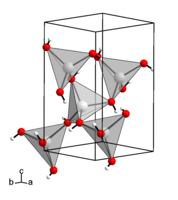
| Гидроксид цинка | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Гидроксид цинка |
| Хим. формула | Zn(OH)2 |
| Рац. формула | Zn(OH)2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 99,38474 г/моль |
| Плотность | 3,053 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 125 °C |
| Классификация | |
| Рег. номер CAS | 20427-58-1 |
| PubChem | 9812759 и 15839126 |
| Рег. номер EINECS | 243-814-3 |
| SMILES | |
| InChI | |
| ChemSpider | 7988510 и 21258001 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидрокси́д ци́нка — амфотерный гидроксид, имеющий формулу Zn(OH)2. Находит широкое применение в различных отраслях химии. Минерал Ашоверит.
Описание
[править | править код]Гидроксид цинка при стандартных условиях представляет собой бесцветные кристаллы, является аморфным веществом. В настоящее время известно 5 полиморфных модификаций, из которых устойчивой является только модификация с ромбической сингонией. Гидроксид цинка практически нерастворим в воде, проявляет амфотерные свойства (с преобладанием основных).[1]
Получение
[править | править код]- Взаимодействие растворимых солей цинка с щелочами:
Химические свойства
[править | править код]- Взаимодействие с кислотами с образованием соли и воды (реакция нейтрализации):
- Взаимодействие с кислотными оксидами:
- Взаимодействие с избыткoм аммиака:
;
- Взаимодействие со щелочами с образованием:
- Термическое разложение:
;
Применение
[править | править код]Гидроксид цинка применяют для синтеза различных соединений цинка, в основном, солей.
Примечания
[править | править код]- ↑ Гидроксид цинка, характеристика, свойства и получение, химические реакции. Вторая индустриализация России (29 октября 2019). Дата обращения: 27 сентября 2022. Архивировано 27 сентября 2022 года.





_{2}}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/81a5eeb0c0674c322bc19aea96d2b56a75510ef2)

![{\displaystyle {\mathsf {Zn(OH)_{2}+2NaOH\longrightarrow Na_{2}[Zn(OH)_{4}]}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/552314e583c6f80809ab19c115a5e0f533967e6b)
