Европий: различия между версиями
| [непроверенная версия] | [непроверенная версия] |
WWBM (обсуждение | вклад) мНет описания правки Метка: ссылка на неоднозначность |
|||
| (не показаны 253 промежуточные версии, сделанные более чем 100 участниками) | |||
| Строка 1: | Строка 1: | ||
{{перенаправление|Eu|}} |
|||
{{Химический_элемент|Европий / Europium (Eu)<!--Название-->|63<!--Атомный номер-->|мягкий серебристо-белый металл<!-- Внешний вид-->|151,965<!--Атомный вес-->|199<!--Радиус атома-->|546,9 (5,67)<!--Энергия ионизации-->|[Xe] 4f<sup>7</sup> 6s<sup>2</sup><!--Электронная конфигурация-->|185<!--Ковалентный радиус-->|(+3e) 95 (+2e) 109<!--Радиус иона-->|1,2<!--Электроотрицательность-->|Eu←Eu<sup>3+</sup> -1,99 В<br />Eu←Eu<sup>2+</sup> -2,80 В<!--Электродный потенциал-->|3, 2<!--Степени окисления-->|5,243<!--Плотность-->|0,176<!--Удельная теплоёмкость-->|13,9<!--Теплопроводность-->|1 095<!--Температура плавления-->|n/a<!--Теплота плавления-->|1 870<!--Температура кипения-->|176<!--Теплота испарения-->|28,9<!--Молярный объём-->|кубическая<br>объёмноцентрированая<!--Структура решётки-->|4,610<!--Период решётки-->|n/a<!--Отношение c/a-->|n/a<!--Температура Дебая-->}} |
|||
{{Карточка химического элемента |
|||
== История == |
|||
| имя = Европий / Europium (Eu) |
|||
Элемент был выделен в [[1886]] году из смеси редкоземельных элементов французским химиком [[Демарсе, Эжен Анатоль|Э. А. Демарсе]]. Его существование было подтверждено спектральным анализом лишь через 15 лет. |
|||
| символ = Eu |
|||
| номер = 63 |
|||
| внизу = [[Америций|Am]] |
|||
| изображение = Eu-Block.jpg |
|||
| подпись = Очищенный европий (~300 г, чистота 99,998%) |
|||
| внешний вид = |
|||
| атомная масса = 151,964(1)<ref name="iupac atomic weights">{{статья|автор=Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu.|заглавие=Atomic weights of the elements 2011 (IUPAC Technical Report)|ссылка=http://iupac.org/publications/pac/85/5/1047/|язык=en|издание=[[Pure and Applied Chemistry]]|год=2013|том=85|номер=5|страницы=1047—1078|doi=10.1351/PAC-REP-13-03-02|archivedate=2014-02-05|archiveurl=https://web.archive.org/web/20140205213140/http://www.iupac.org/publications/pac/85/5/1047/}}</ref> |
|||
| радиус атома = 199 |
|||
| энергия ионизации 1 = 546,9 (5,67) |
|||
| группа = 3 (устар. IIIB) |
|||
| период = 6 |
|||
| блок = <br>[[f-элементы|f-элемент]] |
|||
| конфигурация = [Xe] 6s<sup>2</sup>4f<sup>7</sup> |
|||
| ковалентный радиус = 185 |
|||
| радиус иона = (+3e) 95 (+2e) 109 |
|||
| электроотрицательность = 1,2 |
|||
| электродный потенциал = Eu←Eu<sup>3+</sup> -1,99 В<br>Eu←Eu<sup>2+</sup> -2,80 В |
|||
| степени окисления = +2, +3 |
|||
| плотность = 5,243 |
|||
| теплоёмкость = 27,656<ref name="ХЭ">{{книга |
|||
|автор = Редкол.:Кнунянц И. Л. (гл. ред.) |
|||
|часть = |
|||
|заглавие = Химическая энциклопедия: в 5 т |
|||
|оригинал = |
|||
|ссылка = |
|||
|ответственный = |
|||
|издание = |
|||
|место = Москва |
|||
|издательство = Советская энциклопедия |
|||
|год = 1990 |
|||
|том = 2 |
|||
|страницы = 126 |
|||
|страниц = 671 |
|||
|серия = |
|||
|isbn = |
|||
|тираж = 100000 |
|||
}} |
|||
</ref> |
|||
| теплопроводность = 13,9 |
|||
| температура плавления = 1099 [[кельвин|К]] (826 °C) |
|||
| теплота плавления = 9,21 |
|||
| температура кипения = 1802 K (1529 °C) |
|||
| теплота испарения = 176 |
|||
| молярный объём = 28,9 |
|||
| структура решётки = Кубическая<br>объёмноцентрированая |
|||
| параметры решётки = 4,581 |
|||
| отношение c/a = |
|||
| температура Дебая = |
|||
}} |
|||
{{Элемент периодической системы|align=center|fontsize=100%|number=63}} |
|||
'''Евро́пий''' ([[Химические знаки|химический символ]] — '''Eu''', от {{lang-la|'''Eu'''ropium}}) — [[химический элемент]] [[3 группа элементов|3-й группы]] (по [[Короткая форма периодической системы элементов|устаревшей классификации]] — побочной подгруппы третьей группы, IIIB) [[Шестой период периодической системы|шестого периода]] [[Периодическая система химических элементов|периодической системы химических элементов]] [[Менделеев, Дмитрий Иванович|Д. И. Менделеева]] с [[атомный номер|атомным номером]] 63. |
|||
Относится к семейству [[Лантаноиды|лантаноидов]]. |
|||
== Происхождение названия == |
|||
После подтверждения существования нового элемента Демарсе дал ему название европий — в честь [[Европа|Европы]]. |
|||
[[Простое вещество]] европий — это мягкий [[Редкоземельные элементы|редкоземельный]] [[металл]] серебристо-белого цвета, легко [[Окисление|окисляющийся]] на воздухе. |
|||
== Получение == |
|||
{{sect-stub}} |
|||
{{-|left}} |
|||
=== Цены === |
|||
Цена на оксид европия чистотой 99,9% в 2008 году составляет $400-$600 долларов США за килограмм <ref>[http://www.stanfordmaterials.com/eu.html]</ref>. |
|||
== История == |
|||
Цена на металлический европий чистотой 99.9% в 2008 году составляет $1980-$1300 за килограмм <ref>[http://www.stanfordmaterials.com/eu.html]</ref> |
|||
Первыми спектральные линии, отнесённые впоследствии к европию, наблюдали [[Крукс, Уильям|Крукс]] ([[1886 год в науке|1886]]) и [[Лекок де Буабодран, Поль Эмиль|Лекок де Буабодран]] ([[1892 год в науке|1892]]). [[Демарсе, Эжен Анатоль|Демарсе]] обнаружил полосу спектра элемента в [[Редкоземельные элементы#Термин|самариевой земле]] в [[1896 год в науке|1896 году]], а в [[1901 год в науке|1901 году]] смог выделить элемент, описал его и дал ему название в честь [[Европа|Европы]]<ref>{{ВТ-ЭСБЕ|Европий}}</ref>. |
|||
== Нахождение в природе == |
|||
{{Главная|Соединения европия}} |
|||
=== Месторождения === |
|||
Европий входит в состав [[лантаноид]]ов, которые часто встречаются в [[Российская Федерация|России]], [[Казахстан]]e, [[США]], [[Австралия|Австралии]], [[Бразилия|Бразилии]], [[Индия|Индии]], [[Скандинавия|Скандинавии]]. Крупнейшее в мире месторождение европия находится в [[Кения|Кении]]<ref>{{Cite web |url=http://www.catalogmineralov.ru/deposit/kenia/ |title=Полезные ископаемые Кении |access-date=2015-11-16 |archive-date=2015-11-17 |archive-url=https://web.archive.org/web/20151117031442/http://www.catalogmineralov.ru/deposit/kenia/ |deadlink=no }}</ref>. Значительны запасы в глубоководном месторождении редкоземельных минералов у тихоокеанского острова [[Минамитори]] в исключительной экономической зоне Японии<ref>{{Cite web |url=https://www.nature.com/articles/s41598-018-23948-5.pdf |title=The tremendous potential of deepsea mud as a source of rare-earth elements |access-date=2019-01-01 |archive-date=2019-01-23 |archive-url=https://web.archive.org/web/20190123175230/https://www.nature.com/articles/s41598-018-23948-5.pdf |deadlink=no }}</ref>. |
|||
== Физические свойства == |
== Физические свойства == |
||
[[Файл:Hexagonal.png|слева|мини|Кристаллическая структура европия при давлении свыше 12,5 ГПа.]] |
|||
В чистом виде — мягкий серебристо-белый металл, легко поддаётся механической обработке в инертной атмосфере. |
|||
Полная электронная конфигурация атома европия: 1s<sup>2</sup>2s<sup>2</sup>2p<sup>6</sup>3s<sup>2</sup>3p<sup>6</sup>4s<sup>2</sup>3d<sup>10</sup>4p<sup>6</sup>5s<sup>2</sup>4d<sup>10</sup>5p<sup>6</sup>6s<sup>2</sup>4f<sup>7</sup>. |
|||
Европий (в чистом виде) представляет собой мягкий серебристо-белый [[Металлы|металл]]. Он имеет необычно низкую плотность (5,243 г/см³), температуру плавления (826 °C) и температуру кипения (1440 °C) по сравнению со своими соседями по периодической системе элементов [[Гадолиний|гадолинием]] и [[Самарий|самарием]]. Эти величины противоречат явлению [[Лантаноидное сжатие|лантаноидного сжатия]] из-за влияния [[Электронная конфигурация|электронной конфигурации]] атома европия [Xe]4f<sup>7</sup>6s<sup>2</sup> на его свойства. Так как электронная оболочка f атома европия заполнена наполовину, для образования [[Металлическая связь|металлической связи]] предоставлены только два электрона, притяжение которых к ядру ослаблено и приводит к существенному увеличению радиуса атома. Аналогичное явление наблюдается также у атома [[Иттербий|иттербия]]. При нормальных условиях европий имеет кубическую [[Объемноцентрированная кубическая|объёмно-центрированную]] кристаллическую решетку с постоянной решетки 4,581 Å. При кристаллизации под высоким давлением европий образует ещё две модификации кристаллической решетки. При этом последовательность модификаций при возрастании давления отличается от такой последовательности у других лантаноидов, что наблюдается также и у [[Иттербий|иттербия]]. Первый фазовый переход происходит при давлении свыше 12,5 ГПа, при этом европий образует [[Гексагональная сингония|гексагональную]] кристаллическую решетку с параметрами a = 2,41 Å и c = 5,45 Å. При давлении свыше 18 ГПа европий образует аналогичную гексагональную кристаллическую решетку с более плотной упаковкой. Ионы европия, встроенные в кристаллическую решетку некоторых соединений, способны вызывать интенсивную [[Флуоресценция|флуоресценцию]], причем длина волны излучаемого света зависит от степени окисления [[ион]]ов европия. Eu<sup>3+</sup> практически независимо от того вещества, в кристаллическую решетку которого он встроен, испускает свет с длиной волны 613 и 618 нм, что соответствует интенсивному красному цвету. Напротив, максимальная эмиссия Eu<sup>2+</sup> сильно зависит от строения кристаллической решетки вещества-хозяина и, например, в случае алюмината бария-магния длина волны испускаемого света составляет 447 нм и находится в синей части спектра, а в случае алюмината стронция (SrAl<sub>2</sub>O<sub>4</sub>:Eu<sup>2+</sup>) длина волны составляет 520 нм и находится в зелёной части спектра видимого света. При давлении 80 ГПа<ref name="cmp">[http://www.compulenta.ru/news/426334/ Компьюлента]{{Недоступная ссылка|date=2019-11|bot=InternetArchiveBot }}</ref> и температуре 1,8 К европий приобретает [[Сверхпроводимость|сверхпроводящие свойства]]. |
|||
=== Изотопы === |
|||
{{main|Изотопы европия}} |
|||
Природный европий состоит из двух изотопов, <sup>151</sup>Eu и <sup>153</sup>Eu, в соотношении примерно 1:1. Европий-153 имеет [[Изотопная распространённость|природную распространённость]] 52,2 %, он стабилен. Изотоп европий-151 составляет 47,8 % природного европия. Недавно была обнаружена<ref>{{статья |заглавие=Search for α decay of natural europium |doi=10.1016/j.nuclphysa.2007.03.001 |издание=[[Nuclear Physics|Nuclear Physics A]] |том=789 |страницы=15—29 |bibcode=2007NuPhA.789...15B |язык=en |автор=Belli P., Bernabei R., Cappella F., Cerulli R., Dai C., Danevich F., Dangelo A., Incicchitti A., Kobychev V., Nagorny S. S., Nisi S., Nozzoli F., Prosperi D., Tretyak V.I., Yurchenko S.S. |год=2007 |тип=journal}}</ref> его слабая [[Альфа-распад|альфа-радиоактивность]] с [[Период полураспада|периодом полураспада]] около {{nobr|5×10<sup>18</sup> лет}}, что соответствует примерно 1 распаду за 2 минуты в килограмме природного европия. Кроме этого природного радиоизотопа, созданы и исследованы 35 искусственных радиоизотопов европия, среди которых наиболее устойчивы <sup>150</sup>Eu (период полураспада 36,9 года), <sup>152</sup>Eu (13,516 года) и <sup>154</sup>Eu (8,593 года). Обнаружены также 8 [[ядерная изомерия|метастабильных возбуждённых состояний]], среди которых наиболее стабилен <sup>150m</sup>Eu (12,8 часа), <sup>152m1</sup>Eu (9,3116 часа) и <sup>152m2</sup>Eu (96 минут)<ref name="nucleonica">{{cite web |url=http://www.nucleonica.net/unc.aspx |title=Nucleonica: Universal Nuclide Chart |author=Nucleonica |date=2007–2011 |work=Nucleonica: Universal Nuclide Chart |publisher=Nucleonica |accessdate=2011-07-22 |archive-date=2017-02-19 |archive-url=https://web.archive.org/web/20170219043412/http://www.nucleonica.net/unc.aspx |deadlink=no }}</ref>. |
|||
== Химические свойства == |
== Химические свойства == |
||
Европий является типичным активным металлом и вступает в реакции с большинством неметаллов. Европий в группе лантаноидов имеет максимальную реакционную способность. На воздухе быстро окисляется, на поверхности металла всегда есть оксидная плёнка. Хранят в банках или ампулах под слоем жидкого [[парафин]]а или в [[керосин]]е. При нагревании на воздухе до температуры 180 °C воспламеняется и горит с образованием [[Оксид европия(III)|оксида европия(III)]]. |
|||
На воздухе быстро окисляется, поэтому его хранят в банках или ампулах под слоем жидкого [[парафин]]а. Очень активный и может |
|||
вытеснять из растворов солей почти все металлы. |
|||
<math>\mathrm{4\ Eu + 3\ O_2 \longrightarrow 2\ Eu_2O_3}</math> |
|||
В соединениях, как и большинство [[РЗЭ]], проявляет преимущественно [[валентность]] +3, при определённых условиях (например, электрохимическим восстановлением, восстановлением амальгамой цинка и др.) можно получить [[степень окисления]] +2. |
|||
Очень активен, может вытеснять из растворов солей почти все металлы. В соединениях, как и большинство [[РЗЭ]], проявляет преимущественно [[степень окисления]] +3, при определённых условиях (например, электрохимическим восстановлением, восстановлением амальгамой цинка и др.) можно получить степень окисления +2. Также при изменении окислительно-восстановительных условий возможно получение степени окисления +2 и +3, что соответствует оксиду с химической формулой [[Оксид европия(II,III)|Eu<sub>3</sub>O<sub>4</sub>]]. С водородом европий образует нестехиометрические фазы, в которых атомы водорода находятся в промежутках кристаллической решетки между атомами европия. Европий растворяется в аммиаке с образованием раствора синего цвета, что обусловлено, как и в подобных растворах щелочных металлов, образованием [[сольватированных электронов]]. |
|||
== Получение == |
|||
Металлический европий получают восстановлением Eu<sub>2</sub>O<sub>3</sub> в вакууме лантаном или углеродом, а также электролизом расплава [[Хлорид европия(III)|EuCl<sub>3</sub>]]. |
|||
== Применение == |
== Применение == |
||
=== |
=== Ядерная энергетика === |
||
Европий используется в качестве поглотителя [[нейтрон]]ов (в основном окись европия, гексаборид и борат европия) в [[Атомный реактор|атомных реакторах]], но окись постепенно «выгорает», и по срокам эксплуатации уступает карбиду бора в 1,5 раза (хотя имеет |
Европий используется в [[Ядерная энергетика|ядерной энергетике]] в качестве поглотителя [[нейтрон]]ов (в основном [[окись европия]], [[Гексаборид европия|гексаборид]] и [[борат европия]]) в [[Атомный реактор|атомных реакторах]], но окись постепенно «выгорает», и по срокам эксплуатации уступает [[Карбид бора|карбиду бора]] в 1,5 раза (хотя имеет преимущество в почти полном отсутствии газовыделения и распухания в мощном потоке нейтронов, например, реактор [[БН-600]]). Сечение захвата тепловых нейтронов европием (природной смесью изотопов) составляет около {{nobr|4500 [[барн]]}}, самым активным в отношении захвата нейтронов является европий-151 ({{nobr|9200 барн}}). |
||
=== |
=== Атомно-водородная энергетика === |
||
Оксид европия применяется при термохимическом разложении воды в атомно-водородной энергетике (европий-стронций-йодидный цикл). |
[[Оксид европия]] применяется при термохимическом разложении воды в [[Атомно-водородная энергетика|атомно-водородной энергетике]] (европий-стронций-йодидный цикл). |
||
=== |
=== Лазерные материалы === |
||
Ионы европия служат для генерации |
Ионы европия служат для генерации [[лазер]]ного излучения в видимой области спектра с длиной волны {{nobr|0,61 мкм}} (оранжевые лучи), поэтому оксид европия используется для создания твердотельных, и менее распространённых жидкостных лазеров. |
||
=== |
=== Электроника === |
||
Европий является легирующей примесью в моносульфиде самария (термоэлектрогенераторы), а |
Европий является легирующей примесью в [[моносульфид самария|моносульфиде самария]] (термоэлектрогенераторы), а также как легирующий компонент для синтеза алмазоподобного (сверхтвердого) [[Нитрид углерода|нитрида углерода]]. |
||
Силицид европия в виде тонких пленок находит применение в интегральной [[микроэлектроника|микроэлектронике]]. |
|||
[[Силицид европия]] в виде тонких плёнок находит применение в интегральной [[микроэлектроника|микроэлектронике]]. |
|||
Моноокись европия а так же сплав моноокиси европия и моноокиси самария применяются в виде тонких пленок в качестве магнитных полупроводниковых материалов для стремительно развивающейся функциональной электроники, и в частности МДП — электроники. |
|||
[[Моноокись европия]], а также сплав моноокиси европия и [[моноокись самария|моноокиси самария]] применяются в виде тонких плёнок в качестве магнитных полупроводниковых материалов для функциональной электроники и, в частности, МДП-электроники. |
|||
=== [[Люминофоры]] === |
|||
* Вольфрамат европия практически очень важный используемый микроэлектроникой люминофор. |
|||
* Легированный европием борат стронция используется как люминофор в [[Лампа_чёрного_света|лампах черного света]]. |
|||
=== Люминофоры === |
|||
=== Европий в [[медицина|медицине]] === |
|||
* Европий — непременная составляющая [[люминофор]]ов, используемых в электронно-лучевых и [[Плазменная панель|плазменных]] цветных экранах. |
|||
[[Катион]]ы европия давно и успешно используются в медицине в качестве [[Флуоресценция|флуоресцентных]] зондов. |
|||
* Купюры евро защищены от подделок люминофорами на основе европия. |
|||
* [[Вольфрамат европия]] — люминофор, используемый в микроэлектронике. |
|||
* Легированный европием [[борат стронция]] используется как люминофор в [[Лампа чёрного света|лампах чёрного света]]. |
|||
=== Медицина === |
|||
[[Катион]]ы европия используются в медицинской диагностике в качестве [[Флуоресценция|флуоресцентных]] зондов. |
|||
Радиоактивные [[изотопы]] европия применяются при лечении некоторых форм [[Рак (заболевание)|рака]]. |
Радиоактивные [[изотопы]] европия применяются при лечении некоторых форм [[Рак (заболевание)|рака]]. |
||
=== Другие сферы применения |
=== Другие сферы применения === |
||
* |
* Интенсивно изучаются светочувствительные соединения европия с бромом, хлором и иодом. |
||
* Европий-154 обладает большой мощностью тепловыделения при радиоактивном распаде и предложен в качестве |
* Европий-154 обладает большой мощностью тепловыделения при радиоактивном распаде и предложен в качестве источника в [[радиоизотопные источники энергии|радиоизотопных источниках энергии]]. |
||
== Влияние на качество воды == |
|||
== Биологическая роль == |
|||
В реакциях с водой европий химически ведёт себя как кальций. При уровнях [[Водородный показатель|рН]] ниже 6 европий способен мигрировать в воде в ионном виде. При более высоких уровнях рН европий образует плохо растворимые и, соответственно, менее подвижные гидроксиды. При контакте с кислородом воздуха происходит дальнейшее окисление до Eu<sub>2</sub>O<sub>3</sub>. Максимально наблюдаемые концентрации европия в природных маломинерализованных водах составляют менее {{nobr|1 мкг/л}} (в морской воде — {{nobr|1,1{{e|−6}} мг/л}}). Влияние на качество воды при таких концентрациях представляется незначительным. Предельно допустимая концентрация (ПДК) в воде нормируется только российскими нормами и равна (для питьевой воды) {{nobr|0,3 мг/л}}. |
|||
{{в планах}} |
|||
== Пути поступления в организм == |
|||
Вероятность попадания европия в организм человека представляется незначительной. Возможно поступление европия в организм с водой в микроскопических количествах. Нельзя исключать вероятности и других путей попадания в организм у людей, сталкивающихся с соединениями европия на производстве. |
|||
== Потенциальная опасность для здоровья == |
|||
Европий относится к малотоксичным элементам. Нет какой-либо информации о последствиях воздействия европия на организм человека. |
|||
== Физиологическое значение == |
|||
На данный момент нет данных о какой-либо биологической роли европия в организме человека или животных. |
|||
== Цены == |
|||
Европий является одним из самых дорогих лантаноидов<ref>{{Cite web |url=http://www.periodictable.ru/063Eu/Eu.html |title=Периодическая таблица элементов — Европий |access-date=2010-05-26 |archive-date=2010-03-17 |archive-url=https://web.archive.org/web/20100317104700/http://www.periodictable.ru/063Eu/Eu.html |deadlink=no }}</ref>. В 2014 году цена металлического европия ЕВМ-1 составляла от 800 до 2000 долларов США за кг, а оксида европия чистотой 99,9 % — около 500 долларов за кг. |
|||
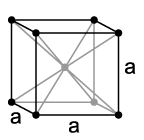
[[Файл:Cubic-body-centered.png|слева|мини|144x144пкс|Кристаллическая структура европия при нормальных условиях (а = 4,581 Å).]] |
|||
== Примечания == |
== Примечания == |
||
{{Примечания|2}} |
|||
{{reflist}} |
|||
== Ссылки == |
|||
{{chem-stub}} |
|||
{{Навигация|Тема=Европий|Викисловарь=европий}} |
|||
{{Шаблон:Периодическая система элементов}} |
|||
* [http://webelements.com/europium/ Данные о европии на сайте WebElements] {{Wayback|url=http://webelements.com/europium/ |date=20151119053414 }}. |
|||
[[Категория:Лантаноиды]] |
|||
* Sinha S.P. Europium. / Springer-Verlag New York Inc., 1967. — 164 p. — (Anorganische und allgemeine Chemie in Einzeldarstellungen. Herausgegeben von Margot Becke-Goehring. Band VIII). |
|||
{{Библиоинформация}} {{^|12px}} |
|||
[[af:Europium]] |
|||
{{Соединения европия}} |
|||
[[ar:يوروبيوم]] |
|||
{{Периодическая система элементов}} |
|||
[[be:Еўропій]] |
|||
{{Ряд Активности Металлов}} |
|||
[[bn:ইউরোপিয়াম]] |
|||
[[bs:Europijum]] |
|||
[[Категория:Химические элементы]] |
|||
[[ca:Europi]] |
|||
[[Категория:Лантаноиды]] |
|||
[[co:Europiu]] |
|||
[[cs:Europium]] |
|||
[[cy:Ewropiwm]] |
|||
[[da:Europium]] |
|||
[[de:Europium]] |
|||
[[el:Ευρώπιο]] |
|||
[[en:Europium]] |
|||
[[eo:Eŭropio]] |
|||
[[es:Europio]] |
|||
[[et:Euroopium]] |
|||
[[eu:Europio]] |
|||
[[fa:یوروپیوم]] |
|||
[[fi:Europium]] |
|||
[[fr:Europium]] |
|||
[[fur:Europi]] |
|||
[[gl:Europio]] |
|||
[[gv:Oarpium]] |
|||
[[he:אירופיום]] |
|||
[[hr:Europij]] |
|||
[[ht:Ewòpyòm]] |
|||
[[hu:Európium]] |
|||
[[hy:Եվրոպիում]] |
|||
[[id:Europium]] |
|||
[[io:Europio]] |
|||
[[it:Europio]] |
|||
[[ja:ユウロピウム]] |
|||
[[jbo:ronjinme]] |
|||
[[jv:Europium]] |
|||
[[kn:ಯುರೋಪಿಯಮ್]] |
|||
[[ko:유로퓸]] |
|||
[[kv:Европий]] |
|||
[[la:Europium]] |
|||
[[lb:Europium]] |
|||
[[lt:Europis]] |
|||
[[lv:Eiropijs]] |
|||
[[ml:യൂറോപ്പിയം]] |
|||
[[nl:Europium]] |
|||
[[nn:Europium]] |
|||
[[no:Europium]] |
|||
[[pl:Europ]] |
|||
[[pt:Európio]] |
|||
[[qu:Iwrupyu]] |
|||
[[ro:Europiu]] |
|||
[[sah:Эуропиум]] |
|||
[[scn:Europiu]] |
|||
[[sh:Europijum]] |
|||
[[simple:Europium]] |
|||
[[sk:Európium]] |
|||
[[sl:Evropij]] |
|||
[[sr:Еуропијум]] |
|||
[[stq:Europium]] |
|||
[[sv:Europium]] |
|||
[[ta:யூரோப்பியம்]] |
|||
[[tg:Европий]] |
|||
[[th:ยูโรเพียม]] |
|||
[[tr:Evropiyum]] |
|||
[[uk:Європій]] |
|||
[[vi:Europi]] |
|||
[[zh:铕]] |
|||
Текущая версия от 08:39, 12 августа 2024
| Европий | ||||
|---|---|---|---|---|
| ← Самарий | Гадолиний → | ||||
| ||||
| Внешний вид простого вещества | ||||
 Очищенный европий (~300 г, чистота 99,998%) |
||||
| Свойства атома | ||||
| Название, символ, номер | Европий / Europium (Eu), 63 | |||
| Группа, период, блок |
3 (устар. IIIB), 6, f-элемент |
|||
| Атомная масса (молярная масса) |
151,964(1)[1] а. е. м. (г/моль) | |||
| Электронная конфигурация | [Xe] 6s24f7 | |||
| Радиус атома | 199 пм | |||
| Химические свойства | ||||
| Ковалентный радиус | 185 пм | |||
| Радиус иона | (+3e) 95 (+2e) 109 пм | |||
| Электроотрицательность | 1,2 (шкала Полинга) | |||
| Электродный потенциал |
Eu←Eu3+ -1,99 В Eu←Eu2+ -2,80 В |
|||
| Степени окисления | +2, +3 | |||
| Энергия ионизации (первый электрон) |
546,9 (5,67) кДж/моль (эВ) | |||
| Термодинамические свойства простого вещества | ||||
| Плотность (при н. у.) | 5,243 г/см³ | |||
| Температура плавления | 1099 К (826 °C) | |||
| Температура кипения | 1802 K (1529 °C) | |||
| Мол. теплота плавления | 9,21 кДж/моль | |||
| Мол. теплота испарения | 176 кДж/моль | |||
| Молярная теплоёмкость | 27,656[2] Дж/(K·моль) | |||
| Молярный объём | 28,9 см³/моль | |||
| Кристаллическая решётка простого вещества | ||||
| Структура решётки |
Кубическая объёмноцентрированая |
|||
| Параметры решётки | 4,581 Å | |||
| Прочие характеристики | ||||
| Теплопроводность | (300 K) 13,9 Вт/(м·К) | |||
| Номер CAS | 7440-53-1 | |||
| 63 | Европий
|
| 4f76s2 | |
Евро́пий (химический символ — Eu, от лат. Europium) — химический элемент 3-й группы (по устаревшей классификации — побочной подгруппы третьей группы, IIIB) шестого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 63.
Относится к семейству лантаноидов.
Простое вещество европий — это мягкий редкоземельный металл серебристо-белого цвета, легко окисляющийся на воздухе.
История
[править | править код]Первыми спектральные линии, отнесённые впоследствии к европию, наблюдали Крукс (1886) и Лекок де Буабодран (1892). Демарсе обнаружил полосу спектра элемента в самариевой земле в 1896 году, а в 1901 году смог выделить элемент, описал его и дал ему название в честь Европы[3].
Нахождение в природе
[править | править код]Месторождения
[править | править код]Европий входит в состав лантаноидов, которые часто встречаются в России, Казахстанe, США, Австралии, Бразилии, Индии, Скандинавии. Крупнейшее в мире месторождение европия находится в Кении[4]. Значительны запасы в глубоководном месторождении редкоземельных минералов у тихоокеанского острова Минамитори в исключительной экономической зоне Японии[5].
Физические свойства
[править | править код]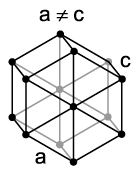
Полная электронная конфигурация атома европия: 1s22s22p63s23p64s23d104p65s24d105p66s24f7.
Европий (в чистом виде) представляет собой мягкий серебристо-белый металл. Он имеет необычно низкую плотность (5,243 г/см³), температуру плавления (826 °C) и температуру кипения (1440 °C) по сравнению со своими соседями по периодической системе элементов гадолинием и самарием. Эти величины противоречат явлению лантаноидного сжатия из-за влияния электронной конфигурации атома европия [Xe]4f76s2 на его свойства. Так как электронная оболочка f атома европия заполнена наполовину, для образования металлической связи предоставлены только два электрона, притяжение которых к ядру ослаблено и приводит к существенному увеличению радиуса атома. Аналогичное явление наблюдается также у атома иттербия. При нормальных условиях европий имеет кубическую объёмно-центрированную кристаллическую решетку с постоянной решетки 4,581 Å. При кристаллизации под высоким давлением европий образует ещё две модификации кристаллической решетки. При этом последовательность модификаций при возрастании давления отличается от такой последовательности у других лантаноидов, что наблюдается также и у иттербия. Первый фазовый переход происходит при давлении свыше 12,5 ГПа, при этом европий образует гексагональную кристаллическую решетку с параметрами a = 2,41 Å и c = 5,45 Å. При давлении свыше 18 ГПа европий образует аналогичную гексагональную кристаллическую решетку с более плотной упаковкой. Ионы европия, встроенные в кристаллическую решетку некоторых соединений, способны вызывать интенсивную флуоресценцию, причем длина волны излучаемого света зависит от степени окисления ионов европия. Eu3+ практически независимо от того вещества, в кристаллическую решетку которого он встроен, испускает свет с длиной волны 613 и 618 нм, что соответствует интенсивному красному цвету. Напротив, максимальная эмиссия Eu2+ сильно зависит от строения кристаллической решетки вещества-хозяина и, например, в случае алюмината бария-магния длина волны испускаемого света составляет 447 нм и находится в синей части спектра, а в случае алюмината стронция (SrAl2O4:Eu2+) длина волны составляет 520 нм и находится в зелёной части спектра видимого света. При давлении 80 ГПа[6] и температуре 1,8 К европий приобретает сверхпроводящие свойства.
Изотопы
[править | править код]Природный европий состоит из двух изотопов, 151Eu и 153Eu, в соотношении примерно 1:1. Европий-153 имеет природную распространённость 52,2 %, он стабилен. Изотоп европий-151 составляет 47,8 % природного европия. Недавно была обнаружена[7] его слабая альфа-радиоактивность с периодом полураспада около 5×1018 лет, что соответствует примерно 1 распаду за 2 минуты в килограмме природного европия. Кроме этого природного радиоизотопа, созданы и исследованы 35 искусственных радиоизотопов европия, среди которых наиболее устойчивы 150Eu (период полураспада 36,9 года), 152Eu (13,516 года) и 154Eu (8,593 года). Обнаружены также 8 метастабильных возбуждённых состояний, среди которых наиболее стабилен 150mEu (12,8 часа), 152m1Eu (9,3116 часа) и 152m2Eu (96 минут)[8].
Химические свойства
[править | править код]Европий является типичным активным металлом и вступает в реакции с большинством неметаллов. Европий в группе лантаноидов имеет максимальную реакционную способность. На воздухе быстро окисляется, на поверхности металла всегда есть оксидная плёнка. Хранят в банках или ампулах под слоем жидкого парафина или в керосине. При нагревании на воздухе до температуры 180 °C воспламеняется и горит с образованием оксида европия(III).
Очень активен, может вытеснять из растворов солей почти все металлы. В соединениях, как и большинство РЗЭ, проявляет преимущественно степень окисления +3, при определённых условиях (например, электрохимическим восстановлением, восстановлением амальгамой цинка и др.) можно получить степень окисления +2. Также при изменении окислительно-восстановительных условий возможно получение степени окисления +2 и +3, что соответствует оксиду с химической формулой Eu3O4. С водородом европий образует нестехиометрические фазы, в которых атомы водорода находятся в промежутках кристаллической решетки между атомами европия. Европий растворяется в аммиаке с образованием раствора синего цвета, что обусловлено, как и в подобных растворах щелочных металлов, образованием сольватированных электронов.
Получение
[править | править код]Металлический европий получают восстановлением Eu2O3 в вакууме лантаном или углеродом, а также электролизом расплава EuCl3.
Применение
[править | править код]Ядерная энергетика
[править | править код]Европий используется в ядерной энергетике в качестве поглотителя нейтронов (в основном окись европия, гексаборид и борат европия) в атомных реакторах, но окись постепенно «выгорает», и по срокам эксплуатации уступает карбиду бора в 1,5 раза (хотя имеет преимущество в почти полном отсутствии газовыделения и распухания в мощном потоке нейтронов, например, реактор БН-600). Сечение захвата тепловых нейтронов европием (природной смесью изотопов) составляет около 4500 барн, самым активным в отношении захвата нейтронов является европий-151 (9200 барн).
Атомно-водородная энергетика
[править | править код]Оксид европия применяется при термохимическом разложении воды в атомно-водородной энергетике (европий-стронций-йодидный цикл).
Лазерные материалы
[править | править код]Ионы европия служат для генерации лазерного излучения в видимой области спектра с длиной волны 0,61 мкм (оранжевые лучи), поэтому оксид европия используется для создания твердотельных, и менее распространённых жидкостных лазеров.
Электроника
[править | править код]Европий является легирующей примесью в моносульфиде самария (термоэлектрогенераторы), а также как легирующий компонент для синтеза алмазоподобного (сверхтвердого) нитрида углерода.
Силицид европия в виде тонких плёнок находит применение в интегральной микроэлектронике.
Моноокись европия, а также сплав моноокиси европия и моноокиси самария применяются в виде тонких плёнок в качестве магнитных полупроводниковых материалов для функциональной электроники и, в частности, МДП-электроники.
Люминофоры
[править | править код]- Европий — непременная составляющая люминофоров, используемых в электронно-лучевых и плазменных цветных экранах.
- Купюры евро защищены от подделок люминофорами на основе европия.
- Вольфрамат европия — люминофор, используемый в микроэлектронике.
- Легированный европием борат стронция используется как люминофор в лампах чёрного света.
Медицина
[править | править код]Катионы европия используются в медицинской диагностике в качестве флуоресцентных зондов. Радиоактивные изотопы европия применяются при лечении некоторых форм рака.
Другие сферы применения
[править | править код]- Интенсивно изучаются светочувствительные соединения европия с бромом, хлором и иодом.
- Европий-154 обладает большой мощностью тепловыделения при радиоактивном распаде и предложен в качестве источника в радиоизотопных источниках энергии.
Влияние на качество воды
[править | править код]В реакциях с водой европий химически ведёт себя как кальций. При уровнях рН ниже 6 европий способен мигрировать в воде в ионном виде. При более высоких уровнях рН европий образует плохо растворимые и, соответственно, менее подвижные гидроксиды. При контакте с кислородом воздуха происходит дальнейшее окисление до Eu2O3. Максимально наблюдаемые концентрации европия в природных маломинерализованных водах составляют менее 1 мкг/л (в морской воде — 1,1⋅10−6 мг/л). Влияние на качество воды при таких концентрациях представляется незначительным. Предельно допустимая концентрация (ПДК) в воде нормируется только российскими нормами и равна (для питьевой воды) 0,3 мг/л.
Пути поступления в организм
[править | править код]Вероятность попадания европия в организм человека представляется незначительной. Возможно поступление европия в организм с водой в микроскопических количествах. Нельзя исключать вероятности и других путей попадания в организм у людей, сталкивающихся с соединениями европия на производстве.
Потенциальная опасность для здоровья
[править | править код]Европий относится к малотоксичным элементам. Нет какой-либо информации о последствиях воздействия европия на организм человека.
Физиологическое значение
[править | править код]На данный момент нет данных о какой-либо биологической роли европия в организме человека или животных.
Цены
[править | править код]Европий является одним из самых дорогих лантаноидов[9]. В 2014 году цена металлического европия ЕВМ-1 составляла от 800 до 2000 долларов США за кг, а оксида европия чистотой 99,9 % — около 500 долларов за кг.
Примечания
[править | править код]- ↑ Michael E. Wieser, Norman Holden, Tyler B. Coplen, John K. Böhlke, Michael Berglund, Willi A. Brand, Paul De Bièvre, Manfred Gröning, Robert D. Loss, Juris Meija, Takafumi Hirata, Thomas Prohaska, Ronny Schoenberg, Glenda O’Connor, Thomas Walczyk, Shige Yoneda, Xiang‑Kun Zhu. Atomic weights of the elements 2011 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2013. — Vol. 85, no. 5. — P. 1047—1078. — doi:10.1351/PAC-REP-13-03-02. Архивировано 5 февраля 2014 года.
- ↑ Редкол.:Кнунянц И. Л. (гл. ред.). Химическая энциклопедия: в 5 т. — Москва: Советская энциклопедия, 1990. — Т. 2. — С. 126. — 671 с. — 100 000 экз.
- ↑ Европий // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- ↑ Полезные ископаемые Кении. Дата обращения: 16 ноября 2015. Архивировано 17 ноября 2015 года.
- ↑ The tremendous potential of deepsea mud as a source of rare-earth elements. Дата обращения: 1 января 2019. Архивировано 23 января 2019 года.
- ↑ Компьюлента (недоступная ссылка)
- ↑ Belli P., Bernabei R., Cappella F., Cerulli R., Dai C., Danevich F., Dangelo A., Incicchitti A., Kobychev V., Nagorny S. S., Nisi S., Nozzoli F., Prosperi D., Tretyak V.I., Yurchenko S.S. Search for α decay of natural europium (англ.) // Nuclear Physics A : journal. — 2007. — Vol. 789. — P. 15—29. — doi:10.1016/j.nuclphysa.2007.03.001. — .
- ↑ Nucleonica. Nucleonica: Universal Nuclide Chart. Nucleonica: Universal Nuclide Chart. Nucleonica (2007–2011). Дата обращения: 22 июля 2011. Архивировано 19 февраля 2017 года.
- ↑ Периодическая таблица элементов — Европий. Дата обращения: 26 мая 2010. Архивировано 17 марта 2010 года.
Ссылки
[править | править код]- Данные о европии на сайте WebElements Архивная копия от 19 ноября 2015 на Wayback Machine.
- Sinha S.P. Europium. / Springer-Verlag New York Inc., 1967. — 164 p. — (Anorganische und allgemeine Chemie in Einzeldarstellungen. Herausgegeben von Margot Becke-Goehring. Band VIII).