Бутил: различия между версиями
| [непроверенная версия] | [непроверенная версия] |
Нет описания правки |
м (1195) Метки: через визуальный редактор с мобильного устройства из мобильной версии через расширенный мобильный режим |
||
| (не показано 69 промежуточных версий 51 участника) | |||
| Строка 1: | Строка 1: | ||
'''Бутил''' — одновалентный [[Углеводородный радикал|радикал]] [[Бутан (вещество)|бутана]], или [[Земеститель (химия)|заместитель]] с формулой −С<sub>4</sub>Н<sub>9</sub>, производное бутана или [[изобутан]]а (С<sub>4</sub>Н<sub>10</sub>). Часто встречается в качестве заместителя в [[органические вещества|органических веществах]]. |
|||
'''Бутил''' С<sub>4</sub>Н<sub>9</sub> – одновалентный [[Радикал (химия)|радикал]] [[бутан]]а (С<sub>3</sub>Н<sub>8</sub>). Часто является заместителем в [[углеводород]]ах. |
|||
'''н-[[бутан (вещество)|Бутан]]''' может быть замещён как в оба терминальных атома, так и в два центральных. |
|||
'''Нормальный, или н-бутил''': CH<sub>3</sub>−CH<sub>2</sub>−CH<sub>2</sub>−CH<sub>2</sub>− (систематическое название: бутил) |
|||
'''Вторичный бутил''', или '''втор-бутил''': CH<sub>3</sub>−CH<sub>2</sub>−CH(CH<sub>3</sub>)− (систематическое название: 1-метилпропил) |
|||
stub |
|||
Другой разветвлённый изомер бутана — [[изобутан]], может быть замещённым по трём терминальным атомам или по центральному |
|||
Butyl |
|||
'''[[Изобутил]]''': (CH<sub>3</sub>)<sub>2</sub>CH−CH<sub>2</sub>− (систематическое название: 2-метилпропил) |
|||
'''Третичный бутил''', '''трет-бутил''': (CH<sub>3</sub>)<sub>3</sub>C− (систематическое название: 1,1-диметилэтил) |
|||
== Номенклатура == |
|||
Согласно [[номенклатура ИЮПАК|номенклатуре ИЮПАК]], обозначения «изобутил», «''втор''-бутил», и «''трет''-бутил» могут использоваться в качестве тривиальных. |
|||
{| class="wikitable" |
|||
! [[Структурная формула]] |
|||
! Устоявшееся название |
|||
! Номенклатура ИЮПАК |
|||
! Систематическое имя |
|||
! Альтернативные названия |
|||
|- |
|||
|[[Файл:N-Butyl-Skeletal-SVG.svg|100px]] |
|||
|''н''-бутил |
|||
|бутил |
|||
|бутил |
|||
|бутан-1-ил |
|||
|- |
|||
|[[Файл:Isobutyl-Skeletal-SVG.svg|80px]] |
|||
|изобутил |
|||
|изобутил |
|||
|2-метилпропил |
|||
|2-метилпропан-1-ил |
|||
|- |
|||
|[[Файл:Sec-Butyl-Skeletal-SVG.svg|80px]] |
|||
|''втор''-бутил |
|||
|''втор''-бутил |
|||
|1-метилпропил |
|||
|бутан-2-ил |
|||
|- |
|||
|[[Файл:Tert-butyl-group-2D-skeletal.svg|60px]] |
|||
|''трет''-бутил |
|||
|''трет''-бутил |
|||
|1,1-диметилэтил |
|||
|2-метилпропан-2- |
|||
|} |
|||
Бутил — самый большой алкильный заместитель, имеющий тривиальное название. |
|||
Префикс ''изо-'', ''втор-'' и ''трет-'' обозначают количество разветвлений цепи (также известен как R<sup>I</sup>). ''Изо'' — означает — одно, ''втор''- два и ''трет-'' три. |
|||
== Примеры == |
|||
Ниже представлены варианты бутильных заместителей на примере изомеров «бутил ацетата» |
|||
{| |
|||
|[[Файл:Butylacetat.svg|200px|butyl acetate]] |
|||
|[[Файл:Isobutyl acetate.svg|150px|isobutyl acetate]] |
|||
|[[Файл:Sec-butyl acetate.svg|150px|sec-butyl acetate]] |
|||
|[[Файл:Tert-Butylacetat.svg|120px|tert-butyl acetate]] |
|||
|- |
|||
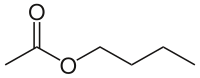
|<center>[[Бутилацетат|''н''-бутил ацетат]]</center> |
|||
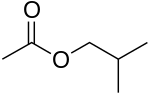
|<center>[[изобутилацетат]]</center> |
|||
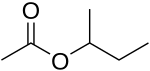
|<center>[[втор-бутилацетат]]</center> |
|||
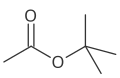
|<center>[[трет-бутилацетат]]</center> |
|||
|} |
|||
== Этимология == |
|||
С ростом количества атомов углерода радикал бутил стал последним названым исторически, а не с использованием греческого счёта. Название «бутил» происходит от английского названия [[Масляная кислота|масляной кислоты]] ({{lang-en|butyric acid}}), которая так названа оттого, что она содержится в прогорклом масле ({{lang-en|butter}}, которое, в свою очередь, восходит к {{lang-la|butyrum}} — масло). |
|||
== Стерические свойства == |
|||
С увеличивающейся разветвлённости проявляются стрерические требование бутильной группы. ''Трет''-бутил группа создаёт стерическое напряжение вокруг себя. Это может стабилизировать вещество благодаря блокировке реакционного центра, что соответственно меняет кинетику реакции: ускорять или замедлять реакцию. В большинстве случаев происходит торможение из-за стерического отталкивания фрагентов молекулы. Ускорение происходит, когда трет-бутил фиксирует необходимую для протекания реакции [[Конформация|конформацию]]. |
|||
== Якорная группа == |
|||
Изобутил также как и трет-бутилгруппа способна применяться как якорная группа. Это означает, что благодаря своему стерическому эффекту изменяет предпочтения конформаций в молекуле. Так для примера отталкивание свободных алкильных групп затрудняется либо предотвращается переход из одной конформацию циклогексанового кольца в другую. Громоздкий трет-бутильный остаток остаётся предпочтительно в [[экваториальном]] положении, так как при этом уменьшается взаимодействия с другими заместителями в циклогексановом кольце. Во-вторых, возможная конформация кресла с остатком [[аксиальном]] положении, вследствие проявляется отталкивания с другими аксиальными группами. Это энергетически неблагоприятно, и равновесие смещено в сторону занятия трет-бутильной группы экваториальной конформации. |
|||
== Трет-бутиловый эффект == |
|||
Трет-бутильный заместитель стерически очень требователен и используется в химии [[kinetic reaction control|кинетической стабилизации]] вместе с другими объёмными группами, такими как [[Триметилхлорсилан|триметилсилильная]] группа. Эффект, который проявляет трет-бутильная группа воздействуя на прогресс химической реакции называют '''трет-бутиловый эффект'''. |
|||
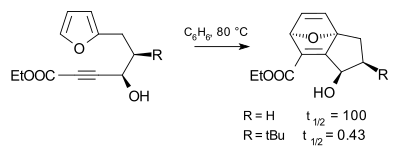
Этот эффект иллюстрируется в реакции [[Реакция Дильса-Альдера|Дильса-Альдера]] ниже, где трет-бутильный заместитель изменяет [[коэффициент скорости реакции]] более чем в 240 раз по сравнению с водородом как заместителя<ref>''Factors affecting ease of ring formation. The effect of anchoring substitution on the rate of an intramolecular diels-alder reaction with furan-diene'' Serge Cauwberghs and Pierre J. De Clercq B. Tinant and J. P. Declercq ''Tetrahedron Letters'' Volume 29, Issue 20 , '''1988''', Pages 2493—2496 {{doi|10.1016/S0040-4039(00)87916-2}}.</ref>. |
|||
[[Файл:Tertbutyleffect.svg|center|400px|Трет-бутиловый эффект]] |
|||
== Электроноакцепторные свойства == |
|||
Благодаря различным позициям, которыми бутильные группы могут соединяться с остальной молекулой, он проявляет различные электроакцепторные свойства. Так между изомерами бутильного остатка [[электронная плотность]] у третичного атома углерода ''трет''-бутилгруппы наибольшая, а у ''н''-бутила наиболее низкая. Это отражается в повышении [[Основание (химия)|основных]] свойств [[литий|литированных]] веществ от ''н''-бутиллития, через ''втор''-бутиллитий к ''трет''-бутиллитию. Подобный эффект увеличения основности существует и в ряду 1-бутанол, 2-бутанол, ''трет''-бутанол. |
|||
== Применение == |
|||
[[Файл:BuLi is.svg|thumb|Структура н-бутиллития]] |
|||
Алкиллитий сильное [[металлорганика|металлорганическое]] основание. Он может депротонировать очень слабые [[кислота|кислоты]], ровно как и литировать вещества. Коммерчески доступны три основания бутиллития, как стандартные реактивы: ''н''-бутиллитий, ''втор''-бутиллитий и ''трет''-бутиллитий. |
|||
[[гидрирование|Гидрирующий]] агент [[диизобутилалюминий гидрид]] содержит два [[изобутил]]ьных остатка. |
|||
== Примечания == |
|||
{{примечания}} |
|||
== Ссылки == |
|||
{{wiktionary|бутил}} |
|||
{{перевести|de|Butylgruppe}} |
|||
{{Углеводородные радикалы}} |
|||
[[Категория:Алкилы]] |
|||
Текущая версия от 14:05, 21 апреля 2024
Бутил — одновалентный радикал бутана, или заместитель с формулой −С4Н9, производное бутана или изобутана (С4Н10). Часто встречается в качестве заместителя в органических веществах.
н-Бутан может быть замещён как в оба терминальных атома, так и в два центральных.
Нормальный, или н-бутил: CH3−CH2−CH2−CH2− (систематическое название: бутил)
Вторичный бутил, или втор-бутил: CH3−CH2−CH(CH3)− (систематическое название: 1-метилпропил)
Другой разветвлённый изомер бутана — изобутан, может быть замещённым по трём терминальным атомам или по центральному
Изобутил: (CH3)2CH−CH2− (систематическое название: 2-метилпропил)
Третичный бутил, трет-бутил: (CH3)3C− (систематическое название: 1,1-диметилэтил)
Номенклатура
[править | править код]Согласно номенклатуре ИЮПАК, обозначения «изобутил», «втор-бутил», и «трет-бутил» могут использоваться в качестве тривиальных.
| Структурная формула | Устоявшееся название | Номенклатура ИЮПАК | Систематическое имя | Альтернативные названия |
|---|---|---|---|---|
| н-бутил | бутил | бутил | бутан-1-ил | |
| изобутил | изобутил | 2-метилпропил | 2-метилпропан-1-ил | |

|
втор-бутил | втор-бутил | 1-метилпропил | бутан-2-ил |

|
трет-бутил | трет-бутил | 1,1-диметилэтил | 2-метилпропан-2- |
Бутил — самый большой алкильный заместитель, имеющий тривиальное название. Префикс изо-, втор- и трет- обозначают количество разветвлений цепи (также известен как RI). Изо — означает — одно, втор- два и трет- три.
Примеры
[править | править код]Ниже представлены варианты бутильных заместителей на примере изомеров «бутил ацетата»
|
|
|
|
Этимология
[править | править код]С ростом количества атомов углерода радикал бутил стал последним названым исторически, а не с использованием греческого счёта. Название «бутил» происходит от английского названия масляной кислоты (англ. butyric acid), которая так названа оттого, что она содержится в прогорклом масле (англ. butter, которое, в свою очередь, восходит к лат. butyrum — масло).
Стерические свойства
[править | править код]С увеличивающейся разветвлённости проявляются стрерические требование бутильной группы. Трет-бутил группа создаёт стерическое напряжение вокруг себя. Это может стабилизировать вещество благодаря блокировке реакционного центра, что соответственно меняет кинетику реакции: ускорять или замедлять реакцию. В большинстве случаев происходит торможение из-за стерического отталкивания фрагентов молекулы. Ускорение происходит, когда трет-бутил фиксирует необходимую для протекания реакции конформацию.
Якорная группа
[править | править код]Изобутил также как и трет-бутилгруппа способна применяться как якорная группа. Это означает, что благодаря своему стерическому эффекту изменяет предпочтения конформаций в молекуле. Так для примера отталкивание свободных алкильных групп затрудняется либо предотвращается переход из одной конформацию циклогексанового кольца в другую. Громоздкий трет-бутильный остаток остаётся предпочтительно в экваториальном положении, так как при этом уменьшается взаимодействия с другими заместителями в циклогексановом кольце. Во-вторых, возможная конформация кресла с остатком аксиальном положении, вследствие проявляется отталкивания с другими аксиальными группами. Это энергетически неблагоприятно, и равновесие смещено в сторону занятия трет-бутильной группы экваториальной конформации.
Трет-бутиловый эффект
[править | править код]Трет-бутильный заместитель стерически очень требователен и используется в химии кинетической стабилизации вместе с другими объёмными группами, такими как триметилсилильная группа. Эффект, который проявляет трет-бутильная группа воздействуя на прогресс химической реакции называют трет-бутиловый эффект.
Этот эффект иллюстрируется в реакции Дильса-Альдера ниже, где трет-бутильный заместитель изменяет коэффициент скорости реакции более чем в 240 раз по сравнению с водородом как заместителя[1].
Электроноакцепторные свойства
[править | править код]Благодаря различным позициям, которыми бутильные группы могут соединяться с остальной молекулой, он проявляет различные электроакцепторные свойства. Так между изомерами бутильного остатка электронная плотность у третичного атома углерода трет-бутилгруппы наибольшая, а у н-бутила наиболее низкая. Это отражается в повышении основных свойств литированных веществ от н-бутиллития, через втор-бутиллитий к трет-бутиллитию. Подобный эффект увеличения основности существует и в ряду 1-бутанол, 2-бутанол, трет-бутанол.
Применение
[править | править код]
Алкиллитий сильное металлорганическое основание. Он может депротонировать очень слабые кислоты, ровно как и литировать вещества. Коммерчески доступны три основания бутиллития, как стандартные реактивы: н-бутиллитий, втор-бутиллитий и трет-бутиллитий.
Гидрирующий агент диизобутилалюминий гидрид содержит два изобутильных остатка.
Примечания
[править | править код]- ↑ Factors affecting ease of ring formation. The effect of anchoring substitution on the rate of an intramolecular diels-alder reaction with furan-diene Serge Cauwberghs and Pierre J. De Clercq B. Tinant and J. P. Declercq Tetrahedron Letters Volume 29, Issue 20 , 1988, Pages 2493—2496 doi:10.1016/S0040-4039(00)87916-2.
Ссылки
[править | править код]В другом языковом разделе есть более полная статья Butylgruppe (нем.). |