Фотосистема I: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
Эрг (обсуждение | вклад) |
м Удаление шаблонов: {{Нп3}}×2 |
||
| (не показано 30 промежуточных версий 17 участников) | |||
| Строка 1: | Строка 1: | ||
{{другие значения|Фотосистема |
{{другие значения|Фотосистема}} |
||
[[Файл: |
[[Файл:PSI.png|thumb|upright=2|Структурно-функциональная организация комплекса ФСI (ССКI не показаны): P700 (П<sub>700</sub>) — специальная пара; А<sub>0</sub> — хлорофилл а<sub>695</sub>; A<sub>1</sub> — филлохинон; F<sub>x</sub>, F<sub>a</sub>,F<sub>b</sub> — железосерные кластеры (на рисунке не показана пара дополнительных хлорофиллов а).]] |
||
'''Фотосисте́ма I''' (''первая фотосистема'', ''фотосистема один'', ФСI), или '''пластоциани́н-ферредокси́н-оксидоредукта́за''' — второй функциональный комплекс электрон-транспортной цепи ([[Электронотранспортная цепь фотосинтеза|ЭТЦ]]) [[хлоропласт]]ов. Он принимает [[электрон]] от [[пластоцианин]]а и, поглощая [[Световая энергия|световую энергию]], формирует сильный восстановитель П<sub>700</sub>, способный через цепь переносчиков электронов осуществить [[Восстановление (химия)|восстановление]] [[НАДФ|НАДФ<sup>+</sup>]]. Таким образом, при участии ФСI синтезируется источник электронов ([[НАДФН]]) для последующих реакций восстановления [[углерод]]а в хлоропластах в [[Цикл Кальвина|цикле Кальвина]]. Кроме того, ФСI может осуществлять циклический транспорт электронов, сопряжённый с синтезом [[АТФ]], обеспечивая дополнительный синтез АТФ в [[хлоропласт]]ах{{sfn|Ермаков|2005|с=173-175}}. |
'''Фотосисте́ма I''' (''первая фотосистема'', ''фотосистема один'', ФСI), или '''пластоциани́н-ферредокси́н-оксидоредукта́за''' — второй функциональный комплекс электрон-транспортной цепи ([[Электронотранспортная цепь фотосинтеза|ЭТЦ]]) [[хлоропласт]]ов. Он принимает [[электрон]] от [[пластоцианин]]а и, поглощая [[Световая энергия|световую энергию]], формирует сильный восстановитель П<sub>700</sub>, способный через цепь переносчиков электронов осуществить [[Восстановление (химия)|восстановление]] [[НАДФ|НАДФ<sup>+</sup>]]. Таким образом, при участии ФСI синтезируется источник электронов ([[НАДФН]]) для последующих реакций восстановления [[углерод]]а в хлоропластах в [[Цикл Кальвина|цикле Кальвина]]. Кроме того, ФСI может осуществлять циклический транспорт электронов, сопряжённый с синтезом [[АТФ]], обеспечивая дополнительный синтез АТФ в [[хлоропласт]]ах{{sfn|Ермаков|2005|с=173-175}}. |
||
| Строка 6: | Строка 6: | ||
Нециклический транспорт электронов начинается с того, что [[марганец|марганцевый]] кластер фотосистемы II [[Окисление|окисляет]] [[вода|воду]], восстанавливая пул [[пластохинон]]ов. Далее [[цитохром b6f-комплекс|цитохром ''b''<sub>6</sub>''f''-комплекс]] окисляет пластохиноны, а электрон через [[пластоцианин]] передаётся на фотосистему I, где используется для синтеза [[НАДФН]]. Нарушение формальной логики в названиях фотосистем связано с тем, что фотосистема I была открыта раньше, чем [[фотосистема II]]. |
Нециклический транспорт электронов начинается с того, что [[марганец|марганцевый]] кластер фотосистемы II [[Окисление|окисляет]] [[вода|воду]], восстанавливая пул [[пластохинон]]ов. Далее [[цитохром b6f-комплекс|цитохром ''b''<sub>6</sub>''f''-комплекс]] окисляет пластохиноны, а электрон через [[пластоцианин]] передаётся на фотосистему I, где используется для синтеза [[НАДФН]]. Нарушение формальной логики в названиях фотосистем связано с тем, что фотосистема I была открыта раньше, чем [[фотосистема II]]. |
||
Первые данные указывающие на существование ФСI появились в 1950-х годах, но в то время никто ещё не мог оценить значимость этих открытий<ref name="Fromme">{{ |
Первые данные указывающие на существование ФСI появились в 1950-х годах, но в то время никто ещё не мог оценить значимость этих открытий<ref name="Fromme">{{статья |заглавие=Unraveling the photosystem I reaction center: a history, or the sum of many efforts |издание={{Нп3|Drugs (журнал)|Drugs||Drugs (journal)}} |том=80 |номер=1—3 |ссылка=http://research.eeescience.utoledo.edu/lees/papers_PDF/Fromme_2004.pdf |страницы=109—124 |pmid=16328814 |doi=10.1023/B:PRES.0000030657.88242.e1 |accessdate=2015-01-31 |archiveurl=https://web.archive.org/web/20151222094148/http://research.eeescience.utoledo.edu/lees/papers_PDF/Fromme_2004.pdf |archivedate=2015-12-22 |deadlink=yes |язык=en |тип=journal |автор=Fromme P., Mathis P. |год=2004 |издательство=[[Springer Nature|Adis International]] }}</ref>. Представление о существовании в [[хлоропласт]]ах двух фотосистем возникло в уже в 1940-е годы на основание опытов лаборатории [[Роберт Эмерсон|Р. Эмерсона]], обнаружившего эффект падения [[Люминесценция#Выход люминесценции|квантового выхода]] [[фотосинтез]]а при освещении хлоропластов [[Монохроматическое излучение|монохроматическим]] красным светом (λ>680 нм), возбуждающим только ФСI, и эффект усиления [[Люминесценция#Выход люминесценции|квантового выхода]] при добавлении подсветки с длиной волны около 650 нм, которая возбуждала [[ФСII]] (так называемый ''[[эффект Эмерсона]]''). Также следует упомянуть открытый Комоннером в 1956 году светоиндуцируемый [[Электронный парамагнитный резонанс|ЭПР]] сигнал, который был назван сигналом I. По чистой случайности сигнал I и сигнал II, исходили от ФСI и ФСII соответственно<ref name="Fromme"/>. Лишь в 1960 году Луис Дюйзенс предложил концепцию фотосистемы I и фотосистемы II, и в том же году Фэй Бендалл и [[Хилл, Роберт (биохимик)|Роберт Хилл]] организовали результаты предыдущих открытий в стройную теорию последовательных реакций [[фотосинтез]]а<ref name="Fromme"/>. Гипотеза Хилла и Бендалля была позднее подтверждена в экспериментах Дюйзенса и Витта в 1961 году<ref name="Fromme"/>. |
||
После этого начались систематические попытки физического выделения фотосистемы I, определения её трёхмерной структуры и тонкого строения. В 1966 году начался бум исследований в этой области: Андерсон и Бордман подвергали мембраны хлоропластов воздействию [[ультразвук]]а с последующей обработкой [[дигитонин]]ом, Вернон использовал [[тритон X-100]], а Огава — [[додецилсульфат]]. Однако, первые полученные экстракты содержали примеси светосособирающих комплексов, а также [[цитохром f|цитохромов f]] и b<sub>6</sub>. Потребовалось много времени |
После этого начались систематические попытки физического выделения фотосистемы I, определения её трёхмерной структуры и тонкого строения. В 1966 году начался бум исследований в этой области: Андерсон и Бордман подвергали мембраны хлоропластов воздействию [[ультразвук]]а с последующей обработкой [[дигитонин]]ом, Вернон использовал [[тритон X-100]], а Огава — [[додецилсульфат]]. Однако, первые полученные экстракты содержали примеси светосособирающих комплексов, а также [[цитохром f|цитохромов f]] и b<sub>6</sub>. Потребовалось много времени, чтобы разобраться, что полученные экстракты были смесью<ref name="Fromme"/>. |
||
В 1968 году Рид и Клайтон смогли выделить [[реакционный центр]] фотосистемы I из [[пурпурные бактерии|пурпурных бактерий]], что значительно подстегнуло исследования оксигенного фотосинтеза. Однако, открытым оставался вопрос: что из выделенного являлось истинным реакционным центром, что антенными комплексами, а что дополнительными субъединицами. Долгое время эффективное выделение реакционного центра фотосистемы I оставалось неразрешённой проблемой. В конце-концов оказалось, что легче всего это сделать у [[цианобактерии|цианобактерий]], поскольку у них отсутствовали интегрированные в мембрану внешние антенны. После многочисленных попыток с разными |
В 1968 году Рид и Клайтон смогли выделить [[реакционный центр]] фотосистемы I из [[пурпурные бактерии|пурпурных бактерий]], что значительно подстегнуло исследования оксигенного фотосинтеза. Однако, открытым оставался вопрос: что из выделенного являлось истинным реакционным центром, что антенными комплексами, а что дополнительными субъединицами. Долгое время эффективное выделение реакционного центра фотосистемы I оставалось неразрешённой проблемой. В конце-концов оказалось, что легче всего это сделать у [[цианобактерии|цианобактерий]], поскольку у них отсутствовали интегрированные в мембрану внешние антенны. После многочисленных попыток с разными видами, выяснилось, что самыми многообещающими в этом отношение видами являются представителями ''[[Synechocystis]]'' и ''[[Synechococcus]]'', поскольку фотосистема I, выделенная из ''[[Thermosynechococcus elongatus]]'' давала очень стабильный [[реакционный центр]], пригодный для кристаллизации и исследования методом [[Рентгеноструктурный анализ|рентгеноструктурного анализ]]<ref name="Fromme"/>. |
||
== Отличия от фотосистемы II == |
== Отличия от фотосистемы II == |
||
| ⚫ | Основная функция [[фотосистема II|фотосистемы II]] — генерация сильного окислителя, который инициирует окисление воды и передачу её электронов на мембранный переносчик. Основная функция фотосистемы I — насытить эти низкоуровневые [[электрон]]ы энергией, чтобы с их помощью осуществить восстановление [[Никотинамидадениндинуклеотидфосфат|НАДФ]]<sup>+</sup>. Поскольку энергия суммарного процесса слишком велика, чтобы осуществить его в рамках одного [[Реакционный центр|реакционного центра]], в ходе эволюции появились две фотосистемы, которые раздельно осуществляют разные части этой реакции. Их специфические функции и определяют особенности их строения. Так, фотосистема I — симметрична, то есть в ней работают две ветви электронного транспорта, что делает его значительно более быстрым, в то время как фотосистема II — асимметрична и обладает только одной рабочей ветвью, что замедляет транспорт электронов, но делает его более управляемым. Обе фотосистемы значительно отличаются по строению антенн, дополнительных субъединиц, способов регуляции и своему положению в мембране{{sfn|Ермаков|2005|с=121}}. Так, фотосистема I обладает интегральной антенной, хлорофиллы которой расположены непосредственно на главных белках комплекса — А и B, в то время как у фотосистемы II они вынесены на внешние белки CP47 и CP43. По количеству дополнительных малых регуляторных субъединиц ФС II значительно превосходит ФС I, что связано с необходимостью тонкой регуляции процесса окисления воды, который потенциально крайне опасен для клетки. Этим же объясняется неоднородное распределение фотосистем в мембране [[тилакоид]]а: в то время как ФС I располагается преимущественно в области маргинальных, торцевых и стромальных мембран, ФС II практически полностью находится в области спаренных мембран, что обеспечивает клетке дополнительную защиту от продуцируемых ею [[Активные формы кислорода|активных форм кислорода]]<ref name="Dimeric and Monomeric">{{статья |заглавие=Dimeric and Monomeric Organization of Photosystem II |издание=[[Journal of Biological Chemistry|The Journal of Biological Chemistry]] |номер=281 |страницы=14241—14249 |doi=10.1074/jbc.M600634200 |язык=en |тип=journal |автор=Ravi Danielsson, Marjaana Suorsa, Virpi Paakkarinen, Per-Åke Albertsson, Stenbjörn Styring, Eva-Mari Aro and Fikret Mamedov |месяц=5 |год=2006}}</ref>. |
||
Основная |
|||
функция [[фотосистема II|фотосистемы II]] — генерация сильного окислителя, который |
|||
инициирует окисление воды и передачу её электронов на мембранный |
|||
переносчик. Основная функция фотосистемы I — насытить эти низкоуровневые |
|||
[[электрон]]ы энергией, что бы с их помощью осуществить восстановление [[Никотинамидадениндинуклеотидфосфат|НАДФ]]<sup>+</sup>. Поскольку энергия суммарного процесса слишком велика, что бы осуществить его в рамках одного [[Реакционный центр|реакционного центра]], |
|||
в ходе эволюции появились две фотосистемы, которые раздельно |
|||
осуществляют разные части этой реакции. Их специфические функции и |
|||
определяют особенности их строения. Так, фотосистема I — симметрична, то |
|||
есть в ней работают две ветви электронного транспорта, что делает его |
|||
значительно более быстрым, в то время как фотосистема II — асимметрична и |
|||
| ⚫ | обладает только одной рабочей ветвью, что замедляет транспорт электронов, но делает его более управляемым. Обе фотосистемы значительно отличаются по строению антенн, дополнительных субъединиц, способов регуляции и своему положению в мембране{{sfn|Ермаков|2005|с=121}}. Так, фотосистема I обладает интегральной антенной, хлорофиллы которой расположены непосредственно на главных белках комплекса — А и B, в то время как у фотосистемы II они вынесены на внешние белки CP47 и CP43. По количеству дополнительных малых регуляторных субъединиц ФС II значительно превосходит ФС I, что связано с необходимостью тонкой регуляции процесса окисления воды, который потенциально крайне опасен для клетки. Этим же объясняется |
||
Главное отличие фотосистемы II от фотосистемы I — это наличие большого обращённого в люмен домена, который содержит марганцевый кластер и окружающие его защитные белки. Именно здесь происходит процесс фотохимического окисления воды, сопровождаемый выделением [[кислород]]а и протонов{{sfn|Ермаков|2005|с=121}}. |
Главное отличие фотосистемы II от фотосистемы I — это наличие большого обращённого в люмен домена, который содержит марганцевый кластер и окружающие его защитные белки. Именно здесь происходит процесс фотохимического окисления воды, сопровождаемый выделением [[кислород]]а и протонов{{sfn|Ермаков|2005|с=121}}. |
||
| Строка 57: | Строка 47: | ||
| CDD = |
| CDD = |
||
}} |
}} |
||
Фотосистема I состоит из следующих [[Белковая субъединица|белковых субъединиц]] и [[кофактор]]ов<ref>{{ |
Фотосистема I состоит из следующих [[Белковая субъединица|белковых субъединиц]] и [[кофактор]]ов<ref>{{статья |doi=10.1016/S0959-440X(02)00317-2 |заглавие=The assembly of protein subunits and cofactors in photosystem I |издание=Curr. Opin. Struct. Biol. |том=12 |номер=2 |страницы=244—254 |pmid=11959504 |ссылка=http://linkinghub.elsevier.com/retrieve/pii/S0959440X02003172 |язык=en |тип=journal |автор=Saenger W., Jordan P., Krauss N. |месяц=4 |год=2002 |archivedate=2018-11-04 |archiveurl=https://web.archive.org/web/20181104170034/https://linkinghub.elsevier.com/retrieve/pii/S0959440X02003172 }}</ref>{{sfn|Страсбургер|2008|с=117}}{{sfn|Ермаков|2005|с=173-175}}: |
||
{| class="wikitable" |
{| class="wikitable" |
||
|- |
|- |
||
| Строка 134: | Строка 124: | ||
|- |
|- |
||
| row 15, cell 1|F<sub>a</sub> |
| row 15, cell 1|F<sub>a</sub> |
||
| row 15, cell 2|Fe<sub>4</sub>S< |
| row 15, cell 2|Fe<sub>4</sub>S<sub>4</sub> [[Железосерные кластеры|железосерный кластер]] (ЭТЦ) |
||
|- |
|- |
||
| row 16, cell 1|F<sub>b</sub> |
| row 16, cell 1|F<sub>b</sub> |
||
| row 16, cell 2|Fe<sub>4</sub>S< |
| row 16, cell 2|Fe<sub>4</sub>S<sub>4</sub> железосерный кластер (ЭТЦ) |
||
|- |
|- |
||
| row 17, cell 1|F<sub>x</sub> |
| row 17, cell 1|F<sub>x</sub> |
||
| row 17, cell 2|Fe<sub>4</sub>S< |
| row 17, cell 2|Fe<sub>4</sub>S<sub>4</sub> железосерный кластер (ЭТЦ) |
||
|- |
|- |
||
| row 18, cell 1|[[Ферредоксин]] |
| row 18, cell 1|[[Ферредоксин]] |
||
| Строка 160: | Строка 150: | ||
| row 34, cell 2|ион [[магний|магния]] |
| row 34, cell 2|ион [[магний|магния]] |
||
|} |
|} |
||
Основная функция ФСI — передача энергии света на электрон, перенос электрона от пластоцианина к ферредоксину<ref name="pmid3333014">{{ |
Основная функция ФСI — передача энергии света на электрон, перенос электрона от пластоцианина к ферредоксину<ref name="pmid3333014">{{статья |заглавие=Structure, function and organization of the Photosystem I reaction center complex |издание={{Нп3|Biochimica et Biophysica Acta|Biochim. Biophys. Acta||Biochimica et Biophysica Acta}} |том=895 |номер=3 |страницы=167—204 |pmid=3333014 |doi=10.1016/s0304-4173(87)80002-2 |язык=en |тип=journal |автор=Golbeck J.H. |год=1987}}</ref>. ФСI содержит свыше 110 [[кофактор]]ов, значительно больше чем [[фотосистема II]]<ref name="bukman">{{статья |заглавие=Structure and funcnions of photosystems I and II |ссылка=http://science.energy.gov/~/media/bes/csgb/pdf/docs/solar_photochemistry_2004.pdf |язык=und |автор=HongQi Yu', Ingo Gortjohann, Yana Bukman, Craig Yolley', Devendra K. Chauhan, Alexander Melkozerov and Petra Fromme |издание= |archivedate=2017-01-01 |archiveurl=https://web.archive.org/web/20170101031106/http://science.energy.gov/~/media/bes/csgb/pdf/docs/Solar_photochemistry_2004.pdf }}</ref>. Каждый из этих компонентов имеет широкий спектр функций. |
||
Основные компоненты электрон-транспортной цепи ФСI — главный донор возбуждённых электронов П<sub>700</sub> (хлорофильный [[димер]]) и пять переносчиков: A<sub>0</sub> ([[хлорофилл а]]), A<sub>1</sub> ([[филлохинон]]) и три Fe<sub>4</sub>S<sub>4</sub> железосерных кластера: F<sub>x</sub>, F<sub>a</sub>, и F<sub>b</sub><ref>{{ |
Основные компоненты электрон-транспортной цепи ФСI — главный донор возбуждённых электронов П<sub>700</sub> (хлорофильный [[димер]]) и пять переносчиков: A<sub>0</sub> ([[хлорофилл а]]), A<sub>1</sub> ([[филлохинон]]) и три Fe<sub>4</sub>S<sub>4</sub> железосерных кластера: F<sub>x</sub>, F<sub>a</sub>, и F<sub>b</sub><ref>{{статья |заглавие=Photosynthesis:Microbial |издание=Encyclopedia of Microbiology, 3rd Ed |страницы=325—341 |doi=10.1016/B978-012373944-5.00352-7 |язык=en |автор=Jagannathan, Bharat; Golbeck, John |год=2009 |тип=book }}</ref>. |
||
Структурно ФСI представляет собой гетеродимер двух [[Интегральный мембранный белок|интегральных белковых комплексов]] — А и В (у всех растений кодируются [[пластом|хлоропластными]] генами ''PsaA'' и ''PsaB''). Белки А и В присоединяют димер Р700, по одной молекуле [[мономер]]а хлорофилла а (Хл<sub>695</sub>) — первичного акцептора электронов А<sub>0</sub>, по одному дополнительному хлорофиллу а и по одной молекуле [[филлохинон]]а (А<sub>1</sub>). Два набора дополнительных хлорофиллов а, первичных акцепторов электрона и филлохинонов формируют две почти симметричные ветви транспорта электронов от Р700 к F<sub>x</sub>. В отличие от [[реакционный центр|реакционных центров]] [[зелёные серобактерии|зелёных]] и [[пурпурные бактерии|пурпурных]] бактерий и ФСII, где из двух ветвей функционирует лишь одна, в ФСI активны обе ветви электронного транспорта, хотя они и не идентичны{{sfn|Ермаков|2005|с=173-175}}.Белок А гомологичен белкам D<sub>1</sub>+СP43 (молекулярная масса белка А соответствует сумме молекулярных масс белков D<sub>1</sub> и СP43) из фотосистемы II, а белок В гомологичен белкам D<sub>2</sub>+CP47 соответственно{{sfn|Хелдт|2011|с = 99}}. |
Структурно ФСI представляет собой гетеродимер двух [[Интегральный мембранный белок|интегральных белковых комплексов]] — А и В (у всех растений кодируются [[пластом|хлоропластными]] генами ''PsaA'' и ''PsaB''). Белки А и В присоединяют димер Р700, по одной молекуле [[мономер]]а хлорофилла а (Хл<sub>695</sub>) — первичного акцептора электронов А<sub>0</sub>, по одному дополнительному хлорофиллу а и по одной молекуле [[филлохинон]]а (А<sub>1</sub>). Два набора дополнительных хлорофиллов а, первичных акцепторов электрона и филлохинонов формируют две почти симметричные ветви транспорта электронов от Р700 к F<sub>x</sub>. В отличие от [[реакционный центр|реакционных центров]] [[зелёные серобактерии|зелёных]] и [[пурпурные бактерии|пурпурных]] бактерий и ФСII, где из двух ветвей функционирует лишь одна, в ФСI активны обе ветви электронного транспорта, хотя они и не идентичны{{sfn|Ермаков|2005|с=173-175}}.Белок А гомологичен белкам D<sub>1</sub>+СP43 (молекулярная масса белка А соответствует сумме молекулярных масс белков D<sub>1</sub> и СP43) из фотосистемы II, а белок В гомологичен белкам D<sub>2</sub>+CP47 соответственно{{sfn|Хелдт|2011|с = 99}}. |
||
Обе субъединицы содержат 11 {{нп5|Трансмембранный домен|трансмембранных сегментов|en|Transmembrane domain}}. Железосодержащий кластер F<sub>x</sub> связан четырьмя [[цистеин]]ами, два из которых находятся на субъединице А, и ещё два на субъединице В. В обоих белках цистеины находятся на [[Проксимальный|проксимальном]] конце, в петле между девятым и десятым трансмембранными сегментами. По всей вероятности, ниже цистеинов находится так называемый [[Мотив (молекулярная биология)|мотив]] [[Лейциновая застёжка-молния|лейциновой молнии]], который вносит существенный вклад в [[Димеризация|димеризацию]] белков А и В<ref name="pmid2186925">{{ |
Обе субъединицы содержат 11 {{нп5|Трансмембранный домен|трансмембранных сегментов|en|Transmembrane domain}}. Железосодержащий кластер F<sub>x</sub> связан четырьмя [[цистеин]]ами, два из которых находятся на субъединице А, и ещё два на субъединице В. В обоих белках цистеины находятся на [[Проксимальный|проксимальном]] конце, в петле между девятым и десятым трансмембранными сегментами. По всей вероятности, ниже цистеинов находится так называемый [[Мотив (молекулярная биология)|мотив]] [[Лейциновая застёжка-молния|лейциновой молнии]], который вносит существенный вклад в [[Димеризация|димеризацию]] белков А и В<ref name="pmid2186925">{{статья |заглавие=Photosystem I reaction-centre proteins contain leucine zipper motifs. A proposed role in dimer formation |издание={{Нп3|FEBS Letters|FEBS Lett.||FEBS Letters}} |том=264 |номер=1 |страницы=1—4 |pmid=2186925 |doi=10.1016/0014-5793(90)80749-9 |язык=en |автор=Webber A.N., Malkin R. |месяц=5 |год=1990 |тип=journal}}</ref>. Конечные акцепторы электронов F<sub>A</sub> и F<sub>B</sub> находятся на субъединице С<ref>{{статья |заглавие=Breaking biological symmetry in membrane proteins: The asymmetrical orientation of PsaC on the pseudo-C2 symmetric Photosystem I core |издание=[[Cellular and Molecular Life Sciences|Cell. Mol. Life Sci.]] |том=66 |номер=7 |страницы=1257—1270 |doi=10.1007/s00018-009-8673-x |язык=en |тип=journal |автор=Jagannathan, Bharat; Golbeck, John |год=2009}}</ref><ref>{{статья |заглавие=Understanding of the Binding Interface between PsaC and the PsaA/PsaB Heterodimer in Photosystem I |издание=Biochemistry |том=48 |страницы=5405—5416 |doi=10.1021/bi900243f |язык=en |тип=journal |автор=Jagannathan, Bharat; Golbeck, John |год=2009}}</ref>. |
||
Следует особо подчеркнуть, что перенос электрона осуществляется в соответствии с [[Энергия Гиббса|термодинамическим потенциалом]]. Увеличение [[Окислительно-восстановительный потенциал|окислительно-восстановительных потенциалов]] в цепи акцепторов обеспечивает быстрое снижение энергии, что предотвращает возврат электрона к пигменту и бесполезную трату энергии электронного возбуждения. Благодаря этому [[энергия]] возбуждения эффективно используется для разделения [[Заряд (физика)|зарядов]]{{sfn|Ермаков|2005|с=157}}. |
Следует особо подчеркнуть, что перенос электрона осуществляется в соответствии с [[Энергия Гиббса|термодинамическим потенциалом]]. Увеличение [[Окислительно-восстановительный потенциал|окислительно-восстановительных потенциалов]] в цепи акцепторов обеспечивает быстрое снижение энергии, что предотвращает возврат электрона к пигменту и бесполезную трату энергии электронного возбуждения. Благодаря этому [[энергия]] возбуждения эффективно используется для разделения [[Заряд (физика)|зарядов]]{{sfn|Ермаков|2005|с=157}}. |
||
| Строка 171: | Строка 161: | ||
=== Пластоцианин === |
=== Пластоцианин === |
||
{{main|Пластоцианин}} |
{{main|Пластоцианин}} |
||
[[Файл:Plastocyanin-from-3BQV-3D-cartoon-balls.png|thumb|right|200px|Структура пластоцианина<ref>{{cite web|url=http://www.rcsb.org/pdb/explore.do?structureId=3BQV |title=PDB 3BQV}}</ref>]] |
[[Файл:Plastocyanin-from-3BQV-3D-cartoon-balls.png|thumb|right|200px|Структура пластоцианина<ref>{{cite web |url=http://www.rcsb.org/pdb/explore.do?structureId=3BQV |title=PDB 3BQV |access-date=2015-01-14 |archive-date=2017-02-24 |archive-url=https://web.archive.org/web/20170224054531/http://www.rcsb.org/pdb/explore.do?structureId=3BQV |deadlink=no }}</ref>]] |
||
Пластоцианин — маленький, подвижный белок с молекулярной массой около 10,5 кДа. К его центральному атому Сu присоединяются остатки [[цистеин]]а и [[метионин]]а, а сбоку его стабилизируют два остатка [[гистидин]]а. При обратимой смене валентности Cu<sup>2+</sup> ↔ Cu<sup>+1</sup> пластоцианин либо поглощает один электрон, либо отдаёт его. Пластоцианин является аналогом [[цитохром c|цитохрома c]], который выполняет схожую функцию в дыхательной цепи [[митохондрия|митохондрий]]{{sfn|Страсбургер|2008|с=117}}. |
Пластоцианин — маленький, подвижный белок с молекулярной массой около 10,5 кДа. К его центральному атому Сu присоединяются остатки [[цистеин]]а и [[метионин]]а, а сбоку его стабилизируют два остатка [[гистидин]]а. При обратимой смене валентности Cu<sup>2+</sup> ↔ Cu<sup>+1</sup> пластоцианин либо поглощает один электрон, либо отдаёт его. Пластоцианин является аналогом [[цитохром c|цитохрома c]], который выполняет схожую функцию в дыхательной цепи [[митохондрия|митохондрий]]{{sfn|Страсбургер|2008|с=117}}. |
||
Он принимает электрон от [[цитохром b6f-комплекс|цитохром ''b''<sub>6</sub>''f''-комплекса]], окисляя цитохром ''f'' и перенося его непосредственно на [[реакционный центр]] П<sub>700</sub> фотосистемы I. На внешней стороне белка имеется группа аминокислот, несущих отрицательный заряд<ref name = "Frazão">{{ |
Он принимает электрон от [[цитохром b6f-комплекс|цитохром ''b''<sub>6</sub>''f''-комплекса]], окисляя цитохром ''f'' и перенося его непосредственно на [[реакционный центр]] П<sub>700</sub> фотосистемы I. На внешней стороне белка имеется группа аминокислот, несущих отрицательный заряд<ref name = "Frazão">{{статья |doi=10.1007/s007750050299 |заглавие=Ab initio structure solution of a dimeric cytochrome c3 from ''Desulfovibrio gigas'' containing disulfide bridges |издание={{Нп3|Journal of Biological Inorganic Chemistry|J. Biol. Inorg. Chem.||Journal of Biological Inorganic Chemistry}} |том=4 |номер=2 |страницы=162—165 |pmid=10499086 |ссылка=http://link.springer.de/link/service/journals/00775/bibs/9004002/90040162.htm |accessdate=2015-01-14 |archiveurl=https://web.archive.org/web/20001015023537/http://link.springer.de/link/service/journals/00775/bibs/9004002/90040162.htm |archivedate=2000-10-15 |deadlink=yes |язык=en |тип=journal |автор=Frazão C., Sieker L., Sheldrick G., Lamzin V., LeGall J., Carrondo M.A. |месяц=4 |год=1999}}</ref>. Предположительно, они связываются с положительно заряженным люминальным доменом субъединицы F, однако механизм связывания недостаточно изучен и остаётся неясным<ref>{{статья |doi=10.1016/S0005-2728(99)00101-2 |заглавие=Electron transfers amongst cytochrome f, plastocyanin and photosystem I: kinetics and mechanisms |издание={{Нп3|Biochimica et Biophysica Acta|Biochim. Biophys. Acta||Biochimica et Biophysica Acta}} |том=1456 |номер=1 |страницы=5—26 |pmid=10611452 |ссылка=http://linkinghub.elsevier.com/retrieve/pii/S0005-2728(99)00101-2 |язык=en |тип=journal |автор=Hope A.B. |месяц=1 |год=2000 |archivedate=2017-08-30 |archiveurl=https://web.archive.org/web/20170830105947/http://linkinghub.elsevier.com/retrieve/pii/S0005-2728(99)00101-2 }}</ref>. |
||
У некоторых водорослей и [[Цианобактерии|цианобактерий]] при недостатке меди в среде пластоцианин не образуется, вместо него синтезируется и выполняет его функции [[цитохром c-553]]<ref>{{ |
У некоторых водорослей и [[Цианобактерии|цианобактерий]] при недостатке меди в среде пластоцианин не образуется, вместо него синтезируется и выполняет его функции [[цитохром c-553]]<ref>{{статья |заглавие=Copper-mediated regulation of cytochrome c553 and plastocyanin in the cyanobacterium Synechocystis 6803 |издание=[[Journal of Biological Chemistry|The journal of biological chemistry]] |том=267 |номер=27 |страницы=19054—19059 |pmid=1326543 |ссылка=http://www.jbc.org/content/267/27/19054.full.pdf |язык=en |тип=journal |автор=Zhang L1, McSpadden B., Pakrasi H.B., Whitmarsh J. |месяц=9 |год=1992 |archivedate=2017-09-09 |archiveurl=https://web.archive.org/web/20170909073732/http://www.jbc.org/content/267/27/19054.full.pdf }}</ref>. |
||
:* Пластоцианин (PC) отдаёт один электрон окисленному П<sub>700</sub><sup>+</sup> и восстанавливает его до исходного состояния: |
:* Пластоцианин (PC) отдаёт один электрон окисленному П<sub>700</sub><sup>+</sup> и восстанавливает его до исходного состояния: |
||
:: <math>\mathsf { P_{700}^+ + PC_{(Cu^{+1})} \rightarrow P_{700} + PC_{(Cu^{+2})}}</math> |
:: <math>\mathsf { P_{700}^+ + PC_{(Cu^{+1})} \rightarrow P_{700} + PC_{(Cu^{+2})}}</math> |
||
=== Специальная пара П<sub>700</sub> === |
=== Специальная пара П<sub>700</sub> === |
||
| ⚫ | П<sub>700</sub> (в [[Английский язык|английской]] литературе P700) представляет собой [[димер]] хлорофилла а и хлорофилла а‘ у которого кетоэфирная группа в V кольце находится в ''[[Цис-изомер|цис]]''-положении относительно плоскости молекулы, с максимумом поглощения 700 [[нм]]<ref name="rutherford">{{статья |doi=10.1007/BF00054105 |заглавие=Primary Photochemistry in Photosystem-I |издание={{Нп3|Drugs (журнал)|Drugs||Drugs (journal)}} |том=6 |номер=4 |страницы=295—316 |язык=en |автор=Rutherford A.W., Heathcote P. |год=1985 |издательство=[[Springer Nature|Adis International]] }}</ref>. Наличие ''цис''-кетоэфирной группы делает возможным образование димера из двух хлорофиллов посредством формирования [[Водородная связь|водородных связей]]. [[П700|П<sub>700</sub>]] получает энергию от антенных комплексов и использует её, чтобы поднять электроны на более высокий уровень. Далее электрон в ходе [[Окислительно-восстановительные реакции|окислительно-восстановительной реакции]] переходит на цепь переносчиков. В окисленном состоянии окислительно-восстановительный редокс-потенциал П<sub>700</sub> составляет +0,52 [[вольт|В]], а в фотовозбуждённом состоянии он становится −1,2 [[вольт|В]], то есть формируется мощный восстановитель, обеспечивающий восстановление НАДФ<sup>+</sup><ref name="Taiz"/><ref name="Shubin">{{статья |doi=10.1007/BF00029726 |заглавие=Molecular Arrangement of Pigment-Protein Complex of Photosystem I |издание={{Нп3|Drugs (журнал)|Drugs||Drugs (journal)}} |том=9 |номер=1—2 |страницы=3—12 |язык=en |тип=journal |автор=Shubin V.V., Karapetyan N.V., Krasnovsky A.A. |год=1986 |издательство=[[Springer Nature|Adis International]] }}</ref>. |
||
[[Файл:PSItransfersystem.png|thumb|250 px|Организация редокс-кофакторов реакционного центра ФСI. П<sub>700</sub> — димер хлорофиллов a и a‘,"специальная пара"; А — дополнительный хлорофилл а; А<sub>0</sub>-хлорофилл а<sub>695</sub>-первичный акцептор электронов; А<sub>1</sub>-витамин К<sub>1</sub>, филлохинон; F<sub>x</sub>, F<sub>a</sub>, F<sub>b</sub> — железосерные кластеры. Цифры на стрелках — расстояния между кофакторами]] |
|||
| ⚫ | П<sub>700</sub> (в [[Английский язык|английской]] литературе P700) представляет собой [[димер]] хлорофилла а и хлорофилла а‘ у которого кетоэфирная группа в V кольце находится в ''[[Цис-изомер|цис]]''-положении относительно плоскости молекулы, с максимумом поглощения 700 [[нм]]<ref name="rutherford">{{ |
||
:* В соответствии со следующим уравнением П<sub>700</sub> поглощает квант света и переходит в фотовозбуждённое состояние, в результате чего один из его электронов переходит с основного подуровня S<sub>0</sub> на первый [[синглетное состояние|синглетный]] подуровень S<sub>1</sub>: |
:* В соответствии со следующим уравнением П<sub>700</sub> поглощает квант света и переходит в фотовозбуждённое состояние, в результате чего один из его электронов переходит с основного подуровня S<sub>0</sub> на первый [[синглетное состояние|синглетный]] подуровень S<sub>1</sub>: |
||
:: <math>\mathsf { \mathit {h\nu} + P_{700} \rightarrow P_{700 \, _{S_{1}}}^* }</math> |
:: <math>\mathsf { \mathit {h\nu} + P_{700} \rightarrow P_{700 \, _{S_{1}}}^* }</math> |
||
| Строка 193: | Строка 181: | ||
=== Филлохинон A<sub>1</sub> === |
=== Филлохинон A<sub>1</sub> === |
||
Следующий акцептор — это [[Филлохинон]] A<sub>1</sub>, также известный как витамин [[Витамин K|K<sub>1</sub>]]. Он, как и хлорофилл, обладает [[фитол]]ьным хвостом<ref name="itoh">{{ |
Следующий акцептор — это [[Филлохинон]] A<sub>1</sub>, также известный как витамин [[Витамин K|K<sub>1</sub>]]. Он, как и хлорофилл, обладает [[фитол]]ьным хвостом<ref name="itoh">{{статья |doi=10.1016/0014-5793(89)81215-3 |заглавие=Vitamin K<sub>1</sub> (Phylloquinone) Restores the Turnover of FeS centers of Ether-extracted Spinach PS I Particles |издание={{Нп3|FEBS Letters|FEBS Lett.||FEBS Letters}} |том=243 |номер=1 |страницы=47—52 |язык=en |тип=journal |автор=Itoh, Shigeru, Msayo Iwaki |год=1989}}</ref>, и приблизительно соответствует [[пластохинон]]у Q<sub>A</sub> фотосистемы II. Поглощая электрон, он образует [[семихинон]]-[[Радикал (химия)|радикал]], который восстанавливает F<sub>x</sub>, передаёт его на F<sub>b</sub> и далее на F<sub>a</sub><ref name="itoh"/><ref>{{статья |doi=10.1016/0014-5793(87)80113-8 |заглавие=Is phylloquinone an obligate electron carrier in photosystem I? |издание={{Нп3|FEBS Letters|FEBS Lett.||FEBS Letters}} |том=215 |номер=1 |страницы=58—62 |pmid=3552735 |ссылка=http://linkinghub.elsevier.com/retrieve/pii/0014-5793(87)80113-8 |язык=en |тип=journal |автор=Palace G.P., Franke J.E., Warden J.T. |месяц=5 |год=1987 |archivedate=2019-05-04 |archiveurl=https://web.archive.org/web/20190504220316/https://linkinghub.elsevier.com/retrieve/pii/0014-5793(87)80113-8 }}</ref>. |
||
:: <math>\mathsf {A_0^- + A_1 \rightarrow A_0 + A_1\cdot}</math> |
:: <math>\mathsf {A_0^- + A_1 \rightarrow A_0 + A_1\cdot}</math> |
||
=== Железосерные кластеры === |
=== Железосерные кластеры === |
||
[[Железосерные кластеры]] ФСI имеют форму [[куб]]а с четырьмя атомами [[железо|железа]] и четырьмя атомами [[сера|серы]], составляющими его восемь вершин. Все три кластера связаны с белками ФСI через остатки цистеина<ref name="Vassiliev">{{ |
[[Железосерные кластеры]] ФСI имеют форму [[куб]]а с четырьмя атомами [[железо|железа]] и четырьмя атомами [[сера|серы]], составляющими его восемь вершин. Все три кластера связаны с белками ФСI через остатки цистеина<ref name="Vassiliev">{{статья |doi=10.1016/S0005-2728(01)00197-9 |заглавие=Iron-sulfur clusters in type I reaction centers |издание={{Нп3|Biochimica et Biophysica Acta|Biochim. Biophys. Acta||Biochimica et Biophysica Acta}} |том=1507 |номер=1—3 |страницы=139—160 |pmid=11687212 |ссылка=http://linkinghub.elsevier.com/retrieve/pii/S0005272801001979 |язык=en |автор=Vassiliev I.R., Antonkine M.L., Golbeck J.H. |месяц=10 |год=2001 |тип=journal |archivedate=2019-01-22 |archiveurl=https://web.archive.org/web/20190122044150/https://linkinghub.elsevier.com/retrieve/pii/S0005272801001979 }}</ref>. F<sub>x</sub> (E<sub>о</sub>‘ = −0,70 В) окисляет восстановленный А<sub>1</sub>. Дальнейший транспорт осуществляют железосерные кластеры F<sub>a</sub>, и F<sub>b</sub>, характеризующиеся низкими окислительно-восстановительными потенциалами (-0,59 и −0,55 В соответственно). |
||
Множество экспериментов выявило несоответствие между разными теориями, описывающими расположение и работу железосерных кластеров<ref name="Vassiliev"/>. Однако большинство результатов позволяет сделать некоторые общие выводы. Во-первых, F<sub>x</sub>, F<sub>a</sub>, и F<sub>b</sub> образуют [[треугольник]], и F<sub>a</sub> располагается ближе к F<sub>x</sub> чем F<sub>b</sub><ref name="Vassiliev"/>. Во-вторых, транспорт электронов начинается с F<sub>x</sub> через F<sub>a</sub> к F<sub>b</sub>, или же через F<sub>a</sub> к F<sub>b</sub>. До сих пор ведутся споры о том, какой из двух кластеров осуществляет перенос электрона на ферредоксин<ref name="Vassiliev"/>. |
Множество экспериментов выявило несоответствие между разными теориями, описывающими расположение и работу железосерных кластеров<ref name="Vassiliev"/>. Однако большинство результатов позволяет сделать некоторые общие выводы. Во-первых, F<sub>x</sub>, F<sub>a</sub>, и F<sub>b</sub> образуют [[треугольник]], и F<sub>a</sub> располагается ближе к F<sub>x</sub> чем F<sub>b</sub><ref name="Vassiliev"/>. Во-вторых, транспорт электронов начинается с F<sub>x</sub> через F<sub>a</sub> к F<sub>b</sub>, или же через F<sub>a</sub> к F<sub>b</sub>. До сих пор ведутся споры о том, какой из двух кластеров осуществляет перенос электрона на ферредоксин<ref name="Vassiliev"/>. |
||
=== Ферредоксин === |
=== Ферредоксин === |
||
{{main|Ферредоксин}} |
{{main|Ферредоксин}} |
||
Ферредоксин — это водорастворимый белок с молекулярной массой 11 кДа и содержащий Fe<sub>2</sub>S<sub>2</sub> центр<ref name="Forti">{{ |
Ферредоксин — это водорастворимый белок с молекулярной массой 11 кДа и содержащий Fe<sub>2</sub>S<sub>2</sub> центр<ref name="Forti">{{статья |doi=10.1016/0014-5793(85)80698-0 |заглавие=Two Sites of Interaction of Ferredoxin with thylakoids |издание={{Нп3|FEBS Letters|FEBS Lett.||FEBS Letters}} |том=186 |номер=2 |страницы=149—152 |язык=en |тип=journal |автор=Forti, Georgio, Paola Maria Giovanna Grubas |год=1985}}</ref>. Примечательно, что он является одноэлектронной окислительно-восстановительной системой, то есть переносит только один электрон, полученный им от железосерных кластеров. Он восстанавливается ФСI на стромальной стороне мембраны и в восстановленном состоянии является сильным восстановителем (E<sub>o</sub>‘ = —0,6 В), благодаря чему может быть переносчиком электронов для различных реакций, протекающих в хлоропласте. Так, ферредоксин поставляет электроны для восстановления [[нитриты|нитритов]], ([[нитритредуктаза]]) и ассимиляции [[сера|серы]] ([[сульфитредуктаза]]) в хлоропласте. Также он поставляет электроны для фиксации атмосферного [[азот]]а ([[нитрогеназа]]) у [[бактерии|бактерий]]. Он восстанавливает [[тиоредоксин]] — низкомолекулярный серосодержащий белок, участвующий в редокс-регуляции хлоропластов, активируя ключевые [[фермент]]ы цикла Кальвина. При нециклическом транспорте электронов ферредоксин взаимодействует с [[Ферредоксин—НАДФ(+) редуктаза|ферредоксин-НАДФ(+) редуктазой]], которая восстанавливает НАДФ<sup>+</sup> до НАДФН (E<sub>o</sub>‘ = −0,32 В) в строме хлоропласта<ref name="Forti"/>. |
||
== Светособирающий комплекс == |
== Светособирающий комплекс == |
||
{{main|Светособирающие комплексы}} |
{{main|Светособирающие комплексы}} |
||
[[Файл:PSI+LHC.png|thumb|left|160 px|ФСI и ССКI]] |
[[Файл:PSI+LHC.png|thumb|left|160 px|ФСI и ССКI]] |
||
Светособирающие комплексы состоят из молекул [[хлорофилл а|хлорофилла а]] и [[хлорофилл b|b]] и [[каротиноид]]ов, соединённых с белками<ref name="Taiz">{{ |
Светособирающие комплексы состоят из молекул [[хлорофилл а|хлорофилла а]] и [[хлорофилл b|b]] и [[каротиноид]]ов, соединённых с белками<ref name="Taiz">{{книга |часть=Ch. 7: Topic 7.8: Photosystem I |ссылка часть=http://4e.plantphys.net/article.php?ch=3&id=73 |заглавие=Plant physiology |издательство={{Нп3|Sinauer Associates}} |место=Sunderland, Mass |год=2006 |isbn=0-87893-856-7 |издание=4th |язык=und |автор=Zeiger, Eduardo; Taiz, Lincoln}} |
||
</ref>. Эти пигменты, возбуждаясь, переносят энергию [[фотон]]ов в [[реакционный центр]] фотосистемы [[Фёрстеровский перенос |
</ref>. Эти пигменты, возбуждаясь, переносят энергию [[фотон]]ов в [[реакционный центр]] фотосистемы [[Фёрстеровский перенос энергии|по Фёрстеровскому механизму]]. В отличие от реакционного центра ФСI, светособирающие комплексы могут поглощать практически во всей области [[видимый спектр|видимого спектра]]<ref name="kent">«The Photosynthetic Process» {{cite web |url=http://kentsimmons.uwinnipeg.ca/cm1504/lightreact.htm |title=Архивированная копия |accessdate=2009-05-05 |archiveurl=https://web.archive.org/web/20090219143934/http://kentsimmons.uwinnipeg.ca/cm1504/lightreact.htm |archivedate=2009-02-19 }}</ref>. Антенные комплексы подразделяют на внутренние, или интегральные, антенны, непосредственно присоединённые к комплексу фотосистемы, и периферические подвижные светособирающие комплексы (ССКI). Так, белки А и В присоединяют [[пигмент]]ы внутренней антенны ФСI: около 95 молекул хлорофилла а и 22 молекулы β-каротина, 5 из которых находятся в ''цис''-конформации. В координации по крайней мере десяти хлорофиллов внутренней антенны принимают участие малые субъединицы J, K, L, M и X. Пигменты внутренней антенны располагаются в виде цилиндра, окружающего все компоненты электрон-транспортной цепи фотосистемы I. Это отличает ФСI от ФСII, где пигменты внутренней антенны расположены на отдельных белках CP43 и CP77{{sfn|Ермаков|2005|с=173-175}}. Внешний светособирающий комплекс ССКI (LHCI) содержит 80—120 молекул хлорофиллов а и b, каротиноиды и состоит из четырёх субъединиц: Lhca1, Lhca2, Lhca3 и Lhca4 — с молекулярными массами 17—24 кДа. Относительно недавно были открыты две дополнительные субъединицы, Lhca5 и Lhca6, однако их концентрация в [[Биологические мембраны|мембране]] [[тилакоид]]а крайне мала, а кодирующие их [[ген]]ы практически не [[Экспрессия генов|экспрессируются]]<ref>{{статья |doi=10.1016/j.febslet.2006.10.063 |заглавие=Lhca5 interaction with plant photosystem I |издание={{Нп3|FEBS Letters|FEBS letters||FEBS Letters}} |том=580 |номер=27 |страницы=6485—6488 |ссылка=http://www.sciencedirect.com/science/article/pii/S0014579306012920 |язык=en |автор=Robert Lucinski, Volkmar H.R. Schmid, Stefan Jansson, Frank Klimmek |год=2006 |тип=journal |archivedate=2015-09-24 |archiveurl=https://web.archive.org/web/20150924152632/http://www.sciencedirect.com/science/article/pii/S0014579306012920 }}</ref><ref name="NADP" />. |
||
== Циклический транспорт электронов == |
== Циклический транспорт электронов == |
||
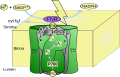
[[Файл:Thylakoid membrane 2.svg|thumb|320px|right|Нециклический транспорт электронов]] |
[[Файл:Thylakoid membrane 2.svg|thumb|320px|right|Нециклический транспорт электронов]] |
||
При слишком сильном освещении и/или закрытых [[Устьице|устьицах]] (голодание по [[диоксид углерода|СО<sub>2</sub>]]) происходит перевосстановление пула [[пластохинон]]ов и, как следствие, перевосстановление пула НАДФ<sup>+</sup>. При недостатке СО<sub>2</sub> НАДФН не может расходоваться в [[Цикл Кальвина|цикле Кальвина]], а значит, не хватает [[Субстрат (биохимия)|субстрата]] для {{нп5|ферредоксин-НАДФ+-редуктаза|ферредоксин-НАДФ<sup>+</sup>-редуктазы|en|Ferredoxin—NADP(+) reductase}}. В конечном итоге это приводит к тому, что ФСI становится некуда сбрасывать возбуждённые электроны, а это в свою очередь может привести к повреждению фотосинтетического аппарата, окислению мембран и образованию [[активные формы кислорода|активных форм кислорода]]{{sfn|Страсбургер|2008|с=117}}. В этих условиях, чтобы предотвратить [[окислительный стресс]] и защититься от фотоповреждения, растения переходят к циклическому транспорту электронов. Полагают, что [[катализатор]]ом циклического транспорта является восстановленный ферредоксин<ref>Кренделева Т. Е., Кукарских Г. П., Тимофеев К. Н., Иванов Б. Н., Рубин А. Б. Ферредоксинзависимый циклический транспорт электронов в изолированных тилакоидах протекает с участием ферредоксин-НАДФ-редуктазы. Доклады академии наук, 2001. 379(5): с. 1-4.</ref><ref>{{ |
При слишком сильном освещении и/или закрытых [[Устьице|устьицах]] (голодание по [[диоксид углерода|СО<sub>2</sub>]]) происходит перевосстановление пула [[пластохинон]]ов и, как следствие, перевосстановление пула НАДФ<sup>+</sup>. При недостатке СО<sub>2</sub> НАДФН не может расходоваться в [[Цикл Кальвина|цикле Кальвина]], а значит, не хватает [[Субстрат (биохимия)|субстрата]] для {{нп5|ферредоксин-НАДФ+-редуктаза|ферредоксин-НАДФ<sup>+</sup>-редуктазы|en|Ferredoxin—NADP(+) reductase}}. В конечном итоге это приводит к тому, что ФСI становится некуда сбрасывать возбуждённые электроны, а это в свою очередь может привести к повреждению фотосинтетического аппарата, окислению мембран и образованию [[активные формы кислорода|активных форм кислорода]]{{sfn|Страсбургер|2008|с=117}}. В этих условиях, чтобы предотвратить [[окислительный стресс]] и защититься от фотоповреждения, растения переходят к циклическому транспорту электронов. Полагают, что [[катализатор]]ом циклического транспорта является восстановленный ферредоксин<ref>Кренделева Т. Е., Кукарских Г. П., Тимофеев К. Н., Иванов Б. Н., Рубин А. Б. Ферредоксинзависимый циклический транспорт электронов в изолированных тилакоидах протекает с участием ферредоксин-НАДФ-редуктазы. Доклады академии наук, 2001. 379(5): с. 1-4.</ref><ref>{{статья |заглавие=Экспериментальное и теоретическое исследование процессов циклического электронного транспорта вокруг фотосистемы 1 |издание=Биофизика |том=48 |номер=4 |страницы=656—665 |ссылка=http://library.biophys.msu.ru/PDF/3346.pdf |язык=ru |тип=журнал |автор=Коваленко И.Б., Устинин Д.М., Грачев Н.Е., Кренделева Т.Е., Кукарских Г.П., Тимофеев К.Н., Ризниченко Г.Ю., Грачев Е.А., Рубин А.Б. |год=2003 |archivedate=2015-04-02 |archiveurl=https://web.archive.org/web/20150402134719/http://library.biophys.msu.ru/PDF/3346.pdf }}</ref>. |
||
=== Циклическое фотофосфорилирование === |
=== Циклическое фотофосфорилирование === |
||
Вначале электрон неким образом перемещается от восстановленного ферредоксина на пул пластохинонов. Точный механизм этого процесса не известен. Полагают, что эту реакцию осуществляет особый фермент |
Вначале электрон неким образом перемещается от восстановленного ферредоксина на пул пластохинонов. Точный механизм этого процесса не известен. Полагают, что эту реакцию осуществляет особый фермент — ферредоксин-пластохинон-оксидоредуктаза. Затем от пластохинона через [[цитохром b6f-комплекс|цитохром ''b''<sub>6</sub>''f''-комплекс]] и пластоцианин электрон вновь попадает на ФСI. При этом происходит закачка [[протон]]а в полость [[тилакоид]]а и идёт синтез [[АТФ]]. В качестве наиболее вероятного кандидата на роль ферредоксин-пластохинон-оксидоредуктазы в последнее время рассматривают ферредоксин-НАДФ<sup>+</sup>-редуктазу, которая может образовывать комплекс с цитохром-''b''<sub>6</sub>''f''-комплексом. Предположительно она может переносить электроны с ферредоксины напрямую на убихинон, связанный цитохром-''b''<sub>6</sub>''f''-комплексом через специальный гем ''c''<sub>n</sub><ref name="Cramer-2006">{{статья |заглавие=Transmembrane traffic in the cytochrome b6f complex |издание={{Нп3|Annual Review of Biochemistry|Annu Rev Biochem||Annual Review of Biochemistry}} |том=75 |страницы=769—790 |doi=10.1146/annurev.biochem.75.103004.142756 |pmid=16756511 |язык=en |тип=journal |автор=Cramer WA.; Zhang H.; Yan j.; Kurisu G.; Smith JL. |год=2006}}</ref><ref name="Cramer-2005">{{статья |заглавие=Structure of the cytochrome b6f complex: new prosthetic groups, Q-space, and the 'hors d'oeuvres hypothesis' for assembly of the complex |издание=Photosynth Res |том=85 |номер=1 |страницы=133—143 |doi=10.1007/s11120-004-2149-5 |pmid=15977064 |язык=en |тип=journal |автор=Cramer WA.; Yan J.; Zhang H.; Kurisu G.; Smith JL. |год=2005}}</ref>. Большое количество данных также говорит в пользу образования суперкомплекса из цитохром-''b''<sub>6</sub>''f''-комплекса, ФСI, ферредоксин-НАДФ<sup>+</sup>-редуктазы и трансмембранного белка PGRL1. Образование и распад такого комплекса, как полагают, переключает режим потока электрона с нециклического на циклический и обратно<ref>{{статья |заглавие=Isolation of the elusive supercomplex that drives cyclic electron flow in photosynthesis |издание=Nature |том=464 |страницы=1210—1213 |doi=10.1038/nature08885 |язык=en |тип=journal |автор=Masakazu Iwai, Kenji Takizawa, Ryutaro Tokutsu, Akira Okamuro, Yuichiro Takahashi & Jun Minagawa |число=22 |месяц=4 |год=2010}}</ref><ref name="Complex">{{статья |заглавие=Cyclic electron flow is redox-controlled but independent of state transition |издание=[[Nature Communications]] |том=4 |doi=10.1038/ncomms2954 |ссылка=http://www.nature.com/ncomms/2013/130613/ncomms2954/full/ncomms2954.html?message-global=remove#ref13 |язык=en |тип=journal |автор=Hiroko Takahashi, Sophie Clowez, Francis-André Wollman, Olivier Vallon & Fabrice Rappaport |число=13 |месяц=6 |год=2013 |издательство=[[Nature Publishing Group]] }}</ref>. |
||
Ещё один фермент, возможно принимающей участие а этом процесс |
Ещё один фермент, возможно принимающей участие а этом процесс — это [[НАДН-дегидрогеназный комплекс хлоропластов]], аналогичный [[НАДН-дегидрогеназный комплекс|НАДH-дегидрогеназному комплексу]] [[митохондрия|митохондрий]] и [[Гомология (биология)|гомологичный]] бактериальному комплексу I<ref>{{статья |doi=10.1074/jbc.M803207200 |заглавие=The Chloroplast NAD(P)H Dehydrogenase Complex Interacts with Photosystem I in Arabidopsis |издание=[[Journal of Biological Chemistry|J Biol Chem.]] |том=283 |номер=50 |страницы=34873—34879. |ссылка=http://www.jbc.org/content/283/50/34873.full |язык=en |тип=journal |автор=Lianwei Peng, Hideyuki Shimizu, Toshiharu Shikanai, |год=2008 |archivedate=2017-09-09 |archiveurl=https://web.archive.org/web/20170909063230/http://www.jbc.org/content/283/50/34873.full }}</ref><ref>{{статья |ссылка=http://onlinelibrary.wiley.com/doi/10.1111/j.1365-313X.2011.04747.x/full |doi=10.1111/j.1365-313X.2011.04747.x |заглавие=Cyclic electron flow around photosystem I via chloroplast NAD(P)H dehydrogenase (NDH) complex performs a significant physiological role during photosynthesis and plant growth at low temperature in rice |издание={{Нп3|The Plant Journal|Plant J.||The Plant Journal}} |том=68 |номер=6 |страницы=966—976 |язык=en |тип=journal |автор=Yamori W., Sakata N., Suzuki Y., Shikanai T., Makino A. |год=2011 |archivedate=2014-12-29 |archiveurl=https://web.archive.org/web/20141229154850/http://onlinelibrary.wiley.com/doi/10.1111/j.1365-313X.2011.04747.x/full }}</ref>. Он окисляет ферредоксин и сбрасывает электроны на пластохинон, предотвращая окислительный стресс. НАДН-дегидрогеназный комплекс хлоропластов образует суперкомплекс с двумя ФСI при помощи белков Lhca5 и Lhca6<ref name="NADP">{{статья |doi=10.1016/j.bbabio.2010.10.015 |заглавие=Structure and biogenesis of the chloroplast NAD(P)H dehydrogenase complex |издание=Biochimica et Biophysica Acta (BBA) |том=1807 |номер=8 |страницы=945—953 |ссылка=http://www.sciencedirect.com/science/article/pii/S0005272810007231 |язык=en |тип=journal |автор=Lianwei Peng, Hiroshi Yamamoto, Toshiharu Shikanai |год=2011 |archivedate=2022-05-06 |archiveurl=https://web.archive.org/web/20220506152536/https://www.sciencedirect.com/science/article/pii/S0005272810007231 }}</ref>. [[Протонный градиент]], созданный в результате циклического фотофосфорилирования на мембране тилакоида, используется белками-переносчиками для встраивания в мембрану приходящих из стромы белков<ref name=Chaddock1995>{{статья |заглавие=A new type of signal peptide: central role of a twin-arginine motif in transfer signals for the delta pH-dependent thylakoidal protein translocase |издание=[[The EMBO Journal|EMBO J.]] |том=14 |номер=12 |страницы=2715—2722 |pmid=7796800 |pmc=398390 |ссылка=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC398390/pdf/emboj00036-0037.pdf |язык=en |тип=journal |автор=Chaddock, A.M.; Mant, A.; Karnauchov, I.; Brink, S.; Herrmann, R.G.; Klösgen, R.B.; Robinson, C. |год=1995 |archivedate=2022-01-22 |archiveurl=https://web.archive.org/web/20220122210447/https://www.ncbi.nlm.nih.gov/pmc/articles/PMC398390/pdf/emboj00036-0037.pdf }}</ref><ref>{{статья |заглавие=Thylakoid ΔpH-dependent precursor proteins bind to a cpTatC–Hcf106 complex before Tha4-dependent transport |издание={{Нп3|Journal of Cell Biology|J Cell Biol.||Journal of Cell Biology}} |том=154 |номер=4 |страницы=719—730 |doi=10.1083/jcb.200105149 |ссылка=http://jcb.rupress.org/content/154/4/719.full |язык=en |тип=journal |автор=Kenneth Cline and Hiroki Mori |число=20 |месяц=8 |год=2001 |archivedate=2015-07-18 |archiveurl=https://web.archive.org/web/20150718230356/http://jcb.rupress.org/content/154/4/719.full }}</ref>. |
||
=== Псевдоциклический транспорт === |
=== Псевдоциклический транспорт === |
||
| Строка 223: | Строка 211: | ||
:: <math>\mathsf {Fd_{red} + O_2 \rightarrow Fd_{ox} + O_2^- \cdot}</math> |
:: <math>\mathsf {Fd_{red} + O_2 \rightarrow Fd_{ox} + O_2^- \cdot}</math> |
||
Ещё один фермент, участвующий в псевдоциклическом транспорте, это [[терминальная оксидаза]] хлоропластов, гомологичная [[Альтернативная оксидаза|альтернативной оксидазе]] растительных митохондрий. Она окисляет пул пластохинонов с участием кислорода, образуя воду и рассеивая энергию в форме тепла<ref name="pmid21056542">{{ |
Ещё один фермент, участвующий в псевдоциклическом транспорте, это [[терминальная оксидаза]] хлоропластов, гомологичная [[Альтернативная оксидаза|альтернативной оксидазе]] растительных митохондрий. Она окисляет пул пластохинонов с участием кислорода, образуя воду и рассеивая энергию в форме тепла<ref name="pmid21056542">{{статья |заглавие=Flexibility in photosynthetic electron transport: the physiological role of plastoquinol terminal oxidase (PTOX) |издание={{Нп3|Biochimica et Biophysica Acta|Biochim. Biophys. Acta||Biochimica et Biophysica Acta}} |том=1807 |номер=8 |страницы=954—967 |pmid=21056542 |doi=10.1016/j.bbabio.2010.10.024 |ссылка=http://www.sciencedirect.com/science/article/pii/S0005272810007425 |язык=en |тип=journal |автор=McDonald A.E., Ivanov A.G., Bode R., Maxwell D.P., Rodermel S.R., Hüner N.P. |месяц=8 |год=2011 |archivedate=2015-09-24 |archiveurl=https://web.archive.org/web/20150924150935/http://www.sciencedirect.com/science/article/pii/S0005272810007425 }}</ref>. |
||
== Локализация в мембране тилакоида == |
== Локализация в мембране тилакоида == |
||
[[Файл: |
[[Файл:Tilacoid structure.png|thumb|Размещение фотосинтетических комплексов в мембране тилакоида]] |
||
Фотосистема I находится в стромальных тилакоидах (32 %), а также в маргинальных (36 %) и торцевых (32 %) областях гран. Такое расположение обусловлено плотностью её поверхностного заряда и силами электростатического отталкивания с другими комплексами{{sfn|Ермаков|2005|с=123}}. |
Фотосистема I находится в стромальных тилакоидах (32 %), а также в маргинальных (36 %) и торцевых (32 %) областях гран. Такое расположение обусловлено плотностью её поверхностного заряда и силами электростатического отталкивания с другими комплексами{{sfn|Ермаков|2005|с=123}}. |
||
У [[цианобактерии|цианобактерий]] и [[прохлорофиты|прохлорофитов]] фотосистема I способна образовывать [[тример]]ы. Это способствует увеличению спектра поглощения на больших глубинах, а также более эффективному перераспределению энергии возбуждения и защите от фотоповреждений<ref>{{ |
У [[цианобактерии|цианобактерий]] и [[прохлорофиты|прохлорофитов]] фотосистема I способна образовывать [[тример]]ы. Это способствует увеличению спектра поглощения на больших глубинах, а также более эффективному перераспределению энергии возбуждения и защите от фотоповреждений<ref>{{статья |заглавие=The photosystem I trimer of cyanobacteria: molecular organization, excitation dynamics and physiological significance |издание={{Нп3|FEBS Letters|FEBS letters||FEBS Letters}} |том=460 |номер=3 |страницы=395—400 |doi=10.1016/S0014-5793(99)01352-6 |ссылка=http://www.sciencedirect.com/science/article/pii/S0014579399013526 |язык=en |тип=journal |автор=Navassard V. Karapetyan, Alfred R. Holzwarth, Matthias Rögner |год=1999 |archivedate=2022-01-20 |archiveurl=https://web.archive.org/web/20220120201330/https://www.sciencedirect.com/science/article/pii/S0014579399013526 }}</ref>. У эукариот фотосистема I утратила эту способность благодаря наличию субъединицы H, а также мутации в субъединице L. Вместо тримерезации у эукариот она при помощи субъединиц L и G взаимодействует с большими мембранными светособирающими комплексами, которых нет у прокариот<ref>{{статья |заглавие=Evolution of photosystem I – from symmetry through pseudosymmetry to asymmetry |издание={{Нп3|FEBS Letters|FEBS letters||FEBS Letters}} |том=565 |номер=3 |страницы=274—280 |doi=10.1016/S0014-5793(04)00360-6 |ссылка=http://www.sciencedirect.com/science/article/pii/S0014579304003606 |язык=en |тип=journal |автор=Adam Ben-Shema, Felix Frolowb, Nathan Nelsona, |год=30 April 2004}}</ref>. |
||
=== Белок Ycf4 === |
=== Белок Ycf4 === |
||
{{main|Белок Ycf4}} |
{{main|Белок Ycf4}} |
||
Трансмембранный белок Ycf4, обнаруженный в мембране тилакоида, жизненно необходим для функционирования фотосистемы I. Он участвует в сборке компонентов комплекса, без него фотосинтез становится неэффективным<ref name="pmid9321389">{{ |
Трансмембранный белок Ycf4, обнаруженный в мембране тилакоида, жизненно необходим для функционирования фотосистемы I. Он участвует в сборке компонентов комплекса, без него фотосинтез становится неэффективным<ref name="pmid9321389">{{статья |заглавие=The chloroplast ycf3 and ycf4 open reading frames of Chlamydomonas reinhardtii are required for the accumulation of the photosystem I complex |издание=[[The EMBO Journal|EMBO J]] |том=16 |номер=20 |страницы=6095—6104 |pmid=9321389 |doi=10.1093/emboj/16.20.6095 |pmc=1326293 |ссылка=http://emboj.embopress.org/content/16/20/6095 |язык=en |тип=journal |автор=Boudreau E., Takahashi Y., Lemieux C., Turmel M., Rochaix J.D. |год=1997 |archivedate=2016-03-07 |archiveurl=https://web.archive.org/web/20160307001516/http://emboj.embopress.org/content/16/20/6095 }}</ref>. |
||
== Зелёные серобактерии и эволюция ФСI == |
== Зелёные серобактерии и эволюция ФСI == |
||
| ⚫ | [[Молекулярная биология|Молекулярно-биологические]] данные говорят в пользу того, что ФСI, вероятно, [[Эволюция (биологическая)|эволюционировала]] из фотосистемы [[Зелёные серобактерии|зелёных серобактерий]]. [[Реакционные центры]] зелёных серобактерий, цианобактерий, водорослей и [[высшие растения|высших растений]] различаются, однако домены, выполняющие аналогичные функции, имеют схожее строение<ref name="Lockau">{{статья |doi=10.1111/j.1399-3054.1993.tb05512.x |заглавие=Photosystem I and its Bacterial Counterparts |издание={{Нп3|Physiologia Plantarum}} |том=88 |номер=2 |страницы=372—381 |язык=en |автор=Lockau, Wolfgang, Wolfgang Nitschke |год=1993 |тип=journal}}</ref>. Так, во всех трёх системах окислительно-восстановительный потенциал достаточен для восстановления ферредоксина<ref name="Lockau"/>. Все три электронотранспортные цепи содержат железо-серные белки<ref name="Lockau"/>. И наконец, все три фотосистемы представляют собой димер двух [[Гидрофобность|гидрофобных]] белков, на которых закреплены редокс-центры и [[пигменты]] интегральной антенны<ref name="Lockau"/>. В свою очередь, фотосистема зелёных серобактерий содержит те же самые [[кофактор]]ы, что и электронотранспортная цепь фотосистемы I<ref name="Lockau"/>. |
||
| ⚫ | [[Молекулярная биология|Молекулярно-биологические]] данные говорят в пользу того, что ФСI, вероятно, [[Эволюция (биологическая)|эволюционировала]] из фотосистемы [[Зелёные серобактерии|зелёных серобактерий]]. [[Реакционные центры]] зелёных серобактерий, цианобактерий, водорослей и [[высшие растения|высших растений]] различаются, однако домены, выполняющие аналогичные функции, имеют схожее строение<ref name="Lockau">{{ |
||
== Галерея == |
== Галерея == |
||
<gallery> |
<gallery> |
||
Image:1QZV.png|Положение хлорофиллов и кофакторов в фотосистеме I. |
Image:1QZV.png|Положение хлорофиллов и кофакторов в фотосистеме I. |
||
Image: |
Image:022-PhotosystemI-1jb0.tiff |Тример фотосистемы I |
||
Image: |
Image:022-PhotosystemI-1jb0-etc.tiff |ЭТЦ фотосистемы I |
||
Image: |
Image:022-PhotosystemI-reaction-centers.tiff |Фотосистемы I и [[реакционный центр]] бактерии. |
||
Image:Fotoukład 1.svg|Модель фотосистемы I. |
Image:Fotoukład 1.svg|Модель фотосистемы I. |
||
</gallery> |
</gallery> |
||
| Строка 303: | Строка 290: | ||
* [http://fizrast.ru/fotosintez/etapy/fotohimiya/potok-elektonov.html «Циклический и нециклический поток электронов.»] в онлайн энциклопедии Физиология растений |
* [http://fizrast.ru/fotosintez/etapy/fotohimiya/potok-elektonov.html «Циклический и нециклический поток электронов.»] в онлайн энциклопедии Физиология растений |
||
{{внешние ссылки}} |
|||
{{Хорошая статья|Химия|Биология}} |
{{Хорошая статья|Химия|Биология}} |
||
Текущая версия от 01:20, 14 августа 2024

Фотосисте́ма I (первая фотосистема, фотосистема один, ФСI), или пластоциани́н-ферредокси́н-оксидоредукта́за — второй функциональный комплекс электрон-транспортной цепи (ЭТЦ) хлоропластов. Он принимает электрон от пластоцианина и, поглощая световую энергию, формирует сильный восстановитель П700, способный через цепь переносчиков электронов осуществить восстановление НАДФ+. Таким образом, при участии ФСI синтезируется источник электронов (НАДФН) для последующих реакций восстановления углерода в хлоропластах в цикле Кальвина. Кроме того, ФСI может осуществлять циклический транспорт электронов, сопряжённый с синтезом АТФ, обеспечивая дополнительный синтез АТФ в хлоропластах[1].
История открытия
[править | править код]Нециклический транспорт электронов начинается с того, что марганцевый кластер фотосистемы II окисляет воду, восстанавливая пул пластохинонов. Далее цитохром b6f-комплекс окисляет пластохиноны, а электрон через пластоцианин передаётся на фотосистему I, где используется для синтеза НАДФН. Нарушение формальной логики в названиях фотосистем связано с тем, что фотосистема I была открыта раньше, чем фотосистема II.
Первые данные указывающие на существование ФСI появились в 1950-х годах, но в то время никто ещё не мог оценить значимость этих открытий[2]. Представление о существовании в хлоропластах двух фотосистем возникло в уже в 1940-е годы на основание опытов лаборатории Р. Эмерсона, обнаружившего эффект падения квантового выхода фотосинтеза при освещении хлоропластов монохроматическим красным светом (λ>680 нм), возбуждающим только ФСI, и эффект усиления квантового выхода при добавлении подсветки с длиной волны около 650 нм, которая возбуждала ФСII (так называемый эффект Эмерсона). Также следует упомянуть открытый Комоннером в 1956 году светоиндуцируемый ЭПР сигнал, который был назван сигналом I. По чистой случайности сигнал I и сигнал II, исходили от ФСI и ФСII соответственно[2]. Лишь в 1960 году Луис Дюйзенс предложил концепцию фотосистемы I и фотосистемы II, и в том же году Фэй Бендалл и Роберт Хилл организовали результаты предыдущих открытий в стройную теорию последовательных реакций фотосинтеза[2]. Гипотеза Хилла и Бендалля была позднее подтверждена в экспериментах Дюйзенса и Витта в 1961 году[2].
После этого начались систематические попытки физического выделения фотосистемы I, определения её трёхмерной структуры и тонкого строения. В 1966 году начался бум исследований в этой области: Андерсон и Бордман подвергали мембраны хлоропластов воздействию ультразвука с последующей обработкой дигитонином, Вернон использовал тритон X-100, а Огава — додецилсульфат. Однако, первые полученные экстракты содержали примеси светосособирающих комплексов, а также цитохромов f и b6. Потребовалось много времени, чтобы разобраться, что полученные экстракты были смесью[2].
В 1968 году Рид и Клайтон смогли выделить реакционный центр фотосистемы I из пурпурных бактерий, что значительно подстегнуло исследования оксигенного фотосинтеза. Однако, открытым оставался вопрос: что из выделенного являлось истинным реакционным центром, что антенными комплексами, а что дополнительными субъединицами. Долгое время эффективное выделение реакционного центра фотосистемы I оставалось неразрешённой проблемой. В конце-концов оказалось, что легче всего это сделать у цианобактерий, поскольку у них отсутствовали интегрированные в мембрану внешние антенны. После многочисленных попыток с разными видами, выяснилось, что самыми многообещающими в этом отношение видами являются представителями Synechocystis и Synechococcus, поскольку фотосистема I, выделенная из Thermosynechococcus elongatus давала очень стабильный реакционный центр, пригодный для кристаллизации и исследования методом рентгеноструктурного анализ[2].
Отличия от фотосистемы II
[править | править код]Основная функция фотосистемы II — генерация сильного окислителя, который инициирует окисление воды и передачу её электронов на мембранный переносчик. Основная функция фотосистемы I — насытить эти низкоуровневые электроны энергией, чтобы с их помощью осуществить восстановление НАДФ+. Поскольку энергия суммарного процесса слишком велика, чтобы осуществить его в рамках одного реакционного центра, в ходе эволюции появились две фотосистемы, которые раздельно осуществляют разные части этой реакции. Их специфические функции и определяют особенности их строения. Так, фотосистема I — симметрична, то есть в ней работают две ветви электронного транспорта, что делает его значительно более быстрым, в то время как фотосистема II — асимметрична и обладает только одной рабочей ветвью, что замедляет транспорт электронов, но делает его более управляемым. Обе фотосистемы значительно отличаются по строению антенн, дополнительных субъединиц, способов регуляции и своему положению в мембране[3]. Так, фотосистема I обладает интегральной антенной, хлорофиллы которой расположены непосредственно на главных белках комплекса — А и B, в то время как у фотосистемы II они вынесены на внешние белки CP47 и CP43. По количеству дополнительных малых регуляторных субъединиц ФС II значительно превосходит ФС I, что связано с необходимостью тонкой регуляции процесса окисления воды, который потенциально крайне опасен для клетки. Этим же объясняется неоднородное распределение фотосистем в мембране тилакоида: в то время как ФС I располагается преимущественно в области маргинальных, торцевых и стромальных мембран, ФС II практически полностью находится в области спаренных мембран, что обеспечивает клетке дополнительную защиту от продуцируемых ею активных форм кислорода[4].
Главное отличие фотосистемы II от фотосистемы I — это наличие большого обращённого в люмен домена, который содержит марганцевый кластер и окружающие его защитные белки. Именно здесь происходит процесс фотохимического окисления воды, сопровождаемый выделением кислорода и протонов[3].
Структурная организация фотосистемы I
[править | править код]| Фотосистема I | |
|---|---|
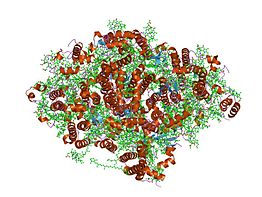
 Растительная Фотосистема I | |
| Идентификаторы | |
| Шифр КФ | 1.97.1.12 |
| Базы ферментов | |
| IntEnz | IntEnz view |
| BRENDA | BRENDA entry |
| ExPASy | NiceZyme view |
| MetaCyc | metabolic pathway |
| KEGG | KEGG entry |
| PRIAM | profile |
| PDB structures | RCSB PDB PDBe PDBj PDBsum |
| Поиск | |
| PMC | статьи |
| PubMed | статьи |
| NCBI | NCBI proteins |
| PsaA_PsaB | |
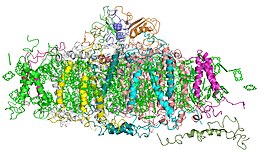
|---|---|
 Структура Фотосистемы I из цианобактерии. Показана интегральная часть(ядро) и белки внешней антенны. | |
| Идентификаторы | |
| Символ | PsaA_PsaB |
| Pfam | PF00223 |
| InterPro | IPR001280 |
| PROSITE | PDOC00347 |
| SCOP | 1jb0 |
| SUPERFAMILY | 1jb0 |
| TCDB | 5.B.4 |
| OPM superfamily | 2 |
| OPM protein | 1jb0 |
| Доступные структуры белков | |
| Pfam | структуры |
| PDB | RCSB PDB; PDBe; PDBj |
| PDBsum | 3D-модель |
Фотосистема I состоит из следующих белковых субъединиц и кофакторов[5][6][1]:
| Субъединицы | Описание |
|---|---|
| A | 83 кДа, 751 аминокислотных остатков |
| B | 82,5 кДа, 735 аминокислотных остатков |
| C | 8,9 кДа, перенос электрона с П700 на ферредоксин |
| D | 19 кДа, обеспечивает связь с ферредоксином |
| E | 7,5 кДа, обеспечивает связь с ферредоксином |
| F | 19 кДа, взаимодействует с пластоцианином |
| G | 8 кДа, только у растений |
| H | 10 кДа, у растений предотвращает формирования тримеров ФСI, обеспечивает взаимодействие со светособирающим комплексом II |
| I | 5 кДа, у растений взаимодействует с PsaH, связывается со светособирающим комплексом II; у цианобактерий играет важную роль в формировании тримеров ФСI |
| J | 5 кДа, несёт три молекулы хлорофилла и выполняет структурную функцию |
| K | 8.5 кДа, несёт две молекулы хлорофилла и выполняет структурную функцию |
| L | 16 кДа, у цианобактерий участвуют в формировании тримера ФСI; у растений она связывает со светособирающим комплексом II |
| M | 3,5 кДа, только у цианобактерий; расположена в области контакта ФСI в тримере |
| N | 9 кДа, есть у растений и водорослей |
| O | только у растений; функция неизвестна |
| X | 4 кДа, только у цианобактерий |
| Пигменты | |
| Хлорофилл a | 95 молекул в антенной системе |
| Хлорофилл а | 2 молекулы дополнительного хлорофилла а |
| Хлорофилл a0 | Хлорофилл а695 — первичный акцептор электронов |
| Хлорофиллы а и a' | специальная пара П700 |
| β-Каротин | 22 молекулы |
| Коферменты/Кофакторы | |
| Fa | Fe4S4 железосерный кластер (ЭТЦ) |
| Fb | Fe4S4 железосерный кластер (ЭТЦ) |
| Fx | Fe4S4 железосерный кластер (ЭТЦ) |
| Ферредоксин | Переносчик электронов |
| Пластоцианин | Растворимый белок, содержащий атом меди |
| QK-A | Филлохинон — акцептор электронов в ЭТЦ (субъединица А) |
| QK-B | Филлохинон — акцептор электронов в ЭТЦ (субъединица В) |
| Ca2+ | ион кальция |
| Mg2+ | ион магния |
Основная функция ФСI — передача энергии света на электрон, перенос электрона от пластоцианина к ферредоксину[7]. ФСI содержит свыше 110 кофакторов, значительно больше чем фотосистема II[8]. Каждый из этих компонентов имеет широкий спектр функций. Основные компоненты электрон-транспортной цепи ФСI — главный донор возбуждённых электронов П700 (хлорофильный димер) и пять переносчиков: A0 (хлорофилл а), A1 (филлохинон) и три Fe4S4 железосерных кластера: Fx, Fa, и Fb[9].
Структурно ФСI представляет собой гетеродимер двух интегральных белковых комплексов — А и В (у всех растений кодируются хлоропластными генами PsaA и PsaB). Белки А и В присоединяют димер Р700, по одной молекуле мономера хлорофилла а (Хл695) — первичного акцептора электронов А0, по одному дополнительному хлорофиллу а и по одной молекуле филлохинона (А1). Два набора дополнительных хлорофиллов а, первичных акцепторов электрона и филлохинонов формируют две почти симметричные ветви транспорта электронов от Р700 к Fx. В отличие от реакционных центров зелёных и пурпурных бактерий и ФСII, где из двух ветвей функционирует лишь одна, в ФСI активны обе ветви электронного транспорта, хотя они и не идентичны[1].Белок А гомологичен белкам D1+СP43 (молекулярная масса белка А соответствует сумме молекулярных масс белков D1 и СP43) из фотосистемы II, а белок В гомологичен белкам D2+CP47 соответственно[10].
Обе субъединицы содержат 11 трансмембранных сегментов[англ.]. Железосодержащий кластер Fx связан четырьмя цистеинами, два из которых находятся на субъединице А, и ещё два на субъединице В. В обоих белках цистеины находятся на проксимальном конце, в петле между девятым и десятым трансмембранными сегментами. По всей вероятности, ниже цистеинов находится так называемый мотив лейциновой молнии, который вносит существенный вклад в димеризацию белков А и В[11]. Конечные акцепторы электронов FA и FB находятся на субъединице С[12][13].
Следует особо подчеркнуть, что перенос электрона осуществляется в соответствии с термодинамическим потенциалом. Увеличение окислительно-восстановительных потенциалов в цепи акцепторов обеспечивает быстрое снижение энергии, что предотвращает возврат электрона к пигменту и бесполезную трату энергии электронного возбуждения. Благодаря этому энергия возбуждения эффективно используется для разделения зарядов[14].
Пластоцианин
[править | править код]
Пластоцианин — маленький, подвижный белок с молекулярной массой около 10,5 кДа. К его центральному атому Сu присоединяются остатки цистеина и метионина, а сбоку его стабилизируют два остатка гистидина. При обратимой смене валентности Cu2+ ↔ Cu+1 пластоцианин либо поглощает один электрон, либо отдаёт его. Пластоцианин является аналогом цитохрома c, который выполняет схожую функцию в дыхательной цепи митохондрий[6].
Он принимает электрон от цитохром b6f-комплекса, окисляя цитохром f и перенося его непосредственно на реакционный центр П700 фотосистемы I. На внешней стороне белка имеется группа аминокислот, несущих отрицательный заряд[16]. Предположительно, они связываются с положительно заряженным люминальным доменом субъединицы F, однако механизм связывания недостаточно изучен и остаётся неясным[17].
У некоторых водорослей и цианобактерий при недостатке меди в среде пластоцианин не образуется, вместо него синтезируется и выполняет его функции цитохром c-553[18].
- Пластоцианин (PC) отдаёт один электрон окисленному П700+ и восстанавливает его до исходного состояния:
Специальная пара П700
[править | править код]П700 (в английской литературе P700) представляет собой димер хлорофилла а и хлорофилла а‘ у которого кетоэфирная группа в V кольце находится в цис-положении относительно плоскости молекулы, с максимумом поглощения 700 нм[19]. Наличие цис-кетоэфирной группы делает возможным образование димера из двух хлорофиллов посредством формирования водородных связей. П700 получает энергию от антенных комплексов и использует её, чтобы поднять электроны на более высокий уровень. Далее электрон в ходе окислительно-восстановительной реакции переходит на цепь переносчиков. В окисленном состоянии окислительно-восстановительный редокс-потенциал П700 составляет +0,52 В, а в фотовозбуждённом состоянии он становится −1,2 В, то есть формируется мощный восстановитель, обеспечивающий восстановление НАДФ+[20][21].
- В соответствии со следующим уравнением П700 поглощает квант света и переходит в фотовозбуждённое состояние, в результате чего один из его электронов переходит с основного подуровня S0 на первый синглетный подуровень S1:
Хлорофилл А0
[править | править код]A0 — первый акцептор электронов в фотосистеме I. Именно здесь происходит первичное фотохимическое разделение зарядов между фотовозбуждённым П700* и A0. Его максимум поглощения составляет 695 нм (Хл а695), что объясняется его взаимодействием с окружающими аминокислотными остатками[19]. Его редокс-потенциал в восстановленном состоянии −1,1 В[1].
- Фотовозбуждённый П700* отдаёт один электрон хлорофиллу A0, в результате чего происходит разделение зарядов, и образуется первичная радикальная пара:
Филлохинон A1
[править | править код]Следующий акцептор — это Филлохинон A1, также известный как витамин K1. Он, как и хлорофилл, обладает фитольным хвостом[22], и приблизительно соответствует пластохинону QA фотосистемы II. Поглощая электрон, он образует семихинон-радикал, который восстанавливает Fx, передаёт его на Fb и далее на Fa[22][23].
Железосерные кластеры
[править | править код]Железосерные кластеры ФСI имеют форму куба с четырьмя атомами железа и четырьмя атомами серы, составляющими его восемь вершин. Все три кластера связаны с белками ФСI через остатки цистеина[24]. Fx (Eо‘ = −0,70 В) окисляет восстановленный А1. Дальнейший транспорт осуществляют железосерные кластеры Fa, и Fb, характеризующиеся низкими окислительно-восстановительными потенциалами (-0,59 и −0,55 В соответственно). Множество экспериментов выявило несоответствие между разными теориями, описывающими расположение и работу железосерных кластеров[24]. Однако большинство результатов позволяет сделать некоторые общие выводы. Во-первых, Fx, Fa, и Fb образуют треугольник, и Fa располагается ближе к Fx чем Fb[24]. Во-вторых, транспорт электронов начинается с Fx через Fa к Fb, или же через Fa к Fb. До сих пор ведутся споры о том, какой из двух кластеров осуществляет перенос электрона на ферредоксин[24].
Ферредоксин
[править | править код]Ферредоксин — это водорастворимый белок с молекулярной массой 11 кДа и содержащий Fe2S2 центр[25]. Примечательно, что он является одноэлектронной окислительно-восстановительной системой, то есть переносит только один электрон, полученный им от железосерных кластеров. Он восстанавливается ФСI на стромальной стороне мембраны и в восстановленном состоянии является сильным восстановителем (Eo‘ = —0,6 В), благодаря чему может быть переносчиком электронов для различных реакций, протекающих в хлоропласте. Так, ферредоксин поставляет электроны для восстановления нитритов, (нитритредуктаза) и ассимиляции серы (сульфитредуктаза) в хлоропласте. Также он поставляет электроны для фиксации атмосферного азота (нитрогеназа) у бактерий. Он восстанавливает тиоредоксин — низкомолекулярный серосодержащий белок, участвующий в редокс-регуляции хлоропластов, активируя ключевые ферменты цикла Кальвина. При нециклическом транспорте электронов ферредоксин взаимодействует с ферредоксин-НАДФ(+) редуктазой, которая восстанавливает НАДФ+ до НАДФН (Eo‘ = −0,32 В) в строме хлоропласта[25].
Светособирающий комплекс
[править | править код]
Светособирающие комплексы состоят из молекул хлорофилла а и b и каротиноидов, соединённых с белками[20]. Эти пигменты, возбуждаясь, переносят энергию фотонов в реакционный центр фотосистемы по Фёрстеровскому механизму. В отличие от реакционного центра ФСI, светособирающие комплексы могут поглощать практически во всей области видимого спектра[26]. Антенные комплексы подразделяют на внутренние, или интегральные, антенны, непосредственно присоединённые к комплексу фотосистемы, и периферические подвижные светособирающие комплексы (ССКI). Так, белки А и В присоединяют пигменты внутренней антенны ФСI: около 95 молекул хлорофилла а и 22 молекулы β-каротина, 5 из которых находятся в цис-конформации. В координации по крайней мере десяти хлорофиллов внутренней антенны принимают участие малые субъединицы J, K, L, M и X. Пигменты внутренней антенны располагаются в виде цилиндра, окружающего все компоненты электрон-транспортной цепи фотосистемы I. Это отличает ФСI от ФСII, где пигменты внутренней антенны расположены на отдельных белках CP43 и CP77[1]. Внешний светособирающий комплекс ССКI (LHCI) содержит 80—120 молекул хлорофиллов а и b, каротиноиды и состоит из четырёх субъединиц: Lhca1, Lhca2, Lhca3 и Lhca4 — с молекулярными массами 17—24 кДа. Относительно недавно были открыты две дополнительные субъединицы, Lhca5 и Lhca6, однако их концентрация в мембране тилакоида крайне мала, а кодирующие их гены практически не экспрессируются[27][28].
Циклический транспорт электронов
[править | править код]
При слишком сильном освещении и/или закрытых устьицах (голодание по СО2) происходит перевосстановление пула пластохинонов и, как следствие, перевосстановление пула НАДФ+. При недостатке СО2 НАДФН не может расходоваться в цикле Кальвина, а значит, не хватает субстрата для ферредоксин-НАДФ+-редуктазы[англ.]. В конечном итоге это приводит к тому, что ФСI становится некуда сбрасывать возбуждённые электроны, а это в свою очередь может привести к повреждению фотосинтетического аппарата, окислению мембран и образованию активных форм кислорода[6]. В этих условиях, чтобы предотвратить окислительный стресс и защититься от фотоповреждения, растения переходят к циклическому транспорту электронов. Полагают, что катализатором циклического транспорта является восстановленный ферредоксин[29][30].
Циклическое фотофосфорилирование
[править | править код]Вначале электрон неким образом перемещается от восстановленного ферредоксина на пул пластохинонов. Точный механизм этого процесса не известен. Полагают, что эту реакцию осуществляет особый фермент — ферредоксин-пластохинон-оксидоредуктаза. Затем от пластохинона через цитохром b6f-комплекс и пластоцианин электрон вновь попадает на ФСI. При этом происходит закачка протона в полость тилакоида и идёт синтез АТФ. В качестве наиболее вероятного кандидата на роль ферредоксин-пластохинон-оксидоредуктазы в последнее время рассматривают ферредоксин-НАДФ+-редуктазу, которая может образовывать комплекс с цитохром-b6f-комплексом. Предположительно она может переносить электроны с ферредоксины напрямую на убихинон, связанный цитохром-b6f-комплексом через специальный гем cn[31][32]. Большое количество данных также говорит в пользу образования суперкомплекса из цитохром-b6f-комплекса, ФСI, ферредоксин-НАДФ+-редуктазы и трансмембранного белка PGRL1. Образование и распад такого комплекса, как полагают, переключает режим потока электрона с нециклического на циклический и обратно[33][34].
Ещё один фермент, возможно принимающей участие а этом процесс — это НАДН-дегидрогеназный комплекс хлоропластов, аналогичный НАДH-дегидрогеназному комплексу митохондрий и гомологичный бактериальному комплексу I[35][36]. Он окисляет ферредоксин и сбрасывает электроны на пластохинон, предотвращая окислительный стресс. НАДН-дегидрогеназный комплекс хлоропластов образует суперкомплекс с двумя ФСI при помощи белков Lhca5 и Lhca6[28]. Протонный градиент, созданный в результате циклического фотофосфорилирования на мембране тилакоида, используется белками-переносчиками для встраивания в мембрану приходящих из стромы белков[37][38].
Псевдоциклический транспорт
[править | править код]При очень активном восстановлении пула ферредоксинов происходит сброс их электронов на О2 с образованием H2O (так называемая реакция Мелера). Он сходен с циклическим транспортом тем, что не синтезируется НАДФН, а только АТФ. Однако в условиях реакции Мелера соотношение АТФ/АДФ очень велико, так что имеющегося количества АДФ не достаточно для синтеза АТФ, и, как следствие, на мембране тилакоида создаётся очень высокий протонный градиент. В результате реакции происходит образование супероксид-анион-радикала O2-·, который превращается в O2 и H2O2 под воздействием фермента супероксиддисмутазы, а перекись превращается в воду ферментом аскорбатпероксидазой[6].
Ещё один фермент, участвующий в псевдоциклическом транспорте, это терминальная оксидаза хлоропластов, гомологичная альтернативной оксидазе растительных митохондрий. Она окисляет пул пластохинонов с участием кислорода, образуя воду и рассеивая энергию в форме тепла[39].
Локализация в мембране тилакоида
[править | править код]
Фотосистема I находится в стромальных тилакоидах (32 %), а также в маргинальных (36 %) и торцевых (32 %) областях гран. Такое расположение обусловлено плотностью её поверхностного заряда и силами электростатического отталкивания с другими комплексами[40].
У цианобактерий и прохлорофитов фотосистема I способна образовывать тримеры. Это способствует увеличению спектра поглощения на больших глубинах, а также более эффективному перераспределению энергии возбуждения и защите от фотоповреждений[41]. У эукариот фотосистема I утратила эту способность благодаря наличию субъединицы H, а также мутации в субъединице L. Вместо тримерезации у эукариот она при помощи субъединиц L и G взаимодействует с большими мембранными светособирающими комплексами, которых нет у прокариот[42].
Белок Ycf4
[править | править код]Трансмембранный белок Ycf4, обнаруженный в мембране тилакоида, жизненно необходим для функционирования фотосистемы I. Он участвует в сборке компонентов комплекса, без него фотосинтез становится неэффективным[43].
Зелёные серобактерии и эволюция ФСI
[править | править код]Молекулярно-биологические данные говорят в пользу того, что ФСI, вероятно, эволюционировала из фотосистемы зелёных серобактерий. Реакционные центры зелёных серобактерий, цианобактерий, водорослей и высших растений различаются, однако домены, выполняющие аналогичные функции, имеют схожее строение[44]. Так, во всех трёх системах окислительно-восстановительный потенциал достаточен для восстановления ферредоксина[44]. Все три электронотранспортные цепи содержат железо-серные белки[44]. И наконец, все три фотосистемы представляют собой димер двух гидрофобных белков, на которых закреплены редокс-центры и пигменты интегральной антенны[44]. В свою очередь, фотосистема зелёных серобактерий содержит те же самые кофакторы, что и электронотранспортная цепь фотосистемы I[44].
Галерея
[править | править код]-
Положение хлорофиллов и кофакторов в фотосистеме I.
-
Тример фотосистемы I
-
ЭТЦ фотосистемы I
-
Фотосистемы I и реакционный центр бактерии.
-
Модель фотосистемы I.
См. также
[править | править код]Примечания
[править | править код]- ↑ 1 2 3 4 5 Ермаков, 2005, с. 173-175.
- ↑ 1 2 3 4 5 6 Fromme P., Mathis P. Unraveling the photosystem I reaction center: a history, or the sum of many efforts (англ.) // Drugs[англ.] : journal. — Adis International, 2004. — Vol. 80, no. 1—3. — P. 109—124. — doi:10.1023/B:PRES.0000030657.88242.e1. — PMID 16328814. Архивировано 22 декабря 2015 года.
- ↑ 1 2 Ермаков, 2005, с. 121.
- ↑ Ravi Danielsson, Marjaana Suorsa, Virpi Paakkarinen, Per-Åke Albertsson, Stenbjörn Styring, Eva-Mari Aro and Fikret Mamedov. Dimeric and Monomeric Organization of Photosystem II (англ.) // The Journal of Biological Chemistry : journal. — 2006. — May (no. 281). — P. 14241—14249. — doi:10.1074/jbc.M600634200.
- ↑ Saenger W., Jordan P., Krauss N. The assembly of protein subunits and cofactors in photosystem I (англ.) // Curr. Opin. Struct. Biol. : journal. — 2002. — April (vol. 12, no. 2). — P. 244—254. — doi:10.1016/S0959-440X(02)00317-2. — PMID 11959504. Архивировано 4 ноября 2018 года.
- ↑ 1 2 3 4 Страсбургер, 2008, с. 117.
- ↑ Golbeck J.H. Structure, function and organization of the Photosystem I reaction center complex (англ.) // Biochim. Biophys. Acta[англ.] : journal. — 1987. — Vol. 895, no. 3. — P. 167—204. — doi:10.1016/s0304-4173(87)80002-2. — PMID 3333014.
- ↑ HongQi Yu', Ingo Gortjohann, Yana Bukman, Craig Yolley', Devendra K. Chauhan, Alexander Melkozerov and Petra Fromme. Structure and funcnions of photosystems I and II (неопр.). Архивировано 1 января 2017 года.
- ↑ Jagannathan, Bharat; Golbeck, John. Photosynthesis:Microbial (англ.) // Encyclopedia of Microbiology, 3rd Ed : book. — 2009. — P. 325—341. — doi:10.1016/B978-012373944-5.00352-7.
- ↑ Хелдт, 2011, с. 99.
- ↑ Webber A.N., Malkin R. Photosystem I reaction-centre proteins contain leucine zipper motifs. A proposed role in dimer formation (англ.) // FEBS Lett.[англ.] : journal. — 1990. — May (vol. 264, no. 1). — P. 1—4. — doi:10.1016/0014-5793(90)80749-9. — PMID 2186925.
- ↑ Jagannathan, Bharat; Golbeck, John. Breaking biological symmetry in membrane proteins: The asymmetrical orientation of PsaC on the pseudo-C2 symmetric Photosystem I core (англ.) // Cell. Mol. Life Sci. : journal. — 2009. — Vol. 66, no. 7. — P. 1257—1270. — doi:10.1007/s00018-009-8673-x.
- ↑ Jagannathan, Bharat; Golbeck, John. Understanding of the Binding Interface between PsaC and the PsaA/PsaB Heterodimer in Photosystem I (англ.) // Biochemistry : journal. — 2009. — Vol. 48. — P. 5405—5416. — doi:10.1021/bi900243f.
- ↑ Ермаков, 2005, с. 157.
- ↑ PDB 3BQV. Дата обращения: 14 января 2015. Архивировано 24 февраля 2017 года.
- ↑ Frazão C., Sieker L., Sheldrick G., Lamzin V., LeGall J., Carrondo M.A. Ab initio structure solution of a dimeric cytochrome c3 from Desulfovibrio gigas containing disulfide bridges (англ.) // J. Biol. Inorg. Chem.[англ.] : journal. — 1999. — April (vol. 4, no. 2). — P. 162—165. — doi:10.1007/s007750050299. — PMID 10499086. Архивировано 15 октября 2000 года.
- ↑ Hope A.B. Electron transfers amongst cytochrome f, plastocyanin and photosystem I: kinetics and mechanisms (англ.) // Biochim. Biophys. Acta[англ.] : journal. — 2000. — January (vol. 1456, no. 1). — P. 5—26. — doi:10.1016/S0005-2728(99)00101-2. — PMID 10611452. Архивировано 30 августа 2017 года.
- ↑ Zhang L1, McSpadden B., Pakrasi H.B., Whitmarsh J. Copper-mediated regulation of cytochrome c553 and plastocyanin in the cyanobacterium Synechocystis 6803 (англ.) // The journal of biological chemistry : journal. — 1992. — September (vol. 267, no. 27). — P. 19054—19059. — PMID 1326543. Архивировано 9 сентября 2017 года.
- ↑ 1 2 Rutherford A.W., Heathcote P. Primary Photochemistry in Photosystem-I (англ.) // Drugs[англ.]. — Adis International, 1985. — Vol. 6, no. 4. — P. 295—316. — doi:10.1007/BF00054105.
- ↑ 1 2 Zeiger, Eduardo; Taiz, Lincoln. Ch. 7: Topic 7.8: Photosystem I // Plant physiology (неопр.). — 4th. — Sunderland, Mass: Sinauer Associates[англ.], 2006. — ISBN 0-87893-856-7.
- ↑ Shubin V.V., Karapetyan N.V., Krasnovsky A.A. Molecular Arrangement of Pigment-Protein Complex of Photosystem I (англ.) // Drugs[англ.] : journal. — Adis International, 1986. — Vol. 9, no. 1—2. — P. 3—12. — doi:10.1007/BF00029726.
- ↑ 1 2 Itoh, Shigeru, Msayo Iwaki. Vitamin K1 (Phylloquinone) Restores the Turnover of FeS centers of Ether-extracted Spinach PS I Particles (англ.) // FEBS Lett.[англ.] : journal. — 1989. — Vol. 243, no. 1. — P. 47—52. — doi:10.1016/0014-5793(89)81215-3.
- ↑ Palace G.P., Franke J.E., Warden J.T. Is phylloquinone an obligate electron carrier in photosystem I? (англ.) // FEBS Lett.[англ.] : journal. — 1987. — May (vol. 215, no. 1). — P. 58—62. — doi:10.1016/0014-5793(87)80113-8. — PMID 3552735. Архивировано 4 мая 2019 года.
- ↑ 1 2 3 4 Vassiliev I.R., Antonkine M.L., Golbeck J.H. Iron-sulfur clusters in type I reaction centers (англ.) // Biochim. Biophys. Acta[англ.] : journal. — 2001. — October (vol. 1507, no. 1—3). — P. 139—160. — doi:10.1016/S0005-2728(01)00197-9. — PMID 11687212. Архивировано 22 января 2019 года.
- ↑ 1 2 Forti, Georgio, Paola Maria Giovanna Grubas. Two Sites of Interaction of Ferredoxin with thylakoids (англ.) // FEBS Lett.[англ.] : journal. — 1985. — Vol. 186, no. 2. — P. 149—152. — doi:10.1016/0014-5793(85)80698-0.
- ↑ «The Photosynthetic Process» Архивированная копия. Дата обращения: 5 мая 2009. Архивировано 19 февраля 2009 года.
- ↑ Robert Lucinski, Volkmar H.R. Schmid, Stefan Jansson, Frank Klimmek. Lhca5 interaction with plant photosystem I (англ.) // FEBS letters[англ.] : journal. — 2006. — Vol. 580, no. 27. — P. 6485—6488. — doi:10.1016/j.febslet.2006.10.063. Архивировано 24 сентября 2015 года.
- ↑ 1 2 Lianwei Peng, Hiroshi Yamamoto, Toshiharu Shikanai. Structure and biogenesis of the chloroplast NAD(P)H dehydrogenase complex (англ.) // Biochimica et Biophysica Acta (BBA) : journal. — 2011. — Vol. 1807, no. 8. — P. 945—953. — doi:10.1016/j.bbabio.2010.10.015. Архивировано 6 мая 2022 года.
- ↑ Кренделева Т. Е., Кукарских Г. П., Тимофеев К. Н., Иванов Б. Н., Рубин А. Б. Ферредоксинзависимый циклический транспорт электронов в изолированных тилакоидах протекает с участием ферредоксин-НАДФ-редуктазы. Доклады академии наук, 2001. 379(5): с. 1-4.
- ↑ Коваленко И.Б., Устинин Д.М., Грачев Н.Е., Кренделева Т.Е., Кукарских Г.П., Тимофеев К.Н., Ризниченко Г.Ю., Грачев Е.А., Рубин А.Б. Экспериментальное и теоретическое исследование процессов циклического электронного транспорта вокруг фотосистемы 1 // Биофизика : журнал. — 2003. — Т. 48, № 4. — С. 656—665. Архивировано 2 апреля 2015 года.
- ↑ Cramer WA.; Zhang H.; Yan j.; Kurisu G.; Smith JL. Transmembrane traffic in the cytochrome b6f complex (англ.) // Annu Rev Biochem[англ.] : journal. — 2006. — Vol. 75. — P. 769—790. — doi:10.1146/annurev.biochem.75.103004.142756. — PMID 16756511.
- ↑ Cramer WA.; Yan J.; Zhang H.; Kurisu G.; Smith JL. Structure of the cytochrome b6f complex: new prosthetic groups, Q-space, and the 'hors d'oeuvres hypothesis' for assembly of the complex (англ.) // Photosynth Res : journal. — 2005. — Vol. 85, no. 1. — P. 133—143. — doi:10.1007/s11120-004-2149-5. — PMID 15977064.
- ↑ Masakazu Iwai, Kenji Takizawa, Ryutaro Tokutsu, Akira Okamuro, Yuichiro Takahashi & Jun Minagawa. Isolation of the elusive supercomplex that drives cyclic electron flow in photosynthesis (англ.) // Nature : journal. — 2010. — 22 April (vol. 464). — P. 1210—1213. — doi:10.1038/nature08885.
- ↑ Hiroko Takahashi, Sophie Clowez, Francis-André Wollman, Olivier Vallon & Fabrice Rappaport. Cyclic electron flow is redox-controlled but independent of state transition (англ.) // Nature Communications : journal. — Nature Publishing Group, 2013. — 13 June (vol. 4). — doi:10.1038/ncomms2954.
- ↑ Lianwei Peng, Hideyuki Shimizu, Toshiharu Shikanai,. The Chloroplast NAD(P)H Dehydrogenase Complex Interacts with Photosystem I in Arabidopsis (англ.) // J Biol Chem. : journal. — 2008. — Vol. 283, no. 50. — P. 34873—34879.. — doi:10.1074/jbc.M803207200. Архивировано 9 сентября 2017 года.
- ↑ Yamori W., Sakata N., Suzuki Y., Shikanai T., Makino A. Cyclic electron flow around photosystem I via chloroplast NAD(P)H dehydrogenase (NDH) complex performs a significant physiological role during photosynthesis and plant growth at low temperature in rice (англ.) // Plant J.[англ.] : journal. — 2011. — Vol. 68, no. 6. — P. 966—976. — doi:10.1111/j.1365-313X.2011.04747.x. Архивировано 29 декабря 2014 года.
- ↑ Chaddock, A.M.; Mant, A.; Karnauchov, I.; Brink, S.; Herrmann, R.G.; Klösgen, R.B.; Robinson, C. A new type of signal peptide: central role of a twin-arginine motif in transfer signals for the delta pH-dependent thylakoidal protein translocase (англ.) // EMBO J. : journal. — 1995. — Vol. 14, no. 12. — P. 2715—2722. — PMID 7796800. — PMC 398390. Архивировано 22 января 2022 года.
- ↑ Kenneth Cline and Hiroki Mori. Thylakoid ΔpH-dependent precursor proteins bind to a cpTatC–Hcf106 complex before Tha4-dependent transport (англ.) // J Cell Biol.[англ.] : journal. — 2001. — 20 August (vol. 154, no. 4). — P. 719—730. — doi:10.1083/jcb.200105149. Архивировано 18 июля 2015 года.
- ↑ McDonald A.E., Ivanov A.G., Bode R., Maxwell D.P., Rodermel S.R., Hüner N.P. Flexibility in photosynthetic electron transport: the physiological role of plastoquinol terminal oxidase (PTOX) (англ.) // Biochim. Biophys. Acta[англ.] : journal. — 2011. — August (vol. 1807, no. 8). — P. 954—967. — doi:10.1016/j.bbabio.2010.10.024. — PMID 21056542. Архивировано 24 сентября 2015 года.
- ↑ Ермаков, 2005, с. 123.
- ↑ Navassard V. Karapetyan, Alfred R. Holzwarth, Matthias Rögner. The photosystem I trimer of cyanobacteria: molecular organization, excitation dynamics and physiological significance (англ.) // FEBS letters[англ.] : journal. — 1999. — Vol. 460, no. 3. — P. 395—400. — doi:10.1016/S0014-5793(99)01352-6. Архивировано 20 января 2022 года.
- ↑ Adam Ben-Shema, Felix Frolowb, Nathan Nelsona,. Evolution of photosystem I – from symmetry through pseudosymmetry to asymmetry (англ.) // FEBS letters[англ.] : journal. — 30 April 2004. — Vol. 565, no. 3. — P. 274—280. — doi:10.1016/S0014-5793(04)00360-6.
- ↑ Boudreau E., Takahashi Y., Lemieux C., Turmel M., Rochaix J.D. The chloroplast ycf3 and ycf4 open reading frames of Chlamydomonas reinhardtii are required for the accumulation of the photosystem I complex (англ.) // EMBO J : journal. — 1997. — Vol. 16, no. 20. — P. 6095—6104. — doi:10.1093/emboj/16.20.6095. — PMID 9321389. — PMC 1326293. Архивировано 7 марта 2016 года.
- ↑ 1 2 3 4 5 Lockau, Wolfgang, Wolfgang Nitschke. Photosystem I and its Bacterial Counterparts (англ.) // Physiologia Plantarum[англ.] : journal. — 1993. — Vol. 88, no. 2. — P. 372—381. — doi:10.1111/j.1399-3054.1993.tb05512.x.
Литература
[править | править код]- Зитте П. и др. Ботаника / Под ред. В. В. Чуба. — 35-е изд. — М.: Академия, 2008. — Т. 2. Физиология растений. — 495 с.
- Медведев С. С. Физиология растений. — СПб.: БХВ-Петербург, 2013. — 335 с.
- Физиология растений / Под ред. И. П. Ермакова. — М.: Академия, 2005. — 634 с.
- Хелдт Г. В. Биохимия растений. — М.: БИНОМ. Лаборатория знаний, 2011. — 471 с.
Ссылки
[править | править код]- Информационная система «Фотосинтетическая мембрана»
- «Циклический и нециклический поток электронов.» в онлайн энциклопедии Физиология растений
Эта статья входит в число хороших статей русскоязычного раздела Википедии. |