Этилбензол: различия между версиями
| [непроверенная версия] | [отпатрулированная версия] |
Метки: отменено с мобильного устройства из мобильной версии |
Hwem (обсуждение | вклад) отмена правки 111334457 участника 109.173.62.37 (обс.) Метка: отмена |
||
| Строка 16: | Строка 16: | ||
Бесцветная жидкость с запахом, напоминающим [[бензин]]; почти нерастворим в воде, растворяется в [[этанол|спирте]], [[бензол]]е, [[диэтиловый эфир|эфире]], [[четыреххлористый углерод|четыреххлористом углероде]]. |
Бесцветная жидкость с запахом, напоминающим [[бензин]]; почти нерастворим в воде, растворяется в [[этанол|спирте]], [[бензол]]е, [[диэтиловый эфир|эфире]], [[четыреххлористый углерод|четыреххлористом углероде]]. |
||
| ⚫ | |||
== Нахождение в природе == |
|||
Этилбензол содержится в [[нефть|нефти]] и [[каменноугольная смола|каменноугольной смоле]]. |
Этилбензол содержится в [[нефть|нефти]] и [[каменноугольная смола|каменноугольной смоле]]. В промышленности получают главным образом из [[бензол]]а и [[Хлорэтан|хлористого этила]] (по [[реакция Фриделя — Крафтса|реакции Фриделя — Крафтса]]). Второй по значимости метод — выделение из С8-фракции продуктов [[каталитический риформинг|риформинга]] на [[НПЗ]] топливно-нефтехимического профиля. |
||
| ⚫ | |||
В промышленности получают главным образом из [[бензол]]а и [[Хлорэтан|хлористого этила]] (по [[реакция Фриделя — Крафтса|реакции Фриделя — Крафтса]]). Второй по значимости метод — выделение из С8-фракции продуктов [[каталитический риформинг|риформинга]] на [[НПЗ]] топливно-нефтехимического профиля. |
|||
== Применение == |
== Применение == |
||
Версия от 11:42, 8 июля 2021
| Этилбензол | |||
|---|---|---|---|
 | |||
| Общие | |||
| Хим. формула | C8H10 | ||
| Физические свойства | |||
| Молярная масса | 106.167 г/моль | ||
| Плотность | 0.8665 г/см³ | ||
| Энергия ионизации | 8,76 ± 0,01 эВ[1] и 8,77 эВ[2] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -95 °C | ||
| • кипения | 136 °C | ||
| • вспышки | 55 ± 1 ℉[1] | ||
| Пределы взрываемости | 0,8 ± 0,1 об.%[1] | ||
| Теплопроводность | 1,726 Вт/(м·K) | ||
| Давление пара | 7 ± 1 мм рт.ст.[1] | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 0.15 г/100 мл | ||
| Оптические свойства | |||
| Показатель преломления | 1,495 | ||
| Структура | |||
| Дипольный момент | 2,0E−30 Кл·м[2] | ||
| Классификация | |||
| Рег. номер CAS | 100-41-4 | ||
| PubChem | 7500 | ||
| Рег. номер EINECS | 202-849-4 | ||
| SMILES | |||
| InChI | |||
| RTECS | DA0700000 | ||
| ChEBI | 16101 | ||
| ChemSpider | 7219 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
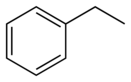
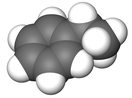
Этилбензо́л — органическое вещество класса углеводородов.
Свойства
Бесцветная жидкость с запахом, напоминающим бензин; почти нерастворим в воде, растворяется в спирте, бензоле, эфире, четыреххлористом углероде.
Получение
Этилбензол содержится в нефти и каменноугольной смоле. В промышленности получают главным образом из бензола и хлористого этила (по реакции Фриделя — Крафтса). Второй по значимости метод — выделение из С8-фракции продуктов риформинга на НПЗ топливно-нефтехимического профиля.
Применение
При пропускании паров этилбензола над катализаторами образуется стирол, являющийся сырьём при производстве важных промышленных продуктов — некоторых видов пластмасс (см. Полистирол) и синтетических каучуков. Этилбензол используют также в органическом синтезе, например для получения ацетофенона жидкофазным каталитическим окислением, как растворитель и компонент высокооктановых бензинов.
Токсичность
Предельно допустимая концентрация паров этилбензола в атмосферном воздухе ПДКм.р. = 0,02 мг/м³, максимально разовая ПДК в воздухе рабочей зоны производственных помещений ПДКм.р. =150,0 мг/м³; среднесменная ПДКс.см. =50,0 мг/м³
При вдыхании паров этилбензола человек начинает чувствовать сонливость, усталость, головную боль. Появляются неприятные ощущения в носу, горле и животе, слезятся глаза, затрудняется дыхание. Этилбензол пагубно воздействует на работу и координацию мышц. При длительном воздействии на организм человека этилбензол провоцирует хронические заболевания крови и печени.
См. также
Примечания
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0264.html
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
Для улучшения этой статьи желательно:
|
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |