Хлорноватая кислота: различия между версиями
| [непроверенная версия] | [непроверенная версия] |
хим. свойство. |
|||
| Строка 36: | Строка 36: | ||
В 40%-ной хлорноватой кислоте воспламеняется бумага. |
В 40%-ной хлорноватой кислоте воспламеняется бумага. |
||
В концентрированном растворе разлагается, продукты разложения зависят от температуры процесса{{sfn|Лидин|2000|с=259|name=Лидин}}: |
|||
:: <math>\mathsf{6HClO_3 \xrightarrow{40-60^oC}\ 4ClO_2 + Cl_2O_7 + 3H_2O}</math> |
|||
:: <math>\mathsf{3HClO_3 \xrightarrow{100^oC}\ HClO_4 + Cl_2\uparrow + 2O_2\uparrow + H_2O}</math> |
|||
== Получение == |
== Получение == |
||
| Строка 48: | Строка 52: | ||
Многие хлораты [[яд]]овиты. |
Многие хлораты [[яд]]овиты. |
||
== Примечания == |
|||
{{примечания}} |
|||
== Литература == |
== Литература == |
||
* {{книга |автор = Зефиров Н.С. и др.|часть = т.5 Три-Ятр|заглавие = Химическая энциклопедия|оригинал = |ссылка = |ответственный = |издание = |место = М.|издательство = Большая Российская Энциклопедия|год = 1998|том = |страницы = |страниц = 783|серия = |isbn = 5-85270-310-9|тираж = }} |
* {{книга |автор = Зефиров Н.С. и др.|часть = т.5 Три-Ятр|заглавие = Химическая энциклопедия|оригинал = |ссылка = |ответственный = |издание = |место = М.|издательство = Большая Российская Энциклопедия|год = 1998|том = |страницы = |страниц = 783|серия = |isbn = 5-85270-310-9|тираж = }} |
||
* {{книга|ref=Лидин|автор=Лидин Р. А. и др.|заглавие=Химические свойства неорганических веществ: Учеб. пособие для вузов|издание=3-е изд., испр|место=М.|издательство=Химия|год=2000|страниц=480|isbn=5-7245-1163-0}} |
|||
{{Хлорсодержащие неорганические кислоты}} |
{{Хлорсодержащие неорганические кислоты}} |
||
Версия от 18:05, 14 декабря 2022
| Хлорноватая кислота | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
Хлорноватая кислота | ||
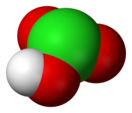
| Хим. формула | HClO3 | ||
| Физические свойства | |||
| Состояние | Бесцветный раствор | ||
| Молярная масса | 84.46 г/моль | ||
| Плотность | 1,282 г/мл | ||
| Химические свойства | |||
| Константа диссоциации кислоты | ~ −1 | ||
| Растворимость | |||
| • в воде | >40 (20 °C) | ||
| Классификация | |||
| Рег. номер CAS | [7790-93-4] | ||
| PubChem | 19654 | ||
| Рег. номер EINECS | 232-233-0 | ||
| SMILES | |||
| InChI | |||
| RTECS | CN9750000 | ||
| ChEBI | 17322 | ||
| ChemSpider | 18513 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Хлорноватая кислота — HClO3, сильная одноосновная кислота, в которой хлор имеет степень окисления +5. В свободном виде не получена; в водных растворах при концентрации ниже 30 % на холоде довольно устойчива; в более концентрированных растворах распадается:
Разложение при хранении:
Химические свойства
Хлорноватая кислота — сильный окислитель; окислительная способность увеличивается с возрастанием концентрации и температуры. HClO3 легко восстанавливается до соляной кислоты:
В слабокислой среде HClO3 восстанавливается сернистой кислотой H2SO3 до Cl−, но при пропускании смеси SO2 и воздуха сквозь сильнокислый раствор, образуется диоксид хлора:
В 40%-ной хлорноватой кислоте воспламеняется бумага.
В концентрированном растворе разлагается, продукты разложения зависят от температуры процесса[1]:
Получение
Хлорноватая кислота образуется при разложении хлорноватистой кислоты, при электролизе растворов хлоридов; в лабораторных условиях получают при взаимодействии хлората бария с разбавленной серной кислотой:
Хлораты
Хлорноватой кислоте соответствуют соли — хлораты; из них наибольшее значение имеют хлораты натрия, калия, кальция и магния.
Соли хлорноватой кислоты (хлораты) — сильные окислители, в смеси с восстановителями взрывоопасны.
Многие хлораты ядовиты.
Примечания
- ↑ Лидин, 2000, с. 259.
Литература
- Зефиров Н.С. и др. т.5 Три-Ятр // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1998. — 783 с. — ISBN 5-85270-310-9.
- Лидин Р. А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.