Луразидон: различия между версиями
| [непроверенная версия] | [непроверенная версия] |
Луговкин (обсуждение | вклад) |
Нет описания правки |
||
| Строка 19: | Строка 19: | ||
| ATC = {{АТХ|N05|AE05}} |
| ATC = {{АТХ|N05|AE05}} |
||
}} |
}} |
||
'''Луразидон''' (Латуда; DSP-1349M; SM-13496; SMP-13496) — [[Атипичные антипсихотики|атипичный антипсихотик]], одобренный для лечения [[Шизофрения|шизофрении]] и [[Биполярная депрессия|биполярного расстройства]]. Луразидон был синтезирован и разработан компаниями [[Dainippon Sumitomo Pharma]] и [[:en:Sunovion#:~:text=Sunovion Pharmaceuticals Inc. (former NASDAQ:,Ontario, and Teaneck, New Jersey|Sunovion Pharmaceuticals]] благодаря химическому объединению структуры ядра молекул антипсихотиков ряда «-донов» ([[рисперидон]], [[зипрасидон]] и др.) и [[Антидепрессанты|антидепрессанта]]-[[анксиолитик]]а тандоспирона с целью усиления их [[Антидепрессанты|антидепрессивных]] и прокогнитивных свойств за счёт повышения [[Аффинитет|афинности]] к [[Серотониновые рецепторы|серотониновым рецепторам]] [[5-HT7-рецептор|5-HT7]] и [[5-HT1A-рецептор|5-HT1А]] типов и исключения из фармакодинамического профиля взаимодействия с нежелательными мишенями, ответственными за развитие целого ряда [[Побочные эффекты|побочных эффектов]]<ref>{{Cite web|url=https://adisinsight.springer.com/drugs/800007206|title=Lurasidone - Sumitomo Dainippon Pharma - AdisInsight|website=adisinsight.springer.com|access-date=2021-11-25|archive-date=2021-11-25|archive-url=https://web.archive.org/web/20211125145802/https://adisinsight.springer.com/drugs/800007206|deadlink=no}}</ref><ref>{{Статья|ссылка=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3171824/|автор=Martin P. Cruz|заглавие=Lurasidone HCl (Latuda), an Oral, Once-Daily Atypical Antipsychotic Agent for the Treatment of Patients with Schizophrenia|год=2011-8|издание=Pharmacy and Therapeutics|том=36|выпуск=8|страницы=489–492|issn=1052-1372}}</ref><ref>{{Книга|ссылка=https://www.worldcat.org/oclc/810409752|автор=Stephen M. Stahl|заглавие=Stahl's essential psychopharmacology : neuroscientific basis and practical application|год=2013|издание=Fourth edition|место=Cambridge|страниц=xv, 608 pages|isbn=978-1-107-02598-1, 1-107-02598-2, 978-1-107-68646-5, 1-107-68646-6, 978-0-521-85702-4, 0-521-85702-3}}</ref><ref name=":0">{{Статья|автор=Беккер РА, Быков ЮВ.|заглавие=Эффективность и безопасность антипсихотика III поколения луразидона (Латуда) при шизофрении и биполярных депрессиях (обзор литературы с комментариями).|год=|язык=русский|издание=Психиатрия и психофармакотерапия им. П.Б. Ганнушкина №04 2019}}</ref>. Луразидон был одобрен в [[Соединённые Штаты Америки|США]] для лечения шизофрении у взрослых и подростков с 13 лет в октябре 2010 года, а также [[Депрессивный эпизод|депрессивных эпизодов]] при [[Биполярное аффективное расстройство|биполярном аффективном расстройстве]] I типа у взрослых и детей с 10 лет в июне 2013 года<ref>{{Cite web|url=http://www.latuda. com/LatudaPrescribingInformation.pdf|title=Latuda (lurasidone HCl). Tablets US prescribing information}}</ref><ref>{{Статья|ссылка=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4382136/|автор=Radhika Bawa, Jonathan R. Scarff|заглавие=Lurasidone: A New Treatment Option for Bipolar Depression—A Review|год=2015|издание=Innovations in Clinical Neuroscience|том=12|выпуск=1—2|страницы=21–23|issn=2158-8333|archivedate=2020-11-11|archiveurl=https://web.archive.org/web/20201111163344/https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4382136/}}</ref>. В [[Россия|Российской Федерации]] Латуда зарегистрирована в августе 2016 года и одобрена для лечения шизофрении у взрослых и подростков с 13 лет и депрессии при биполярном аффективном расстройстве I типа у взрослых и детей с 10 лет в монотерапии, а также для [[Адъювант|адъювантной терапии]] в сочетании с [[Препараты лития|литием]] или [[Вальпроаты|вальпроатами]] у взрослых<ref name=":1">{{Cite web|url=https://grls.rosminzdrav.ru/grls.aspx?s=%D0%BB%D0%B0%D1%82%D1%83%D0%B4%D0%B0&m=tn|title=Государственный реестр лекарственных средств|website=grls.rosminzdrav.ru|access-date=2021-11-25|archive-date=2021-11-25|archive-url=https://web.archive.org/web/20211125145755/https://grls.rosminzdrav.ru/grls.aspx?s=%D0%BB%D0%B0%D1%82%D1%83%D0%B4%D0%B0&m=tn|deadlink=no}}</ref>. |
'''Луразидон''' (Латуда; DSP-1349M; SM-13496; SMP-13496) — [[Атипичные антипсихотики|атипичный антипсихотик]], одобренный для лечения [[Шизофрения|шизофрении]] и [[Биполярная депрессия|биполярного расстройства]]. Луразидон был синтезирован и разработан компаниями [[Dainippon Sumitomo Pharma]] и [[:en:Sunovion#:~:text=Sunovion Pharmaceuticals Inc. (former NASDAQ:,Ontario, and Teaneck, New Jersey|Sunovion Pharmaceuticals]] благодаря химическому объединению структуры ядра молекул антипсихотиков ряда «-донов» ([[рисперидон]], [[зипрасидон]] и др.) и [[Антидепрессанты|антидепрессанта]]-[[анксиолитик]]а тандоспирона с целью усиления их [[Антидепрессанты|антидепрессивных]] и прокогнитивных свойств за счёт повышения [[Аффинитет|афинности]] к [[Серотониновые рецепторы|серотониновым рецепторам]] [[5-HT7-рецептор|5-HT7]] и [[5-HT1A-рецептор|5-HT1А]] типов и исключения из фармакодинамического профиля взаимодействия с нежелательными мишенями, ответственными за развитие целого ряда [[Побочные эффекты|побочных эффектов]]<ref>{{Cite web|url=https://adisinsight.springer.com/drugs/800007206|title=Lurasidone - Sumitomo Dainippon Pharma - AdisInsight|website=adisinsight.springer.com|access-date=2021-11-25|archive-date=2021-11-25|archive-url=https://web.archive.org/web/20211125145802/https://adisinsight.springer.com/drugs/800007206|deadlink=no}}</ref><ref>{{Статья|ссылка=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3171824/|автор=Martin P. Cruz|заглавие=Lurasidone HCl (Latuda), an Oral, Once-Daily Atypical Antipsychotic Agent for the Treatment of Patients with Schizophrenia|год=2011-8|издание=Pharmacy and Therapeutics|том=36|выпуск=8|страницы=489–492|issn=1052-1372}}</ref><ref>{{Книга|ссылка=https://www.worldcat.org/oclc/810409752|автор=Stephen M. Stahl|заглавие=Stahl's essential psychopharmacology : neuroscientific basis and practical application|год=2013|издание=Fourth edition|место=Cambridge|страниц=xv, 608 pages|isbn=978-1-107-02598-1, 1-107-02598-2, 978-1-107-68646-5, 1-107-68646-6, 978-0-521-85702-4, 0-521-85702-3}}</ref><ref name=":0">{{Статья|автор=Беккер РА, Быков ЮВ.|заглавие=Эффективность и безопасность антипсихотика III поколения луразидона (Латуда) при шизофрении и биполярных депрессиях (обзор литературы с комментариями).|год=|язык=русский|издание=Психиатрия и психофармакотерапия им. П.Б. Ганнушкина №04 2019}}</ref>. Луразидон был одобрен в [[Соединённые Штаты Америки|США]] для лечения шизофрении у взрослых и подростков с 13 лет в октябре 2010 года, а также [[Депрессивный эпизод|депрессивных эпизодов]] при [[Биполярное аффективное расстройство|биполярном аффективном расстройстве]] I типа у взрослых и детей с 10 лет в июне 2013 года<ref>{{Cite web|url=http://www.latuda. com/LatudaPrescribingInformation.pdf|title=Latuda (lurasidone HCl). Tablets US prescribing information}}</ref><ref>{{Статья|ссылка=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4382136/|автор=Radhika Bawa, Jonathan R. Scarff|заглавие=Lurasidone: A New Treatment Option for Bipolar Depression—A Review|год=2015|издание=Innovations in Clinical Neuroscience|том=12|выпуск=1—2|страницы=21–23|issn=2158-8333|archivedate=2020-11-11|archiveurl=https://web.archive.org/web/20201111163344/https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4382136/}}</ref>. В [[Россия|Российской Федерации]] Латуда зарегистрирована в августе 2016 года и одобрена для лечения шизофрении у взрослых и подростков с 13 лет и депрессии при биполярном аффективном расстройстве I типа у взрослых и детей с 10 лет в монотерапии, а также для [[Адъювант|адъювантной терапии]] в сочетании с [[Препараты лития|литием]] или [[Вальпроаты|вальпроатами]] у взрослых<ref name=":1">{{Cite web|url=https://grls.rosminzdrav.ru/grls.aspx?s=%D0%BB%D0%B0%D1%82%D1%83%D0%B4%D0%B0&m=tn|title=Государственный реестр лекарственных средств|website=grls.rosminzdrav.ru|access-date=2021-11-25|archive-date=2021-11-25|archive-url=https://web.archive.org/web/20211125145755/https://grls.rosminzdrav.ru/grls.aspx?s=%D0%BB%D0%B0%D1%82%D1%83%D0%B4%D0%B0&m=tn|deadlink=no}}</ref>. |
||
== Клиническая эффективность == |
== Клиническая эффективность == |
||
Версия от 15:07, 24 декабря 2024
Статья содержит ошибки и/или опечатки. |
Эту статью необходимо исправить в соответствии с правилом Википедии об оформлении статей. |
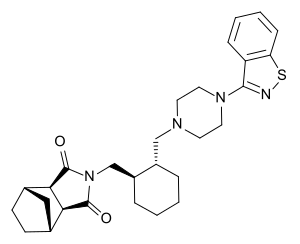
| Луразидон | |
|---|---|
| Lurasidonum | |
 | |
| Химическое соединение | |
| ИЮПАК | N-[4-[4-(1,2-бензизотиазол-3-ил)-1-пиперазинил]-(2R,3R)-2,3-тетраметилен-бутил]-(1'R,2'S,3'R,4'S)-2,3-бицикло[2,2,1]гептандикарбоксиимида гидрохлорид |
| Брутто-формула | C28H36N4O2S |
| Молярная масса | 492,67604 г/моль |
| CAS | 367514-87-2 |
| PubChem | 213046 |
| DrugBank | DB08815 |
| Состав | |
| Классификация | |
| АТХ | N05AE05 |
| Фармакокинетика | |
| Биодоступн. | 10-20% |
| Метаболизм | CYP3A4 |
| Период полувывед. | 20-40 часов |
| Лекарственные формы | |
| таблетки по 20, 40 и 80 мг | |
| Способы введения | |
| пероральный | |
| Другие названия | |
| «Латуда» | |
Луразидон (Латуда; DSP-1349M; SM-13496; SMP-13496) — атипичный антипсихотик, одобренный для лечения шизофрении и биполярного расстройства. Луразидон был синтезирован и разработан компаниями Dainippon Sumitomo Pharma и Sunovion Pharmaceuticals благодаря химическому объединению структуры ядра молекул антипсихотиков ряда «-донов» (рисперидон, зипрасидон и др.) и антидепрессанта-анксиолитика тандоспирона с целью усиления их антидепрессивных и прокогнитивных свойств за счёт повышения афинности к серотониновым рецепторам 5-HT7 и 5-HT1А типов и исключения из фармакодинамического профиля взаимодействия с нежелательными мишенями, ответственными за развитие целого ряда побочных эффектов[1][2][3][4]. Луразидон был одобрен в США для лечения шизофрении у взрослых и подростков с 13 лет в октябре 2010 года, а также депрессивных эпизодов при биполярном аффективном расстройстве I типа у взрослых и детей с 10 лет в июне 2013 года[5][6]. В Российской Федерации Латуда зарегистрирована в августе 2016 года и одобрена для лечения шизофрении у взрослых и подростков с 13 лет и депрессии при биполярном аффективном расстройстве I типа у взрослых и детей с 10 лет в монотерапии, а также для адъювантной терапии в сочетании с литием или вальпроатами у взрослых[7].
Клиническая эффективность
Луразидон исследован в обширной клинической программе, включавшей исследования как краткосрочной, так и долгосрочной противорецидивной эффективности при шизофрении и депрессивных эпизодах, обусловленных биполярным аффективным расстройством I типа в качестве монотерапии и дополнительной терапии с препаратами лития или вальпроевой кислоты[8] (стабилизаторы настроения).
Шизофрения
Эффективность луразидона для лечения острого рецидива шизофрении была продемонстрирована в ходе пяти многоцентровых, плацебо-контролируемых, двойных слепых 6-недельных клинических исследований (КИ) в дозах 40-160 мг в сутки. В них основной показатель эффективности определялся как среднее изменение суммы баллов к 6-й неделе терапии, относительно исходного значения по оценке с помощью шкалы позитивных и негативных синдромов (PANSS)[9][10][11][12][13]. Статистически значимые отличия от плацебо были зарегистрированы уже на 4-й день терапии[7]. Кроме того, луразидон превосходил плацебо по заранее определённому вторичному показателю эффективности — показателю шкалы общего клинического впечатления о тяжести заболевания (CGI-S)[7]. В двух из пяти краткосрочных исследованиях для оценки чувствительности в одной из параллельных с луразидоном и плацебо групп использовались оланзапин и кветиапин типа XR. Оба препарата продемонстрировали значительное преимущество перед плацебо, но не перед луразидоном, то есть по результатам рандомизированного контролируемого испытания (РКИ) луразидон показал одинаковую эффективность как в сочетании с оланзапином, так и в сочетании с кветиапином XR в терапии острого рецидива психотической симптоматики шизофрении[10][13]. Кроме того, краткосрочная эффективность луразидона при лечении шизофрении оценивалась в ходе нескольких объединённых анализов данных вышеупомянутых 6-недельных исследований. Так, объединённый анализ пяти РКИ (n = 1029) с использованием пятифакторной модели шкалы PANSS показал, что луразидон в фиксированных дозах 40-160 мг в сутки статистически достоверно улучшал к 6-й неделе терапии как общий балл шкалы PANSS (p < 0,001; величина эффекта — 0,45), так и показатели позитивной, негативной симптоматики шизофрении, нарушения мышления, агрессивности/возбуждения, а также депрессии/тревоги[14].
Симптомы депрессии широко распространены при шизофрении, и их наличие может ухудшить клинические результаты. В ходе краткосрочных исследований применялась шкала Монтгомери-Асберг для оценки депрессии (MADRS). Объединённый анализ четырёх рандомизированных плацебо-контролируемых 6-недельных КИ у пациентов с шизофренией (n = 1330) показал, что луразидон является эффективным антидепрессантом у пациентов с депрессивными симптомами, ассоциированными с шизофренией: лечение луразидоном приводило к статистически достоверному улучшению депрессивной симптоматики в сравнении с плацебо. Среднее изменение балла шкалы MADRS составило −2,8 в группе луразидона и −1,4 в группе плацебо (p < 0,001; величина эффекта — 0,24)[15].
Долгосрочная эффективность препарата изучалась в двойном-слепом РКИ, где луразидон продемонстрировал более высокие показатели ремиссии и меньший риск госпитализации в сравнении с кветиапином XR[16]. Оценка вероятности госпитализации по Каплану-Мейеру к 12 месяцу была статистически достоверно ниже у пациентов в группе луразидона (9,8 %) в сравнении с группой кветиапина XR (23,1 %; p < 0,05). 12 месяцев лечения луразидоном было связано с 56,7 % сокращением риска госпитализации в сравнении с кветиапином XR. Отмечалось статистически достоверно большее изменение общего балла PANSS (-34,6; p < 0,01 от исходного уровня острой фазы исследования и −5,0; p < 0,01 от исходного уровня расширенной 12-месячной фазы) и субшкалы позитивных симптомов PANSS (-12,3; p < 0,01 от исходного уровня острой фазы исследования и −1,5; p < 0,01 от исходного уровня расширенной 12-месячной фазы) в группе луразидона в сравнении с группой кветиапина XR. Помимо этого, было обнаружено и статистически достоверное превосходство луразидона над кветиапином XR по оценке изменений по шкале MADRS от исходного уровня острой фазы РКИ до финальной оценки по завершении расширенной 12-месячной фазы (-6,0 против −3,8; p < 0,05)[16].
Кроме клинического состояния, чрезвычайно важным при длительной поддерживающей терапии шизофрении является уровень социального функционирования, и оказывающий на него наибольшее влияние когнитивный статус пациентов. В одном из двойных слепых рандомизированных клинических исследований[17] было показано, что изменение композитного индекса, полученного при проведении компьютеризированной нейрокогнитивной батареи тестов CogState, оказалось статистически значимо лучше при использовании луразидона в дозе 160 мг в сравнении как с группой плацебо (p = 0,038), так и с группой кветиапина XR (p = 0,018). В расширенной 12-месячной фазе этого исследования изменение композитного индекса по сравнению с его первоначальным значением было также более выражено для объединённой группы луразидона в сравнении с группой кветиапина XR как на 19-й (p = 0,05), так и на 32-й неделях терапии (p = 0,008). В проведённом ретроспективном анализе этого исследования улучшение когнитивного функционирования по композитному нейрокогнитивному Z-баллу было достоверно выше в группе пациентов, получавших луразидон в финальной дозе 120 мг в сутки (p = 0,02) и 160 мг в сутки (p = 0,05)[18].
Шизофрения у подростков
Луразидон также может быть эффективен при лечении шизофрении у подростков с 13 лет. Так, в двойном слепом плацебо-контролируемом РКИ луразидон в дозах 40 и 80 мг в сутки показал статистически достоверное и клинически значимое улучшение позитивной, негативной, когнитивной и аффективной симптоматик шизофрении по шкале PANSS, по сравнению с плацебо[19]. Кроме того, на основании двухлетнего открытого расширенного исследования при более длительном лечении продолжает наблюдаться постоянное улучшение состояния пациентов[20]. Луразидон хорошо переносится и имеет минимальное влияние на аппетит, массу тела и метаболические параметры. Это особенно важно при лечении подростков, в связи с их эндокринной неустойчивостью и особой повышенной чувствительностью к метаболическим ПЭ при применении АП[19][20].
Биполярное аффективное расстройство
В рандомизированном двойном слепом плацебо-контролируемом исследовании монотерапии с применением луразидона депрессии в рамках БАР I типа пациенты получали лечение луразидоном (20-60 мг в сутки [n = 166] или 80-120 мг в сутки [n = 169]) или плацебо (n = 170) в течение 6 недель. Оценка проводилась по шкалам MADRS и CGI-BP. Луразидон значительно снижал средние общие баллы по шкале MADRS на 6-й неделе как в группе 20-60 мг в сутки (-15,4; величина эффекта = 0,51), так и в группе 80-120 мг в сутки (-15,4; величина эффекта = 0,51) по сравнению с плацебо (-10,7). Точно так же лечение луразидоном привело к значительно большему снижению тяжести депрессии по шкале CGI-BP как для группы 20-60 мг в сутки (-1,8; величина эффекта = 0,61), так и для группы 80-120 мг в сутки (-1,7; величина эффекта = 0,50) по сравнению с плацебо (-1,1). Обе группы луразидона также продемонстрировали значительное улучшение симптомов тревоги. Частота прекращения приёма из-за побочных эффектов была аналогичной в группах 20-60 мг в сутки (6,6 %), 80-120 мг в сутки (5,9 %) и плацебо (6,5 %)[21].
В одном исследовании оценивали эффективность луразидона, в качестве дополнительной терапии литием или вальпроатом при биполярной депрессии I типа. Пациенты были рандомизированы в группу луразидона (N = 183) или плацебо (N = 165), добавленным к терапевтическим уровням лития или вальпроата. Динамика депрессивной симптоматики оценивалась по шкалам MADRS и CGI-BP. Лечение луразидоном значительно снизило средний общий балл по шкале MADRS на 6-й неделе по сравнению с группой плацебо (-17,1 против −13,5; величина эффекта = 0,34). Точно так же лечение луразидоном привело к значительно большему снижению тяжести депрессии по шкале CGI-BP по сравнению с плацебо (-1,96 против −1,51; величина эффекта = 0,36), а также к значительному улучшению симптомов тревоги. Частота прекращения лечения из-за побочных эффектов составила 6,0 % и 7,9 % в группах луразидона и плацебо, соответственно[22].
Депрессия при БАР-I у детей
В недавнем исследовании[23] пациенты в возрасте 10-17 лет с биполярной депрессией I типа, завершившие 6-недельное двойное слепое исследование луразидона по сравнению с плацебо, имели право на участие в двухлетнем расширенном открытом исследовании, в котором пациенты продолжали принимать луразидон в гибких дозах (20-80 мг в сутки) или переходили с плацебо на луразидон. Показатели эффективности включали пересмотренную шкалу оценки детской депрессии (CDRS-R) и Шкалу общего клинического впечатления и тяжести биполярной депрессии (CGI-BP-S). Функционирование оценивалось с использованием шкалы глобальной оценки детей (CGAS), при этом значение более 70 баллов указывало на отсутствие клинически значимого функционального нарушения. Критерии ответа были соблюдены, если пациент достиг 50 % снижения балльной оценки от исходного уровня в двойной-слепой фазе по общему баллу CDRS-R: критерии ремиссии были соблюдены, если пациент достиг общего балла CDRS-R = 28 и общего балла YMRS = 8 и CGI-BP-S = 3, и пациент считался соответствующим критериям выздоровления, если он достиг ремиссии с показателем CGAS > 70. Кроме того, также был проанализирован более строгий результат — устойчивая ремиссия, которая требовала, чтобы пациент соответствовал критериям ремиссии в течение 24 недель подряд. В общей сложности 306 пациентов завершили двойное-слепое 6-недельное исследование и вошли в расширенное открытое исследование; 195 (63,7 %) пациентов завершили курс лечения в течение одного года, а 168 (54,9 %) пациентов завершили курс лечения в течение двух лет. Процент ответчиков на начало открытой фазы, в конце первого года и в конце второго года открытой фазы составлял: 51,0 %, 88,4 % и 91,1 % соответственно; частота ремиссии составила 24,3 %, 61,3 % и 75,6 % соответственно. Устойчивая ремиссия была достигнута у 37,2 % пациентов через год и 57 % пациентов через два года. Таким образом, у детей и подростков с биполярной депрессией при лечении луразидоном до 2 лет наблюдалось неуклонное улучшение депрессивных симптомов, что приводило к прогрессивно более высокому уровню ответа, ремиссии, выздоровления и более строго рассчитанному результату устойчивой ремиссии[23].
Побочные эффекты
Наиболее частыми побочными действиями луразидона в клинических испытаниях являлись тошнота, сонливость, экстрапирамидные расстройства (акатизия, паркинсонизм, дистония), тревога и ажитация[24], бессонница[25], седация, головная боль, головокружение, рвота[26]. Акатизия и сонливость являются дозозависимыми побочными эффектами[25]. Наблюдалось также повышение уровня глюкозы натощак[27]. По другим данным, клинически значимого изменения уровня глюкозы и липидов не наблюдалось[25][28].
Луразидон, по-видимому, может вызывать такие общие для различных антипсихотиков побочные действия, как ортостатическая гипотензия и обмороки, злокачественный нейролептический синдром, поздняя дискинезия, увеличение веса и метаболические нарушения, гиперпролактинемия и связанные с ней расстройства (нарушения репродуктивной функции, снижение плотности костной ткани и др.)[24].
Поскольку для луразидона характерно низкое или очень низкое связывание с такими «нежелательными» рецепторными мишенями, как H1 гистаминовые рецепторы, 5-HT2C серотониновые рецепторы, М-холинергические, α1 адренорецепторы, D1 и D4 дофаминовые рецепторы[29][30][31][32][33], при его приёме маловероятно развитие таких побочных эффектов, как дневная сонливость, ортостатическая гипотензия и тахикардия, Повышение аппетита, прибавка массы тела, метаболические нарушения, снижение либидо, импотенция, антихолинергические эффекты (парез аккомодации глаз, запоры, задержка мочи, сухость во рту, нарушения памяти и когнитивных функций)[4].
Влияние на массу тела
Луразидон обладает благоприятным профилем побочных эффектов с минимальным влиянием на массу тела и метаболический профиль. Так, в 12-месячном исследовании безопасности и переносимости луразидона с рисперидоном в качестве активного контроля отмечалось увеличение медианы глюкозы натощак при применении рисперидона, но не луразидона (медиана изменений уровня глюкозы (мг/дл, LOCF) для луразидона −0,5; для рисперидона 3,0; p = 0,005)[34]. Помимо этого, отмечалось сокращение средней массы тела (-0,97 ± 5,06 кг) и индекса массы тела (ИМТ) (-0.33 ± 1,71 кг/м2) у пациентов, получавших луразидон, тогда как у пациентов, получавших рисперидон, эти показатели выросли (1,47 ± 5,03 кг и 0,53 ± 1,76 кг/м2 соответственно); эта разница оказалась статистически достоверной для обоих показателей (P < 0,001 для каждого)[34]. В расширенной открытой фазе КИ с гибким дозированием (40-120 мг в сутки) лечение луразидоном было эффективным и в целом хорошо переносилось в течение 6 месяцев у пациентов, завершивших 6-недельное лечение луразидоном, оланзапином или плацебо; пациенты, изначально получавшие плацебо или луразидон, испытывали небольшое повышение веса и минимальные изменения метаболических параметров в течение последующего лечения в открытой фазе в течение 6 месяцев, тогда как у пациентов, изначально набравших вес на оланзапине, наблюдалось сокращение массы тела и улучшение уровня липидов после переключения на луразидон[35].
Влияние на пролактин
Способность повышать уровень пролактина зависит, главным образом, от способности антипсихотика проникать через ГЭБ, что определяет антипсихотическую дозу, применяемую в клинике. Низкая способность проникать через ГЭБ определяет более высокие концентрации антипсихотика на периферии. Поскольку гипофиз находится не за ГЭБ, он подвергается воздействию циркулирующих уровней антипсихотика в крови[36][37]. Ввиду высокой липофильности луразидон хорошо проникает через ГЭБ[29].
Для оценки долгосрочной безопасности луразидона у пациентов с шизофренией был проведён анализ двойного слепого сравнительного с рисперидоном исследования. Клинически стабильные взрослые амбулаторные пациенты с шизофренией были рандомизированы в соотношении 2:1 на 12 месяцев двойного слепого лечения с гибкими дозами луразидона (40-120 мг) или рисперидона (2-6 мг) один раз в сутки. Анализ уровней пролактина для пациентов мужского и женского пола показал стойкое повышение уровня пролактина для пациентов, рандомизированных в группы рисперидона, и практически отсутствие изменений для пациентов, получавших луразидон. Медианное изменение пролактина от исходного уровня у пациентов женского пола к 6 неделе терапии в группе рисперидона составило 40 нг/мл (нанограмм на миллилитр), а в группе луразидона — 0,9 нг/мл, а к концу 12 месяца — 28,4 нг/мл и 0,1 нг/мл соответственно. Таким образом, показано стойкое повышение уровня пролактина у пациентов, рандомизированных в группу рисперидона, и практически полное отсутствие изменений у пациентов, получавших луразидон[34].
Дневная сонливость
Поскольку дневная сонливость является значительным фактором риска несоблюдения режима лечения, ухудшения когнитивных функций, профессиональной состоятельности и качества жизни, для систематической оценки этого неблагоприятного эффекта использовалась проверенная Шкала сонливости Эпворта. Лечение луразидоном в дозах 80 и 160 мг в сутки не было связано с увеличением сонливости по шкале Эпворта (улучшение уровня бодрствования), тогда как лечение кветиапином было связано со значительным увеличением дневной сонливости[38]. Согласно инструкции по медицинскому применению сонливость наблюдается примерно у 10 % пациентов, что связано с сонливостью, наблюдаемой у некоторых пациентов в первые часы после приёма препарата, поэтому рекомендуемый режим дозирования предусматривает однократный вечерний приём препарата с последним приёмом пищи[7].
Удлинение интервала QT
В программе клинических исследований луразидона не наблюдалось нежелательных явлений, связанных с удлинением интервала QT. У пациентов в рамках исследований не сообщалось об удлинении интервала QT свыше 500 м/сек, не отмечалось случаев аритмии, желудочковой тахикардии, фибрилляции или трепетания желудочков, у пациентов, получавших луразидон во всех краткосрочных и долгосрочных исследованиях[39]. В специально проведённом исследовании влиянии луразидона на интервал QT с участием 73 пациентов c шизофренией или шизоаффективным расстройством, получавших луразидон 120 мг в сутки или 600 мг в сутки, ни один из пациентов не продемонстрировал удлинение интервала QT на >60 мсек от исходного уровня или продолжительности интервала QT > 480 мсек[39].
Лекарственные взаимодействия
Луразидон метаболизируется главным образом в печени через систему цитохрома CYP3A4, и его совместный приём с препаратами, которые являются сильными ингибиторами CYP3A4 (например, кетоконазол) или сильными индукторами (например, рифампицин), противопоказан[40].
Фармакодинамика
Луразидон — это селективный антагонист дофаминовых и моноаминовых рецепторов, обладающий высоким сродством к D2 дофаминовым и 5-HT2А и 5-HT7 серотониновым рецепторам (степень сродства 0,994, 0,47 и 0,495 нМ, соответственно)[7]. Среди атипичных антипсихотиков луразидон имеет самый высокий аффинитет к 5-HT7 рецепторам[41]. Луразидон также блокирует α2С и α2А адренорецепторы (степень сродства 10,8 и 40,7 нМ, соответственно), обладает частичным агонизмом к 5-HT1А серотониновым рецепторам со степенью сродства 6,38 нМ. Луразидон клинически значимо не связывается с H1 гистаминовыми и мускариновыми рецепторами[7].
Антипсихотическое и нормотимическое действие луразидона, как и других антипсихотиков, связано с блокадой D2 рецепторов дофамина. При этом луразидон обладает очень высокой селективностью именно к D2 подтипу дофаминовых рецепторов, не связываясь в применяемых дозах с D1 и D4 рецепторами[30][42][43]. Считается, что отсутствие значимого связывания луразидона с D1 и D4, блокада которых в префронтальной коре приводит к ухудшению когнитивного функционирования, лежит в основе прокогнитивного эффекта луразидона, особенно выраженного у пациентов с шизофренией[42][44]. В диапазоне однократных доз от 40 до 80 мг луразидон обеспечивает >60 % занятость D2 рецепторов в базальных ганглиях, необходимую для достижения антипсихотического действия[45]. Таким образом, минимальной антипсихотической является доза 40 мг в сутки, а доза в 20 мг в сутки обладает достоверной антидепрессивной эффективностью, по-видимому, за счёт выраженного 5-HT7-антагонизма и парциального 5-HT1А-агонизма[46].
Теоретические представления о механизме действия луразидона, лежащем в основе его выраженного прокогнитивного, антинегативного и антидепрессивного действия, связаны с представлением о его способности повышать уровень дофамина и серотонина в префронтальной коре[46]. Стимуляция 5-HT1А рецепторов на телах тормозных ГАМКергических нейронов префронтальной коры приводит к ингибированию высвобождения ГАМК и ускоряет глутаматергические пирамидные нейроны, проецирующиеся в катехоламинергические ядра ствола мозга. Это повышает возбуждающую глутаматергическую нейротрансмиссию на телах дофаминергических нейронов (VTA), что, в свою очередь, приводит к увеличению активности мезокортикального дофаминергического пути, проецирующегося в префронтальную кору[47]. 5-HT7 и 5-HT2А рецепторы — возбуждающие. В коре они также располагаются на телах тех же ГАМКергических нейронов, что и 5-HT1А (тормозные), поэтому блокада 5-HT2А и 5-HT7 рецепторов приводит функционально тем же эффектам, что и стимуляция 5-HT1А рецепторов, и синергически повышает уровень дофамина в префронтальной коре. Таким образом, стимуляция 5-HT1А рецепторов имеет однонаправленное с блокадой 5-HT2А/5-HT7 рецепторов действие[47]. Под действием луразидона быстрой десенситизации подвергаются не только 5-HT1А ауторецепторы на телах серотонинергических нейронов, но и также 5-HT7 рецепторы, расположенные на ГАМКергических нейронах ядер шва, тормозящих активность серотонинергических нейронов. Таким образом, инактивируются оба контура отрицательной обратной связи внутри DRN, что приводит к выраженному дезингибированию серотонинергической нейротрансмиссии[48].
Фармакокинетика
Луразидон следует принимать с едой. При приёме с порцией пищи не менее 350 ккал биодоступность луразидона увеличивается в 2 раза.
- Всасывание
Tmax в крови составляет от 1 до 3 ч. После приёма луразидона с пищей средняя Сmах и AUC увеличивались в 2-3 и 1,5-2 раза соответственно по сравнению со значениями после приёма луразидона натощак.
- Распределение
После приёма внутрь 40 мг луразидона средний кажущийся Vd составлял приблизительно 6000 л. Луразидон значительно (на 99 %) связывается белками плазмы крови.
- Метаболизм
Луразидон метаболизируется в основном при участии изофермента CYP3А4. Основными путями метаболизма являются окислительное N-деалкилирование, гидроксилирование нонборнанового кольца, S-окисление.
Луразидон метаболизируется с образованием двух активных метаболитов (ID-14283 и ID-14326) и двух неактивных метаболитов (ID-20219 и ID-20220). На долю луразидона и его метаболитов (ID-14283, ID-14326, ID-20219 и ID-20220) приходится приблизительно 11,4; 4,1; 0,4; 24 и 11 % радиоактивности плазмы соответственно. Активный метаболит ID-14283 метаболизируется в основном при участии изофермента CYP3A4. Фармакодинамический эффект обусловлен действием луразидона и его активного метаболита ID-14283 на дофаминовые и серотониновые рецепторы.
В исследованиях in vitro было выявлено, что луразидон не является субстратом изоферментов CYP1A1, CYP1A2, CYP2A6, CYP4A11, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 и CYP2E1.
В исследованиях in vitro луразидон не показал прямой или слабый ингибирующий эффект (прямой или зависимый от времени, 105,9 мкмоль) в отношении изоферментов CYP1А2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4. На основании этих данных не ожидается влияние луразидона на фармакокинетику ЛС, являющихся субстратами изоферментов CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 и CYP2E1.
В исследованиях in vitro было выявлено, что луразидон является субстратом для эффлюксных переносчиков P-gp и BCRP. Луразидон не является субстратом для активного транспорта с помощью транспортных полипептидов органических анионов ОАТР1В1 и ОАТР1В3.
Также исследования in vitro показывают, что луразидон является ингибитором P-gp, BCRP и транспортёров органических катионов первого типа (ОСТ1). Луразидон не оказывает клинически значимый ингибирующий эффект на ОАТР1В1, ОАТР1В3, транспортёры органических катионов второго типа (ОСТ2), транспортёры органических анионов первого (ОАТ1) и третьего типов (ОАТ3), почечные транспортёры МАТЕ1 и МАТЕ2К или экспортирующую помпу желчных кислот (BSEP).
- Выведение
T 1/2 составляет около 20-40 ч. После приёма внутрь луразидона, меченного радиоактивным изотопом, около 67 % дозы выводится кишечником и около 19 % — почками. Моча содержит главным образом метаболиты вследствие минимальной почечной экскреции исходного соединения.
Фармакокинетические параметры луразидона линейны в диапазоне общей суточной дозы от 20 до 160 мг. Равновесная концентрация Css луразидона достигается в течение 7 дней с момента начала терапии.
Примечания
- ↑ Lurasidone - Sumitomo Dainippon Pharma - AdisInsight. adisinsight.springer.com. Дата обращения: 25 ноября 2021. Архивировано 25 ноября 2021 года.
- ↑ Martin P. Cruz. Lurasidone HCl (Latuda), an Oral, Once-Daily Atypical Antipsychotic Agent for the Treatment of Patients with Schizophrenia // Pharmacy and Therapeutics. — 2011-8. — Т. 36, вып. 8. — С. 489–492. — ISSN 1052-1372.
- ↑ Stephen M. Stahl. Stahl's essential psychopharmacology : neuroscientific basis and practical application. — Fourth edition. — Cambridge, 2013. — xv, 608 pages с. — ISBN 978-1-107-02598-1, 1-107-02598-2, 978-1-107-68646-5, 1-107-68646-6, 978-0-521-85702-4, 0-521-85702-3.
- ↑ 1 2 Беккер РА, Быков ЮВ. Эффективность и безопасность антипсихотика III поколения луразидона (Латуда) при шизофрении и биполярных депрессиях (обзор литературы с комментариями). (рус.) // Психиатрия и психофармакотерапия им. П.Б. Ганнушкина №04 2019.
- ↑ com/LatudaPrescribingInformation.pdf Latuda (lurasidone HCl). Tablets US prescribing information.
- ↑ Radhika Bawa, Jonathan R. Scarff. Lurasidone: A New Treatment Option for Bipolar Depression—A Review // Innovations in Clinical Neuroscience. — 2015. — Т. 12, вып. 1—2. — С. 21–23. — ISSN 2158-8333. Архивировано 11 ноября 2020 года.
- ↑ 1 2 3 4 5 6 7 Государственный реестр лекарственных средств. grls.rosminzdrav.ru. Дата обращения: 25 ноября 2021. Архивировано 25 ноября 2021 года.
- ↑ Шмуклер АБ. Новый атипичный антипсихотик луразидон: результаты рандомизированных клинических исследований // Социальная и клиническая психиатрия. 2019. №3.
- ↑ Mitsutaka Nakamura, Masaaki Ogasa, John Guarino, Debra Phillips, Joseph Severs. Lurasidone in the treatment of acute schizophrenia: a double-blind, placebo-controlled trial // The Journal of Clinical Psychiatry. — 2009-06. — Т. 70, вып. 6. — С. 829–836. — ISSN 1555-2101. — doi:10.4088/JCP.08m04905. Архивировано 25 ноября 2021 года.
- ↑ 1 2 Herbert Y. Meltzer, Josephine Cucchiaro, Robert Silva, Masaaki Ogasa, Debra Phillips. Lurasidone in the treatment of schizophrenia: a randomized, double-blind, placebo- and olanzapine-controlled study // The American Journal of Psychiatry. — 2011-09. — Т. 168, вып. 9. — С. 957–967. — ISSN 1535-7228. — doi:10.1176/appi.ajp.2011.10060907. Архивировано 25 ноября 2021 года.
- ↑ Henry A. Nasrallah, Robert Silva, Debra Phillips, Josephine Cucchiaro, Jay Hsu. Lurasidone for the treatment of acutely psychotic patients with schizophrenia: a 6-week, randomized, placebo-controlled study // Journal of Psychiatric Research. — 2013-05. — Т. 47, вып. 5. — С. 670–677. — ISSN 1879-1379. — doi:10.1016/j.jpsychires.2013.01.020. Архивировано 25 ноября 2021 года.
- ↑ Masaaki Ogasa, Tatsuya Kimura, Mitsutaka Nakamura, John Guarino. Lurasidone in the treatment of schizophrenia: a 6-week, placebo-controlled study // Psychopharmacology. — 2013-02. — Т. 225, вып. 3. — С. 519–530. — ISSN 1432-2072. — doi:10.1007/s00213-012-2838-2. Архивировано 25 ноября 2021 года.
- ↑ 1 2 Antony Loebel, Josephine Cucchiaro, Kaushik Sarma, Lei Xu, Chuanchieh Hsu. Efficacy and safety of lurasidone 80 mg/day and 160 mg/day in the treatment of schizophrenia: a randomized, double-blind, placebo- and active-controlled trial // Schizophrenia Research. — 2013-04. — Т. 145, вып. 1—3. — С. 101–109. — ISSN 1573-2509. — doi:10.1016/j.schres.2013.01.009. Архивировано 25 ноября 2021 года.
- ↑ A. Loebel, J. Cucchiaro, R. Silva, Y. Mao, J. Xu. Efficacy of lurasidone across five symptom dimensions of schizophrenia: pooled analysis of short-term, placebo-controlled studies // European Psychiatry: The Journal of the Association of European Psychiatrists. — 2015-01. — Т. 30, вып. 1. — С. 26–31. — ISSN 1778-3585. — doi:10.1016/j.eurpsy.2014.08.001. Архивировано 25 ноября 2021 года.
- ↑ Henry A. Nasrallah, Josephine B. Cucchiaro, Yongcai Mao, Andrei A. Pikalov, Antony D. Loebel. Lurasidone for the treatment of depressive symptoms in schizophrenia: analysis of 4 pooled, 6-week, placebo-controlled studies // CNS spectrums. — 2015-04. — Т. 20, вып. 2. — С. 140–147. — ISSN 1092-8529. — doi:10.1017/S1092852914000285. Архивировано 25 ноября 2021 года.
- ↑ 1 2 Antony Loebel, Josephine Cucchiaro, Jane Xu, Kaushik Sarma, Andrei Pikalov. Effectiveness of lurasidone vs. quetiapine XR for relapse prevention in schizophrenia: A 12-month, double-blind, noninferiority study // Schizophrenia Research. — 2013-06. — Т. 147, вып. 1. — С. 95–102. — ISSN 0920-9964. — doi:10.1016/j.schres.2013.03.013.
- ↑ Philip D. Harvey, Cynthia O. Siu, Jay Hsu, Josephine Cucchiaro, Paul Maruff. Effect of lurasidone on neurocognitive performance in patients with schizophrenia: A short-term placebo- and active-controlled study followed by a 6-month double-blind extension // European Neuropsychopharmacology. — 2013-11. — Т. 23, вып. 11. — С. 1373–1382. — ISSN 0924-977X. — doi:10.1016/j.euroneuro.2013.08.003.
- ↑ Philip D. Harvey, Cynthia O. Siu, Masaaki Ogasa, Antony Loebel. Effect of lurasidone dose on cognition in patients with schizophrenia: Post-hoc analysis of a long-term, double-blind continuation study // Schizophrenia Research. — 2015-08. — Т. 166, вып. 1—3. — С. 334–338. — ISSN 0920-9964. — doi:10.1016/j.schres.2015.06.008.
- ↑ 1 2 Robert Goldman, Antony Loebel, Josephine Cucchiaro, Ling Deng, Robert L. Findling. Efficacy and Safety of Lurasidone in Adolescents with Schizophrenia: A 6-Week, Randomized Placebo-Controlled Study // Journal of Child and Adolescent Psychopharmacology. — 2017-08. — Т. 27, вып. 6. — С. 516–525. — ISSN 1557-8992 1044-5463, 1557-8992. — doi:10.1089/cap.2016.0189.
- ↑ 1 2 Matt Shirley. Lurasidone in schizophrenia in adolescents: a profile of its use // Drugs & Therapy Perspectives. — 2021-08. — Т. 37, вып. 8. — С. 347–353. — ISSN 1179-1977 1172-0360, 1179-1977. — doi:10.1007/s40267-021-00849-8.
- ↑ Antony Loebel, Josephine Cucchiaro, Robert Silva, Hans Kroger, Jay Hsu. Lurasidone Monotherapy in the Treatment of Bipolar I Depression: A Randomized, Double-Blind, Placebo-Controlled Study // American Journal of Psychiatry. — 2014-02. — Т. 171, вып. 2. — С. 160–168. — ISSN 1535-7228 0002-953X, 1535-7228. — doi:10.1176/appi.ajp.2013.13070984.
- ↑ Antony Loebel, Josephine Cucchiaro, Robert Silva, Hans Kroger, Kaushik Sarma. Lurasidone as Adjunctive Therapy With Lithium or Valproate for the Treatment of Bipolar I Depression: A Randomized, Double-Blind, Placebo-Controlled Study (англ.) // American Journal of Psychiatry. — 2014-02. — Vol. 171, iss. 2. — P. 169–177. — ISSN 1535-7228 0002-953X, 1535-7228. — doi:10.1176/appi.ajp.2013.13070985.
- ↑ 1 2 Manpreet Singh, Michael Tocco, Edward Schweizer, Andrei Pikalov. Long-Term Effectiveness of Lurasidone in Pediatric Bipolar Depression: Response, Remission and Recovery (англ.) // CNS Spectrums. — 2021-04. — Vol. 26, iss. 2. — P. 148–148. — ISSN 2165-6509 1092-8529, 2165-6509. — doi:10.1017/S1092852920002345.
- ↑ 1 2 LATUDA (lurasidone hydrochloride) tablet, film coated (англ.). DailyMed. U. S. National Library of Medicine.
- ↑ 1 2 3 Samalin L, Garnier M, Llorca PM. Clinical potential of lurasidone in the management of schizophrenia // Ther Clin Risk Manag. — 2011. — № 7. — С. 239—50. — doi:10.2147/TCRM.S12701. — PMID 21753886.
- ↑ Yasui-Furukori N. Update on the development of lurasidone as a treatment for patients with acute schizophrenia // Drug Des Devel Ther. — 2012. — Т. 6. — С. 107—15. — doi:10.2147/DDDT.S11180. — PMID 22675261. Архивировано 24 марта 2022 года.
- ↑ lurasidone (Rx) — Latuda [Internet]. Medscape Reference. [cited 2013 Oct 1]. Available from: http://reference.medscape.com/drug/latuda-lurasidone-999605#4 Архивная копия от 17 августа 2021 на Wayback Machine
- ↑ Alamo C, López-Muñoz F, García-García P. The effectiveness of lurasidone as an adjunct to lithium or divalproex in the treatment of bipolar disorder // Expert Rev Neurother. — 2014 Jun. — Т. 14, № 6. — С. 593—605. — doi:10.1586/14737175.2014.915741. — PMID 24779382.
- ↑ 1 2 Silvio Caccia, Pasina, Alessandro Nobili. Critical appraisal of lurasidone in the management of schizophrenia // Neuropsychiatric Disease and Treatment. — 2012-04. — С. 155. — ISSN 1176-6328. — doi:10.2147/ndt.s18059.
- ↑ 1 2 Tadashi Ishibashi, Tomoko Horisawa, Kumiko Tokuda, Takeo Ishiyama, Masaaki Ogasa. Pharmacological Profile of Lurasidone, a Novel Antipsychotic Agent with Potent 5-Hydroxytryptamine 7 (5-HT7) and 5-HT1A Receptor Activity // Journal of Pharmacology and Experimental Therapeutics. — 2010-04-19. — Т. 334, вып. 1. — С. 171–181. — ISSN 1521-0103 0022-3565, 1521-0103. — doi:10.1124/jpet.110.167346.
- ↑ Roger S McIntyre, Danielle S Cha, Mohammad Alsuwaidan, Diane McIntosh, Alissa M Powell. A review of published evidence reporting on the efficacy and pharmacology of lurasidone // Expert Opinion on Pharmacotherapy. — 2012-05-05. — Т. 13, вып. 11. — С. 1653–1659. — ISSN 1744-7666 1465-6566, 1744-7666. — doi:10.1517/14656566.2012.683174.
- ↑ Massimo Carlo Mauri. Reply to Periclou et al.: “Clinical Pharmacokinetics of Atypical Antipsychotics: An Update” // Clinical Pharmacokinetics. — 2019-07-11. — Т. 58, вып. 9. — С. 1217–1218. — ISSN 1179-1926 0312-5963, 1179-1926. — doi:10.1007/s40262-019-00796-8.
- ↑ Hua Zhang, Hubo Wang, Xueyan Zhu, Zhedong Yuan, Huijuan Jiang. Lurasidone hydrochloride // Acta Crystallographica Section E Structure Reports Online. — 2012-04-13. — Т. 68, вып. 5. — С. o1357–o1357. — ISSN 1600-5368. — doi:10.1107/s1600536812012883.
- ↑ 1 2 3 Leslie Citrome, Josephine Cucchiaro, Kaushik Sarma, Debra Phillips, Robert Silva. Long-term safety and tolerability of lurasidone in schizophrenia // International Clinical Psychopharmacology. — 2012-05. — Т. 27, вып. 3. — С. 165–176. — ISSN 0268-1315. — doi:10.1097/yic.0b013e32835281ef.
- ↑ Stephen M. Stahl, Josephine Cucchiaro, Doreen Simonelli, Jay Hsu, Andrei Pikalov. Effectiveness of Lurasidone for Patients With Schizophrenia Following 6 Weeks of Acute Treatment With Lurasidone, Olanzapine, or Placebo // The Journal of Clinical Psychiatry. — 2013-03-13. — Т. 74, вып. 05. — С. 507–515. — ISSN 0160-6689. — doi:10.4088/jcp.12m08084.
- ↑ Liana Dehelean, Ana-Maria Romosan, Ion Papava, Cristina Ana Bredicean, Victor Dumitrascu. Prolactin response to antipsychotics: An inpatient study (англ.) // PLOS ONE / Kenji Hashimoto. — 2020-02-04. — Vol. 15, iss. 2. — P. e0228648. — ISSN 1932-6203. — doi:10.1371/journal.pone.0228648.
- ↑ Subramoniam Madhusoodanan, Suprit Parida, Carolina Jimenez. Hyperprolactinemia associated with psychotropics-a review (англ.) // Human Psychopharmacology: Clinical and Experimental. — 2010-05-06. — Vol. 25, iss. 4. — P. 281–297. — doi:10.1002/hup.1116. Архивировано 25 ноября 2021 года.
- ↑ Antony Loebel, Josephine Cucchiaro, Kaushik Sarma, Lei Xu, Chuanchieh Hsu. Efficacy and safety of lurasidone 80mg/day and 160mg/day in the treatment of schizophrenia: A randomized, double-blind, placebo- and active-controlled trial (англ.) // Schizophrenia Research. — 2013-04. — Vol. 145, iss. 1—3. — P. 101–109. — doi:10.1016/j.schres.2013.01.009. Архивировано 3 мая 2022 года.
- ↑ 1 2 Human medicines European public assessment report (EPAR): Latuda, lurasidone, Schizophrenia, Date of authorisation: 20/03/2014, Revision: 17, Status: Authorised // Case Medical Research. — 2019-09-02. — ISSN 2643-4652. — doi:10.31525/cmr-6036d0.
- ↑ Citrome L. Lurasidone for schizophrenia: a brief review of a new second-generation antipsychotic // Clin Schizophr Relat Psychoses. — 2011 Jan. — Т. 4, № 4. — С. 251—7. — doi:10.3371/CSRP.4.4.5. — PMID 21177242.
- ↑ Norio Yasui-Furukori. Update on the development of lurasidone as a treatment for patients with acute schizophrenia // Drug Design, Development and Therapy. — 2012-05. — С. 107. — ISSN 1177-8881. — doi:10.2147/dddt.s11180.
- ↑ 1 2 Takeshi Murai, Tomokazu Nakako, Kazuhito Ikeda, Masaru Ikejiri, Takeo Ishiyama. Lack of dopamine D4 receptor affinity contributes to the procognitive effect of lurasidone // Behavioural Brain Research. — 2014-03. — Т. 261. — С. 26–30. — ISSN 0166-4328. — doi:10.1016/j.bbr.2013.11.036.
- ↑ Leslie Citrome. Lurasidone for Schizophrenia: A Brief Review of a New Second-Generation Antipsychotic // Clinical Schizophrenia & Related Psychoses. — 2011-01. — Т. 4, вып. 4. — С. 251–257. — ISSN 1935-1232. — doi:10.3371/csrp.4.4.5.
- ↑ Stephen M. Stahl. Stahl's essential psychopharmacology : prescriber's guide. — Sixth edition. — Cambridge, United Kingdom, 2017. — xvi, 868 pages с. — ISBN 978-1-316-61813-4, 1-316-61813-7, 978-1-108-40488-4, 1-108-40488-X.
- ↑ Dean F. Wong, Hiroto Kuwabara, James Robert Brašić, Thomas Stock, Atul Maini. Determination of dopamine D2 receptor occupancy by lurasidone using positron emission tomography in healthy male subjects (англ.) // Psychopharmacology. — 2013-09. — Vol. 229, iss. 2. — P. 245–252. — ISSN 1432-2072 0033-3158, 1432-2072. — doi:10.1007/s00213-013-3103-z.
- ↑ 1 2 Mei Huang, Masakuni Horiguchi, Anna R. Felix, Herbert Y. Meltzer. 5-HT1A and 5-HT7 receptors contribute to lurasidone-induced dopamine efflux // NeuroReport. — 2012-05-09. — Т. 23, вып. 7. — С. 436–440. — ISSN 0959-4965. — doi:10.1097/wnr.0b013e328352de40.
- ↑ 1 2 Mei Huang, Sunoh Kwon, Lakshmi Rajagopal, Wenqi He, Herbert Y. Meltzer. 5-HT1A parital agonism and 5-HT7 antagonism restore episodic memory in subchronic phencyclidine-treated mice: role of brain glutamate, dopamine, acetylcholine and GABA // Psychopharmacology. — 2018-07-31. — Т. 235, вып. 10. — С. 2795–2808. — ISSN 1432-2072 0033-3158, 1432-2072. — doi:10.1007/s00213-018-4972-y.
- ↑ Okada, Fukuyama, Okubo, Shiroyama, Ueda. Lurasidone Sub-Chronically Activates Serotonergic Transmission via Desensitization of 5-HT1A and 5-HT7 Receptors in Dorsal Raphe Nucleus (англ.) // Pharmaceuticals. — 2019-10-06. — Vol. 12, iss. 4. — P. 149. — ISSN 1424-8247. — doi:10.3390/ph12040149. Архивировано 25 ноября 2021 года.