Пиперилен: различия между версиями
Перейти к навигации
Перейти к поиску
| [непроверенная версия] | [непроверенная версия] |
Содержимое удалено Содержимое добавлено
Нет описания правки |
Нет описания правки |
||
| Строка 134: | Строка 134: | ||
'''Пиперилен''' — летучий, горючий [[углеводород]], состоящий из пяти углеродных цепей с двумя [[двойные связи|двойными связями]]. Получается как побочный продукт [[этилен]]произведённого из сырой нефти. |
'''Пиперилен''' — летучий, горючий [[углеводород]], состоящий из пяти углеродных цепей с двумя [[двойные связи|двойными связями]]. Получается как побочный продукт [[этилен]]произведённого из сырой нефти. |
||
Пиперилена используется в качестве [[мономер] |
Пиперилена используется в качестве [[мономер]]а при производстве пластмасс, клеев и смол.<ref>[http://www.shell.com/home/content/chemicals/products_services/our_products/lower_olefins/piperylene/product_overview/piperylene_overview.html Piperylene] at Shell Chemicals. Retrieved 2009-05-19.</ref> |
||
Пиперилен бесцветный.<ref>http://msds.chem.ox.ac.uk/PI/piperylene.html</ref> |
Пиперилен бесцветный.<ref>http://msds.chem.ox.ac.uk/PI/piperylene.html</ref> |
||
Версия от 05:19, 25 мая 2011
| Пиперилен | |||
|---|---|---|---|
| |||
| Общие | |||
| Хим. формула | C5H8 | ||
| Физические свойства | |||
| Молярная масса | 68,117 г/моль | ||
| Плотность | 0,683 г/см³ | ||
| Классификация | |||
| Рег. номер CAS | 504-60-9 | ||
| PubChem | 62204 | ||
| Рег. номер EINECS | 207-995-2 | ||
| SMILES | |||
| InChI | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
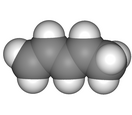
Пиперилен — летучий, горючий углеводород, состоящий из пяти углеродных цепей с двумя двойными связями. Получается как побочный продукт этиленпроизведённого из сырой нефти.
Пиперилена используется в качестве мономера при производстве пластмасс, клеев и смол.[1] Пиперилен бесцветный.[2]
См. также
Примечания
- ↑ Piperylene at Shell Chemicals. Retrieved 2009-05-19.
- ↑ http://msds.chem.ox.ac.uk/PI/piperylene.html
Это заготовка статьи по органической химии. Помогите Википедии, дополнив её. |