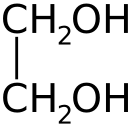Этиленгликоль: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
762bot (обсуждение | вклад) м автоматическое удаление устаревших параметров карточки {{Вещество}} |
|||
| Строка 87: | Строка 87: | ||
== Меры безопасности == |
== Меры безопасности == |
||
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8- 6,4 % (по объему). |
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8- 6,4 % (по объему). Этиленгликоль токсичен. По степени воздействия на организм относится к веществам 3-го класса опасности. |
||
| ⚫ | Летальная доза при однократном пероральном употреблении составляет 100—300 мл этиленгликоля (1,5-5мл на 1 кг массы тела)<ref>[http://www.medline.ru/public/art/tom4/art124.phtml Medline.Ru — Отравления этиленгликолем и его эфирами<!-- Название сгенерировано ботом -->]</ref>. Имеет относительно низкую летучесть при нормальной температуре, пары обладают не столь высокой токсичностью и представляют опасность лишь при хроническом вдыхании. Определённую опасность представляют туманы, однако при их вдыхании об опасности сигнализируют раздражение и кашель. [[Противоядие]]м при отравлении этиленгликолем являются [[этанол]] и [[4-метилпиразол]]<ref>{{книга|автор = Flomenbaum, Goldfrank et al.|заглавие = Goldfrank's Toxicologic Emergencies. 8th Edition|ссылка=http://books.google.ru/books?id=cvJuLqBxGUcC&lpg=PP1&pg=PP1#v=onepage&q=&f=false|год = 2006|издательство = McGraw Hill|страниц = 2170|isbn = 0071437630|страницы=1460, 1465}}</ref>. |
||
Требования безопасности |
|||
Этиленгликоль горюч, по степени воздействия на организм относится к веществам 3-го класса опасности. |
|||
| ⚫ | |||
== См. также == |
== См. также == |
||
Версия от 06:25, 20 сентября 2013
| Этиленгликоль | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
этан диол-1,2 | ||
| Традиционные названия | этиленгликоль, 1,2-диоксиэтан, 1,2-этандиол | ||
| Хим. формула | C2H4(OH)2 | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 62,068 г/моль | ||
| Плотность | 1,11 ± 0,01 г/см³[1] | ||
| Энергия ионизации | 10,16 эВ[4] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −12,9 °C | ||
| • кипения | 197,3 °C | ||
| • вспышки | 232 ± 1 ℉[1] | ||
| Пределы взрываемости | 3,2 ± 0,1 об.%[1] | ||
| Энтальпия | |||
| • кипения | 50,5 кДж/моль[2] и 57,4 кДж/моль[3] | ||
| Давление пара | 7900 миллипаскаль[5] | ||
| Химические свойства | |||
| Константа диссоциации кислоты | 15,1 ± 0,1[5] | ||
| Оптические свойства | |||
| Показатель преломления | 1,3811[6] | ||
| Структура | |||
| Дипольный момент | 7,6E−30 Кл·м[4] | ||
| Классификация | |||
| Рег. номер CAS | 107-21-1 | ||
| PubChem | 174 | ||
| Рег. номер EINECS | 203-473-3 | ||
| SMILES | |||
| InChI | |||
| RTECS | KW2975000 | ||
| ChEBI | 30742 | ||
| ChemSpider | 13835235 | ||
| Безопасность | |||
| Токсичность | токсичен | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
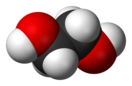
Этиленглико́ль (гликоль; 1,2-диоксиэтан; этандиол-1,2), HO—CH2—CH2—OH — простейший представитель полиолов (многоатомных спиртов). В очищенном виде представляет собой прозрачную бесцветную жидкость слегка маслянистой консистенции. Не имеет запаха и обладает сладковатым вкусом. Токсичен. Попадание этиленгликоля или его растворов в организм человека может привести к необратимым изменениям в организме и к летальному исходу[7].
История открытий и производства
Этиленгликоль впервые был получен в 1859 французским химиком Вюрцом из диацетата этиленгликоля омылением гидроксидом калия и в 1860 гидратацией этиленоксида. Он не находил широкого применения до Первой мировой войны, когда в Германии его стали получать из дихлорэтана для использования в качестве замены глицерина при производстве взрывчатых веществ. В США полупромышленное производство начато в 1917 году через этиленхлоргидрин. Первое крупномасштабное производство начато с возведением завода в 1925 году около Южного Чарлстона (западная Вирджиния, США) компанией "Carbide and Carbon Chemicals Co." К 1929 году этиленгликоль использовался практически всеми производителями динамита. В 1937 кампания Carbide начала первое крупномасштабное производство, основанное на газофазном окислении этилена до этиленоксида. Монополия компании Carbide на данный процесс продолжалась до 1953 года.
Получение
В промышленности этиленгликоль получают путём гидратации оксида этилена при 10 атм и 190—200°С или при 1 атм и 50—100°С в присутствии 0,1—0,5 % серной или ортофосфорной кислоты, достигая 90% выхода. Побочными продуктами при этом являются триэтиленгликоль и незначительное количество высших полимергомологов этиленгликоля.
Применение
Благодаря своей дешевизне этиленгликоль нашёл широкое применение в технике.
- Как компонент автомобильных антифризов и тормозных жидкостей, что составляет 60 % его потребления. Смесь 60 % этиленгликоля и 40 % воды замерзает при −45 °С. Коррозионно активен, поэтому применяется с ингибиторами коррозии;
- В качестве теплоносителя в виде раствора в автомобилях, в системах жидкостного охлаждения компьютеров;
- В производстве целлофана, полиуретанов и ряда других полимеров. Это второе основное применение;
- Как растворитель красящих веществ;
- В органическом синтезе:
- в качестве высокотемпературного растворителя.
- для защиты карбонильной группы путём получения 1,3-диоксалана. Обработкой вещества с карбонильной группой в бензоле или толуоле этиленгликолем в присутствии кислого катализатора (толуолсульфоновой кислоты, BF3•Et2O и др.) и азеотропной отгонкой на насадке Дина-Старка образующейся воды. Например, защита карбонильной группы изофорона

1,3-диоксоланы могут быть получены также при реакции этиленгликоля с карбонильными соединениями в присутствии триметилхлорсилана[8] или комплекса диметилсульфат-ДМФА[9] 1,3-диоксалана устойчивы к действию нуклеофилов и оснований. Легко регенерируют исходное карбонильное соединение в присутствии кислоты и воды.
- Как компонент жидкости «И», используемой для предотвращения обводнения авиационных топлив.
- В качестве криопротектора
- Для поглощения воды, для предотвращения образования гидрата метана, который забивает трубопроводы при добыче газа в открытом море. На наземных станциях его регенириуют путём осушения и удаления солей.
- Этиленгликоль является исходным сырьём для производства взрывчатого вещества нитрогликоля.
Этиленгликоль также применяется:
- при производстве конденсаторов
- при производстве 1,4-диоксана
- компонент в составе систем жидкостного охлаждения компьютеров
- как теплоноситель в системах чиллер-фанкойл
- в качестве компонента крема для обуви (1—2 %)
- в составе для мытья стёкол вместе с изопропиловым спиртом
Очистка и осушение
Осушается молекулярным ситом 4А, полуводным сульфатом кальция, сульфатом натрия, Mg+I2, фракционной перегонкой под пониженным давлением, азеотропной отгонкой с бензолом. Чистота полученного продукта легко определяется по плотности.
Таблица плотности водных растворов этиленгликоля, 20°С
| Концентрация % | 30 | 35 | 40 | 45 | 50 | 55 | 60 |
|---|---|---|---|---|---|---|---|
| Плотность, г/мл | 1,050 | 1,058 | 1,067 | 1,074 | 1,082 | 1,090 | 1,098 |
Меры безопасности
Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C. Температура самовоспламенения 380 °C. Температурные пределы воспламенения паров в воздухе, °С: нижний — 112, верхний — 124. Пределы воспламенения паров в воздухе от нижнего до верхнего, 3,8- 6,4 % (по объему). Этиленгликоль токсичен. По степени воздействия на организм относится к веществам 3-го класса опасности. Летальная доза при однократном пероральном употреблении составляет 100—300 мл этиленгликоля (1,5-5мл на 1 кг массы тела)[10]. Имеет относительно низкую летучесть при нормальной температуре, пары обладают не столь высокой токсичностью и представляют опасность лишь при хроническом вдыхании. Определённую опасность представляют туманы, однако при их вдыхании об опасности сигнализируют раздражение и кашель. Противоядием при отравлении этиленгликолем являются этанол и 4-метилпиразол[11].
См. также
Примечания
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0272.html
- ↑ https://pubchem.ncbi.nlm.nih.gov/compound/174#section=Heat-of-Vaporization
- ↑ https://webbook.nist.gov/cgi/cbook.cgi?ID=C107211&Mask=4
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 1 2 http://sitem.herts.ac.uk/aeru/ppdb/en/Reports/1310.htm
- ↑ http://www.refractometer.pl/refraction-datasheet-ethylene-glycol
- ↑ Monograph on the Potential Human Reproductive and Developmental Effects of Ethylene Glycol
- ↑ SYNTHESIS 1983, No 3,pp 203—205
- ↑ Liebigs Annalen Chemie 1979, pp 1362—1369
- ↑ Medline.Ru — Отравления этиленгликолем и его эфирами
- ↑ Flomenbaum, Goldfrank et al. Goldfrank's Toxicologic Emergencies. 8th Edition. — McGraw Hill, 2006. — С. 1460, 1465. — 2170 с. — ISBN 0071437630.
Ссылки
- Международная карта химической безопасности для этиленгликоля (рус.)
- Сертификаты на этиленгликоль (рус.)
- ГОСТ 19710-83. Этиленгликоль. Технические условия. (рус.)
- Об отравлениях этиленгликолем
- Hairong Yue, Yujun Zhao, Xinbin Ma and Jinlong Gong. Ethylene glycol: properties, synthesis, and applications. Critical Review — Chemical Society Reviews. Issue 11, 2012, 41, 4218-4244. DOI: 10.1039/C2CS15359A
Это заготовка статьи об органическом веществе. Помогите Википедии, дополнив её. |