Диметилсульфат: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
Djem92 (обсуждение | вклад) |
Djem92 (обсуждение | вклад) |
||
| Строка 101: | Строка 101: | ||
Высокотоксичное вещество с кожно-резорбтивным воздействием, ЛД<sub>50</sub> = 140 г/кг (мыши, перорально). |
Высокотоксичное вещество с кожно-резорбтивным воздействием, ЛД<sub>50</sub> = 140 г/кг (мыши, перорально). |
||
Пары диметилсульфата оказывают сильное раздражающее и прижигающее воздействие на слизистые оболочки дыхательных путей и глаз (воспалительные явления, отёки, поражения дыхательных путей, [[конъюктивит]]). Оказывает также общее токсическое действие, особенно на [[ЦНС]]. Жидкий диметилсульфат при попадании на кожу вызывает [[ожог]]и и долго незаживающие [[Язва|язвы]], в высоких концентрациях омертвение (некроз). Токсичность обусловлена продуктами гидролиза, которые включают [[метанол]] и едкую [[Серная кислота|серную кислоту]]. |
Пары диметилсульфата оказывают сильное раздражающее и прижигающее воздействие на слизистые оболочки дыхательных путей и глаз (воспалительные явления, отёки, поражения дыхательных путей, [[конъюктивит]])<ref name="A">Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей. Изд. 7-е, пер. и доп. В трех томах. Том III. Органические вещества. Под ред. засл. деят. науки проф. Н. В. Лазарева и докт. мед. наук Э. Н. Левиной. Л., «Химия», 1976. 592 стр., 27 табл., библиография —1850 названий.</ref>. Оказывает также общее токсическое действие, особенно на [[ЦНС]]. Жидкий диметилсульфат при попадании на кожу вызывает [[ожог]]и и долго незаживающие [[Язва|язвы]], в высоких концентрациях омертвение (некроз). Токсичность обусловлена продуктами гидролиза, которые включают [[метанол]] и едкую [[Серная кислота|серную кислоту]]. |
||
Скрытый период при лёгких отравлениях составляет до 15 часов, при отравлениях средней тяжести - до 5 часов, при тяжелых - до 2-3 часов. |
Скрытый период при лёгких отравлениях составляет до 15 часов, при отравлениях средней тяжести - до 5 часов, при тяжелых - до 2-3 часов<ref name="A" />. |
||
Особенно опасно поражение глаз (возможна потеря зрения). В тяжелых случаях отравления наблюдается кома, паралич и смерть в течение 3-4 дней. Является сильным [[Канцероген|канцерогеном]], проявляет мутагенные эффекты. Канцерогенный и мутагенный эффекты обусловлены метилированием [[ДНК]]. |
Особенно опасно поражение глаз (возможна потеря зрения). В тяжелых случаях отравления наблюдается кома, паралич и смерть в течение 3-4 дней<ref name="A" />. Является сильным [[Канцероген|канцерогеном]], проявляет мутагенные эффекты. Канцерогенный и мутагенный эффекты обусловлены метилированием [[ДНК]]. |
||
== См. также == |
== См. также == |
||
Версия от 15:52, 18 февраля 2016
| Диметилсульфат | |||
|---|---|---|---|
| |||
| Общие | |||
| Хим. формула | (CH3)2SO4 | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 126.13 г/моль | ||
| Плотность | 1.33 г/см³ | ||
| Динамическая вязкость | 1,60 Па·с | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -32 °C | ||
| • кипения | 188 с разложением °C | ||
| • разложения | 370 ± 1 ℉[1] | ||
| • вспышки | 83 °C | ||
| Давление пара | 0,1 ± 0,1 мм рт.ст. | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | гидролизуется | ||
| Оптические свойства | |||
| Показатель преломления | 1,3874 | ||
| Структура | |||
| Дипольный момент | 10,92 Д | ||
| Классификация | |||
| Рег. номер CAS | 77-78-1 | ||
| PubChem | 6497 | ||
| Рег. номер EINECS | 201-058-1 | ||
| SMILES | |||
| InChI | |||
| RTECS | WS8225000 | ||
| ChEBI | 59050 | ||
| ChemSpider | 6252 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
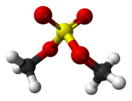
Диметилсульфат — химическое соединение, органический сульфат с формулой (CH3)2SO4. Представляет собой бесцветную жидкость, малорастворимую в воде. Чистый диметилсульфат не имеет запаха. Примеси могут придавать ему слабый запах чеснока. Впервые получен в начале XIX века. Как и все алкилирующие реагенты диметилсульфат токсичен и канцерогенен. В то же время он широко применяется как метилирующий агент в органическом синтезе. В некоторых случаях может быть заменён метиловым эфиром трифторметансульфоновой кислоты (CF3SO3CH3).
Получение
Для получения диметилсульфата в лаборатории используются различные методы. Простейший — этерификация серной кислоты с метанолом:
- 2 CH3OH + H2SO4 → (CH3)2SO4 + 2 H2O
Другой возможный способ включает в себя дистилляцию метилсерной кислоты в вакууме (перегонка 60 % олеум с метанолом):
- 2 CH3HSO4 → H2SO4 + (CH3)2SO4
Метилнитрит и метилхлорсульфонат также дают диметисульфат:
- CH3ONO + (CH3)OSO2Cl → (CH3)2SO4 + NOCl
В США Me2SO4 производится коммерчески с 20-х годов XX века. В непрерывном процессе реакции диметилового эфира и трёхокиси серы:
- (CH3)2O + SO3 → (CH3)2SO4
Ещё один способ получения диметилсульфата — реакция хлорсульфоновой кислоты с метанолом:
- 2CH3OH + HOSO2Cl → (CH3)2SO4 + HCl↑ + H2O [2]
Химические свойства
Растворим в метаноле, этаноле, этиловом эфире, дихлорметане, ацетоне, хлороформе, нитробензоле, также реакции иногда ведут в воде. Со взрывом реагирует с аммиаком и аминами. Реакции растворов аминов дает соответственно вещества с большим содержанием метильных групп при азоте, третичные амины дают четвертичные соли. При этом первая метильная группа уходит значительно быстрее второй. Он также алкилирует фенолы и тиолы. Считается, что реакции идут по SN2 механизму. Несмотря на высокую эффективность диметилсульфата, из-за токсичности и высокой стоимости ему часто ищут замену. Так при О-алкилировании используют иодметан. Диметилкарбонат менее токсичен предыдущих реагентов, поэтому может успешно быть заменить их при N-алкилировании. В целом токсичность алкилирующих агентов прямо коррелирует с их способностью алкилировать.
Применение
Широко применяется в органическом синтезе для метилирования различных веществ: фенолов, аминов, некоторых гетероциклических соединений пуринового ряда, таких как мочевая кислота и других. Так же применяется для получения нитрометана:
2NaNO2 + (CH3)2SO4 = 2CH3NO2 + Na2SO4
Метилирование по углероду
С-Н кислоты метилируются диметилсульфатом в апротонных растворителях
Метилирование по кислороду
Чаще всего Me2SO4 используется для метилирования фенолов. Некоторые простые спирты также могут быть прометилированы, как, например, трет-бутанол в трет-бутилметиловый эфир.
- 2 (CH3)3COH + (CH3O)2SO2→ 2 (CH3)3COCH3 + H2SO4
Алкоголяты легко метилируются:[3]
- RO− Na+ + (CH3O)2SO2 → ROCH3 + Na(CH3)SO4
Метилирование сахаров диметилсульфатом называется метилированием по Гаворту. [4][5]
Метилирование по азоту
Me2SO4 используется как для получения четвертичных солей так и третичных Аминов.
- C6H5CH=NC4H9 + (CH3O)2SO2 → C6H5CH=N+(CH3)C4H9 + CH3OSO3−
Кватернизованные аммониевые соли жирных кислот используют как ПАВ так и в качестве смягчителя тканей.[3]:
- CH3(C6H4)NH2 + (CH3O)2SO2 (in NaHCO3 aq.) → CH3(C6H4)N(CH3)2 + Na(CH3)SO4
Метилирование по сере
Так же как и метилирование спиртов, алкилируются соли тиолов, но с большей скоростью[3]:
- RS−Na+ + (CH3O)2SO2 → RSCH3 + Na(CH3)SO4
Например:[6]
- p-CH3C6H4SO2Na + (CH3O)2SO2 → p-CH3C6H4SO2CH3 + Na(CH3)SO4
Этот метод был использован для получения тиоэфиров:
- RC(O)SH + (CH3O)2SO2 → RC(O)S(CH3) + HOSO3CH3
Другие применения
Диметилсульфат может вызвать специфические расщепление гуанина в ДНК путём разрушения имидазольного цикла.[7] Этот процесс может быть использован для определения последовательности оснований в ДНК и других применениях.
Диметилсульфат используется для картирования одноцепочечных фрагментов ДНК. Метод основан на различии скорости метилирования фрагментов цитозина в составе одно- и двуцепочечных нуклеиновых кислот[8].
Токсикология и безопасность
Высокотоксичное вещество с кожно-резорбтивным воздействием, ЛД50 = 140 г/кг (мыши, перорально).
Пары диметилсульфата оказывают сильное раздражающее и прижигающее воздействие на слизистые оболочки дыхательных путей и глаз (воспалительные явления, отёки, поражения дыхательных путей, конъюктивит)[9]. Оказывает также общее токсическое действие, особенно на ЦНС. Жидкий диметилсульфат при попадании на кожу вызывает ожоги и долго незаживающие язвы, в высоких концентрациях омертвение (некроз). Токсичность обусловлена продуктами гидролиза, которые включают метанол и едкую серную кислоту.
Скрытый период при лёгких отравлениях составляет до 15 часов, при отравлениях средней тяжести - до 5 часов, при тяжелых - до 2-3 часов[9].
Особенно опасно поражение глаз (возможна потеря зрения). В тяжелых случаях отравления наблюдается кома, паралич и смерть в течение 3-4 дней[9]. Является сильным канцерогеном, проявляет мутагенные эффекты. Канцерогенный и мутагенный эффекты обусловлены метилированием ДНК.
См. также
Примечания
- ↑ http://www.cdc.gov/niosh/npg/npgd0229.html
- ↑ Препаративная органическая химия. М., Госхимиздат, 1959, стр. 399
- ↑ 1 2 3 Dupont product information
- ↑ W. N. Haworth, J. Chem. Soc. 107, 13 (1915).
- ↑ Химическая энциклопедия Т1, М 1988 стр 64
- ↑ Fieser, L. F. and Fieser, M. Reagents for Organic Synthesis. John Wiley & Sons, Inc. 1967. p. 295
- ↑ Streitwieser, A., Heathcock, C. H., and Kosower, E. M. Introduction to Organic Chemistry. Prentice-Hall Inc. 1992. p. 1169
- ↑ K. Kirkegaard, H. Buc, A. Spassky, and J. C. Wang. Mapping of single-stranded regions in duplex DNA at the sequence level: single-strand-specific cytosine methylation in RNA polymerase-promoter complexes (англ.) // PNAS. — 1983. — Vol. 80. — P. 2544-2548. — PMID 6573669.
- ↑ 1 2 3 Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей. Изд. 7-е, пер. и доп. В трех томах. Том III. Органические вещества. Под ред. засл. деят. науки проф. Н. В. Лазарева и докт. мед. наук Э. Н. Левиной. Л., «Химия», 1976. 592 стр., 27 табл., библиография —1850 названий.
Литература
- Сьютер Ч., Химия органических соединений серы, пер. с англ., ч. 1, М., 1950, с. 61-74.