Нитрат уранила: различия между версиями
| [отпатрулированная версия] | [отпатрулированная версия] |
Aesopus (обсуждение | вклад) дополнение, источники |
Aesopus (обсуждение | вклад) м оформление |
||
| Строка 135: | Строка 135: | ||
: <math>~\mathsf{Ag_4[Fe(CN)_6] + 2UO_2(NO_3)_2 = 4AgNO_3 + (UO_2)_2[Fe(CN)_6]}</math> |
: <math>~\mathsf{Ag_4[Fe(CN)_6] + 2UO_2(NO_3)_2 = 4AgNO_3 + (UO_2)_2[Fe(CN)_6]}</math> |
||
В 60-е годы XX века в [[СССР]] азотнокислый уранил свободно продавался в фотомагазинах. Входил в состав промышленно выпускаемых усилителей, применяемых в фотопечати, в частности, ОРВО 604. |
В 60-е годы XX века в [[СССР]] азотнокислый уранил свободно продавался в фотомагазинах. Входил в состав промышленно выпускаемых усилителей, применяемых в фотопечати, в частности, ОРВО 604. |
||
Версия от 09:22, 3 апреля 2016
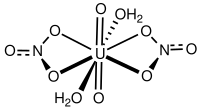
| Нитрат уранила | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Уранила нитрат |
| Традиционные названия | Азотнокислый уранил |
| Хим. формула | UO8N2 |
| Рац. формула | UO2(NO3)2 |
| Физические свойства | |
| Состояние | твёрдое, кристаллическое |
| Молярная масса | 394,04(безводн.); 502,13(дигидрат) г/моль |
| Плотность | 3,35 г/см3 (дигидрат) |
| Термические свойства | |
| Температура | |
| • разложения | 100°C |
| Энтальпия | |
| • образования | 1987 кДж/моль кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде, 20°C | 119 г/100 мл |
| • в воде, 30°C | 138 г/100 мл |
| • в ацетоне | растворим |
| • в этаноле | растворим |
| Классификация | |
| Рег. номер CAS | 10102-06-4 |
| PubChem | 24933 и 25199613 |
| Рег. номер EINECS | 233-266-3 |
| SMILES | |
| InChI | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Урани́л азотноки́слый, азотнокислая окись урана: UO2(NO3)2(безводный); UO2(NO3)2·6H2O (кристаллогидрат).
Молекулярный вес безводной формы 394,04; кристаллогидрата 502,13.
Роль металла в этой соли исполняет катион уранила [UO2]2+.
Физические свойства
Кристаллы жёлтого цвета с зеленоватым отблеском, легко растворимые в воде. Водный раствор имеет кислую реакцию. Также растворим в этаноле, ацетоне и эфире, нерастворим в бензоле, толуоле и хлороформе.
Химические свойства
При нагревании кристаллы плавятся и выделяют азотную кислоту и воду. Кристаллогидрат легко выветривается на воздухе.
Характерная реакция — при действии аммиака образуется жёлтый осадок урановокислого аммония.
Обладает свойством дубить желатин. Ядовит.
Применение
В фотографии на основе солей серебра применяется как усилитель негативов и для тонирования готовых отпечатков (рецепт на основе азотнокислого уранила окрашивает фотоснимок в красно-коричневые тона). При этом часть серебра в изображении заменяется на железосинеродистый уранил (UO2)2[Fe(CN)6].
Реакции протекают по уравнениям:
В 60-е годы XX века в СССР азотнокислый уранил свободно продавался в фотомагазинах. Входил в состав промышленно выпускаемых усилителей, применяемых в фотопечати, в частности, ОРВО 604.
Литература
- К. И. Мархилевич, В. А. Яштолд-Говорко. Фотографическая химия. М., Искусство, 1956.
- А. Г. Волгин. Фотография. 1000 рецептов. М., Химия, 1993
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |
![{\displaystyle ~{\mathsf {4Ag+4K_{3}[Fe(CN)_{6}]=3K_{4}[Fe(CN)_{6}]+Ag_{4}[Fe(CN)_{6}]}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/e25cac3151f07df8b8298bd80fe380c10b7a3b20)
![{\displaystyle ~{\mathsf {Ag_{4}[Fe(CN)_{6}]+2UO_{2}(NO_{3})_{2}=4AgNO_{3}+(UO_{2})_{2}[Fe(CN)_{6}]}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/d764af46e199eae26f819169583d71d4ed96b2f4)
