Благородные газы: различия между версиями
| [непроверенная версия] | [отпатрулированная версия] |
Ping08 (обсуждение | вклад) отмена правки 93725281 участника 188.0.175.221 (обс.)? Метка: отмена |
|||
| Строка 39: | Строка 39: | ||
== Химические свойства == |
== Химические свойства == |
||
[[Файл:Electron shell 010 Neon - no label.svg|thumb|Неон, как и все благородные газы, имеет полную [[электронная оболочка|электронную оболочку]]. Все атомы благородных газов имеют на внешней орбите 8 электронов. Исключением является гелий (только 2 электрона)|alt=An atomic shell diagram with neon core, 2 electrons in the inner shell and 8 in the outer shell. |
[[Файл:Electron shell 010 Neon - no label.svg|thumb|Неон, как и все благородные газы, имеет полную [[электронная оболочка|электронную оболочку]]. Все атомы благородных газов имеют на внешней орбите 8 электронов. Исключением является гелий (только 2 электрона)|alt=An atomic shell diagram with neon core, 2 electrons in the inner shell and 8 in the outer shell.]] |
||
Благородные газы не имеют цвета, запаха, вкуса, а также не возгораются при нормальных условиях |
Благородные газы не имеют цвета, запаха, вкуса, а также не возгораются при нормальных условиях. <!-- They were once labeled ''group 0'' in the periodic table because it was believed they had a [[valence (chemistry)|valence]] of zero, meaning their [[atom]]s cannot combine with those of other elements to form [[chemical compound|compounds]]. However, it was later discovered some do indeed form compounds, causing this label to fall into disuse.<ref name="brit" /> |
||
Like other groups, the members of this family show patterns [[electron configuration]], especially the outermost shells resulting in trends in chemical behavior:--> |
|||
{| class="wikitable" border="1" cellpadding="3" cellspacing="0" |
|||
|- |
|||
![[Атомный номер|№]] !! [[Химический элемент|Элемент]] !! № электронов/[[Электронная оболочка|электронной оболочки]] |
|||
|- |
|||
| 2 || [[гелий]] || 2 |
|||
|- |
|||
| 10 || [[неон]] || 2, 8 |
|||
|- |
|||
| 18 || [[аргон]] || 2, 8, 8 |
|||
|- |
|||
| 36 || [[криптон]] || 2, 8, 18, 8 |
|||
|- |
|||
| 54 || [[ксенон]] || 2, 8, 18, 18, 8 |
|||
|- |
|||
| 86 || [[радон]] || 2, 8, 18, 32, 18, 8<!--не добавляйте унуноктий (оганесон), т.к до сих пор неизвестна его электронная оболочка и относится ли он к благородным газам вообще--> |
|||
|} |
|||
=== Соединения === |
|||
[[Файл:Xenon-tetrafluoride-3D-vdW.png|thumb|left|Структура [[тетрафторид ксенона|тетрафторида ксенона]] XeF<sub>4</sub>, одного из первых когда-либо обнаруженных соединений благородных газов|alt=Структура XeF<sub>4</sub>, одного из первых когда-либо обнаруженных соединений благородных газов]] |
|||
{{main|Соединения благородных газов}} |
|||
Инертные газы отличаются химической неактивностью (отсюда и название). Тем не менее, в 1962 году [[Бартлетт, Нил|Нил Барлетт]] показал, что все они при определённых условиях могут образовывать [[соединения благородных газов|соединения]] (особенно охотно со [[фтор]]ом). Наиболее «инертны» неон и гелий: чтобы заставить их вступить в реакцию, нужно применить много усилий, искусственно ионизируя каждый атом. Ксенон же, наоборот, слишком активен (для инертных газов) и реагирует даже при [[Нормальные условия|нормальных условиях]], демонстрируя чуть ли не все возможные степени окисления (+1, +2, +4, +6, +8). [[Радон]] тоже имеет высокую химическую активность (по сравнению с лёгкими инертными газами), но он радиоактивен и быстро распадается, поэтому подробное изучение его химических свойств осложнено, в отличие от ксенона. |
Инертные газы отличаются химической неактивностью (отсюда и название). Тем не менее, в 1962 году [[Бартлетт, Нил|Нил Барлетт]] показал, что все они при определённых условиях могут образовывать [[соединения благородных газов|соединения]] (особенно охотно со [[фтор]]ом). Наиболее «инертны» неон и гелий: чтобы заставить их вступить в реакцию, нужно применить много усилий, искусственно ионизируя каждый атом. Ксенон же, наоборот, слишком активен (для инертных газов) и реагирует даже при [[Нормальные условия|нормальных условиях]], демонстрируя чуть ли не все возможные степени окисления (+1, +2, +4, +6, +8). [[Радон]] тоже имеет высокую химическую активность (по сравнению с лёгкими инертными газами), но он радиоактивен и быстро распадается, поэтому подробное изучение его химических свойств осложнено, в отличие от ксенона. |
||
| Строка 47: | Строка 70: | ||
== Физические свойства == |
== Физические свойства == |
||
[[Файл:First Ionization Energy.svg|lang=ru|thumb| |
[[Файл:First Ionization Energy.svg|lang=ru|thumb|270px|right|Инертные газы имеют самые большие [[Энергия ионизации|энергии ионизации]].]] |
||
В небольшом количестве они присутствуют в [[воздух]]е и некоторых [[горная порода|горных породах]], а также в атмосферах некоторых [[Планеты-гиганты|планет-гигантов]] и планет земной группы |
Инертные газы [[Цвет|бесцветны]] и не имеют [[запах]]а. В небольшом количестве они присутствуют в [[воздух]]е и некоторых [[горная порода|горных породах]], а также в атмосферах некоторых [[Планеты-гиганты|планет-гигантов]] и планет земной группы |
||
== Биологическое действие == |
== Биологическое действие == |
||
| Строка 58: | Строка 81: | ||
== Применение == |
== Применение == |
||
[[Файл:Glowing noble gases.jpg|мини|350px|справа|Благородные газы в вакуумных стеклянных колбах, через которые пропущен ток]] |
|||
Инертные газы имеют очень низкие точки кипения и плавления, что позволяет их использовать в качестве [[холодильный агент|холодильного агента]] в [[криогенная техника|криогенной технике]]. [[Жидкий гелий]], который кипит при {{nobr|4,2 К}} {{nobr|(−268,95 °C)}}, используется для получения сверхпроводимости — в частности, для охлаждения [[Сверхпроводник|сверхпроводящих]] обмоток электромагнитов, применяемых, например, для [[Магнитно-резонансная томография|магнитно-резонансной томографии]] и других приложений [[Ядерный магнитный резонанс|ядерного магнитного резонанса]]. Жидкий неон, хотя его температура кипения {{nobr|(–246,03 °C)}} и не достигает таких низких значений как у жидкого гелия, также находит применение в криогенике, потому что его охлаждающие свойства (удельная теплота испарения) более чем в 40 раз лучше, чем у жидкого гелия, и более чем в три раза лучше, чем у жидкого водорода. |
Инертные газы имеют очень низкие точки кипения и плавления, что позволяет их использовать в качестве [[холодильный агент|холодильного агента]] в [[криогенная техника|криогенной технике]]. [[Жидкий гелий]], который кипит при {{nobr|4,2 К}} {{nobr|(−268,95 °C)}}, используется для получения сверхпроводимости — в частности, для охлаждения [[Сверхпроводник|сверхпроводящих]] обмоток электромагнитов, применяемых, например, для [[Магнитно-резонансная томография|магнитно-резонансной томографии]] и других приложений [[Ядерный магнитный резонанс|ядерного магнитного резонанса]]. Жидкий неон, хотя его температура кипения {{nobr|(–246,03 °C)}} и не достигает таких низких значений как у жидкого гелия, также находит применение в криогенике, потому что его охлаждающие свойства (удельная теплота испарения) более чем в 40 раз лучше, чем у жидкого гелия, и более чем в три раза лучше, чем у жидкого водорода. |
||
| Строка 66: | Строка 90: | ||
Аргон, наиболее дешёвый среди инертных газов (его содержание в атмосфере составляет около 1 %), широко используется при сварке в защитных газах, резке и других приложениях для изоляции от воздуха металлов, реагирующих при нагреве с кислородом (и азотом), а также для обработки жидкой стали. Аргон также применяется в [[Люминесцентная лампа|люминесцентных лампах]] для предотвращения окисления разогретого [[вольфрам]]ового электрода. Также, ввиду низкой теплопроводности, аргон (а также криптон) используют для заполнения стеклопакетов. |
Аргон, наиболее дешёвый среди инертных газов (его содержание в атмосфере составляет около 1 %), широко используется при сварке в защитных газах, резке и других приложениях для изоляции от воздуха металлов, реагирующих при нагреве с кислородом (и азотом), а также для обработки жидкой стали. Аргон также применяется в [[Люминесцентная лампа|люминесцентных лампах]] для предотвращения окисления разогретого [[вольфрам]]ового электрода. Также, ввиду низкой теплопроводности, аргон (а также криптон) используют для заполнения стеклопакетов. |
||
После крушения [[Дирижабль|дирижабля]] [[Гинденбург (дирижабль)|«Гинденбург»]] в 1937 году негорючий гелий заменил огнеопасный водород в качестве заполняющего газа в дирижаблях и воздушных шарах, несмотря на снижение плавучести на 8,6 % по сравнению с водородом. Несмотря на замену, катастрофа оказала непропорционально большое влияние на всю область герметичных летательных аппаратов легче воздуха и подорвала планы по расширению этой области авиации более чем на полвека. Они стали популярнее только в последнее время, с развитием нановолоконных тканей и альтернативной энергетики. |
После крушения [[Дирижабль|дирижабля]] [[Гинденбург (дирижабль)|«Гинденбург»]] в 1937 году негорючий гелий заменил огнеопасный водород в качестве заполняющего газа в дирижаблях и воздушных шарах, несмотря на снижение плавучести на 8,6 % по сравнению с водородом. Несмотря на замену, катастрофа оказала непропорционально большое влияние на всю область герметичных летательных аппаратов легче воздуха и подорвала планы по расширению этой области авиации более чем на полвека. Они стали популярнее только в последнее время, с развитием нановолоконных тканей и альтернативной энергетики. |
||
== Цвета и спектры благородных газов == |
== Цвета и спектры благородных газов == |
||
<center> |
<center> |
||
Версия от 10:49, 3 июля 2018
| Группа → | 18 | ||||||
|---|---|---|---|---|---|---|---|
| ↓ Период | |||||||
| 1 |
| ||||||
| 2 |
| ||||||
| 3 |
| ||||||
| 4 |
| ||||||
| 5 |
| ||||||
| 6 |
| ||||||
| 7 |
| ||||||
Благоро́дные га́зы (также ине́ртные или ре́дкие га́зы[1]) — группа химических элементов со схожими свойствами: при нормальных условиях они представляют собой одноатомные газы без цвета, запаха и вкуса с очень низкой химической реактивностью[англ.]. К благородным газам относятся гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радиоактивный радон (Rn). Формально к этой группе также причисляют недавно открытый оганесон (Og), однако его химические свойства почти не исследованы.
В первых 6 периодах периодической таблицы химических элементов инертные газы относятся к последней, 18-й группе. Возможно, что из-за релятивистских эффектов элемент 7-го периода 14-й группы флеровий обладает некоторыми свойствами благородных газов[2]. Он может заменить в периодической таблице оганесон[3]. Благородные газы химически неактивны и способны участвовать в химических реакциях лишь при экстремальных условиях.
Характеристики благородных газов объяснены современными теориями структуры атома: их электронные оболочки из валентных электронов являются заполненными, тем самым позволяя участвовать лишь в очень малом количестве химических реакций: известны всего несколько сотен химических соединений этих элементов. При нормальном давлении температуры плавления и кипения у любого благородного газа отличаются менее чем на 10 °C; таким образом, они остаются жидкими лишь в малом температурном интервале.
Неон, аргон, криптон и ксенон выделяют из воздуха специальными установками, используя при этом методы сжижения газов и фракционированной конденсации. Источником гелия являются месторождения природного газа с высокой концентрацией гелия, который отделяется с помощью методов криогенного разделения газов. Радон обычно получают как продукт радиоактивного распада радия из растворов соединений этого элемента.
Химические свойства

Благородные газы не имеют цвета, запаха, вкуса, а также не возгораются при нормальных условиях.
| № | Элемент | № электронов/электронной оболочки |
|---|---|---|
| 2 | гелий | 2 |
| 10 | неон | 2, 8 |
| 18 | аргон | 2, 8, 8 |
| 36 | криптон | 2, 8, 18, 8 |
| 54 | ксенон | 2, 8, 18, 18, 8 |
| 86 | радон | 2, 8, 18, 32, 18, 8 |
Соединения
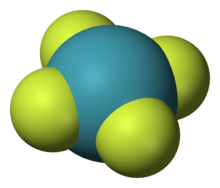
Инертные газы отличаются химической неактивностью (отсюда и название). Тем не менее, в 1962 году Нил Барлетт показал, что все они при определённых условиях могут образовывать соединения (особенно охотно со фтором). Наиболее «инертны» неон и гелий: чтобы заставить их вступить в реакцию, нужно применить много усилий, искусственно ионизируя каждый атом. Ксенон же, наоборот, слишком активен (для инертных газов) и реагирует даже при нормальных условиях, демонстрируя чуть ли не все возможные степени окисления (+1, +2, +4, +6, +8). Радон тоже имеет высокую химическую активность (по сравнению с лёгкими инертными газами), но он радиоактивен и быстро распадается, поэтому подробное изучение его химических свойств осложнено, в отличие от ксенона.
Оганесон, несмотря на его принадлежность к 18-й группе периодической таблицы, может не являться инертным газом, так как предполагается, что при нормальных условиях в силу релятивистских эффектов, влияющих на движение электронов вблизи его ядра с высоким зарядом, он будет находиться в твердом состоянии[4].
Физические свойства

Инертные газы бесцветны и не имеют запаха. В небольшом количестве они присутствуют в воздухе и некоторых горных породах, а также в атмосферах некоторых планет-гигантов и планет земной группы
Биологическое действие
Инертные газы не ядовиты. Однако атмосфера с увеличенной концентрацией инертных газов и соответствующим снижением концентрации кислорода может оказывать удушающее действие на человека, вплоть до потери сознания и смерти[5][6]. Известны случаи гибели людей при утечках инертных газов.
Вдыхание значительного количества радиоактивного радона может вызвать рак.
Инертные газы обладают биологическим действием, которое проявляется в их наркотическом воздействии на организм и по силе этого воздействия располагаются по убыванию в следующем порядке (в сравнении приведены также азот и водород): Xe — Кr — Ar — N2 — H2 — Ne — He. При этом ксенон и криптон проявляют наркотический эффект при нормальном барометрическом давлении, аргон — при давлении свыше 0,2 МПа (2 атм), азот — свыше 0,6 МПа (6 атм), водород — свыше 2,0 МПа (20 атм). Наркотическое действие неона и гелия в опытах не регистрируются, так как под давлением раньше возникают симптомы «нервного синдрома высокого давления» (НСВД)[7].
Применение

Инертные газы имеют очень низкие точки кипения и плавления, что позволяет их использовать в качестве холодильного агента в криогенной технике. Жидкий гелий, который кипит при 4,2 К (−268,95 °C), используется для получения сверхпроводимости — в частности, для охлаждения сверхпроводящих обмоток электромагнитов, применяемых, например, для магнитно-резонансной томографии и других приложений ядерного магнитного резонанса. Жидкий неон, хотя его температура кипения (–246,03 °C) и не достигает таких низких значений как у жидкого гелия, также находит применение в криогенике, потому что его охлаждающие свойства (удельная теплота испарения) более чем в 40 раз лучше, чем у жидкого гелия, и более чем в три раза лучше, чем у жидкого водорода.
Гелий, благодаря его пониженной растворимости в жидкостях, особенно в липидах, используется вместо азота как компонент дыхательных смесей для дыхания под давлением (например, при подводном плавании). Растворимость газов в крови и биологических тканях растёт под давлением. В случае использования для дыхания обычного воздуха или других азотсодержащих дыхательных смесей это может стать причиной эффекта, известного как азотное отравление.
Благодаря меньшей растворимости в липидах, атомы гелия задерживаются клеточной мембраной, и поэтому гелий используется в дыхательных смесях, таких как тримикс и гелиокс, уменьшая наркотический эффект газов, возникающий на глубине. Кроме того, пониженная растворимость гелия в жидкостях тела позволяет избежать кессонной болезни при быстром всплытии с глубины. Уменьшение остатка растворённого газа в теле означает, что во время всплытия образуется меньшее количество газовых пузырьков; это уменьшает риск газовой эмболии. Другой инертный газ, аргон, рассматривается как лучший выбор для использования в качестве прослойки к сухому костюму[8][неавторитетный источник] для подводного плавания.
Аргон, наиболее дешёвый среди инертных газов (его содержание в атмосфере составляет около 1 %), широко используется при сварке в защитных газах, резке и других приложениях для изоляции от воздуха металлов, реагирующих при нагреве с кислородом (и азотом), а также для обработки жидкой стали. Аргон также применяется в люминесцентных лампах для предотвращения окисления разогретого вольфрамового электрода. Также, ввиду низкой теплопроводности, аргон (а также криптон) используют для заполнения стеклопакетов.
После крушения дирижабля «Гинденбург» в 1937 году негорючий гелий заменил огнеопасный водород в качестве заполняющего газа в дирижаблях и воздушных шарах, несмотря на снижение плавучести на 8,6 % по сравнению с водородом. Несмотря на замену, катастрофа оказала непропорционально большое влияние на всю область герметичных летательных аппаратов легче воздуха и подорвала планы по расширению этой области авиации более чем на полвека. Они стали популярнее только в последнее время, с развитием нановолоконных тканей и альтернативной энергетики.
Цвета и спектры благородных газов
| Форма | Гелий | Неон | Аргон | Криптон | Ксенон |
| В колбе под действием электричества | 
|

|

|

|

|
| В прямой трубке | 
|

|

|

|

|
| В трубках-литерах Периодической таблицы | 
|

|

|

|

|
| Cпектр поглощения газа |
См. также
Примечания
- ↑ Благородные газы — статья из Химической энциклопедии
- ↑ Flerov laboratory of nuclear reactions. JINR. Дата обращения: 8 августа 2009.
- ↑ Nash, Clinton S. (2005). "Atomic and Molecular Properties of Elements 112, 114, and 118". J. Phys. Chem. A. 109 (15): 3493—3500. doi:10.1021/jp050736o. PMID 16833687.
- ↑ Wieser M.E. (2006). "Atomic weights of the elements 2005 (IUPAC Technical Report)". Pure Appl. Chem. 78 (11): 2051—2066. doi:10.1351/pac200678112051.
- ↑ Опасности при работе с азотом и аргоном
- ↑ Инструкция по эксплуатации баллонов с аргоном используемых в спектральной лаборатории (недоступная ссылка)
- ↑ Павлов Б.Н. Проблема защиты человека в экстремальных условиях гипербарической среды обитания. www.argonavt.com (15 мая 2007). Дата обращения: 22 мая 2010. Архивировано 22 августа 2011 года.
- ↑ en:Dry_suit (англ.)
Литература
- Беннетт, Питер. The Physiology and Medicine of Diving / Питер Беннетт, Дэвид Эллиотт. — SPCK Publishing, 1998. — ISBN 0-7020-2410-4.
- Bobrow Test Preparation Services. CliffsAP Chemistry. — CliffsNotes, 2007-12-05. — ISBN 0-470-13500-X.
- Гринвуд, Н.Н. Chemistry of the Elements / Н.Н. Гринвуд, A. Ёрншо. — 2nd. — Oxford:Butterworth-Heinemann, 1997. — ISBN 0-7506-3365-4.
- Хардинг, Чарли Дж. Elements of the P Block / Чарли Дж. Хардинг, Роб Джейнс. — Royal Society of Chemistry, 2002. — ISBN 0-85404-690-9.
- Холловэй, Джон. Noble-Gas Chemistry. — Лондон : Methuen Publishing, 1968. — ISBN 0-412-21100-9.
- Менделеев, Дмитрий. Основы Химии : []. — 7-е. — 1902–1903.
- Оджима, Минору. Ошибка: не задан параметр
|заглавие=в шаблоне {{публикация}}. — Cambridge University Press, 2002. — ISBN 0-521-80366-7. - Вайнхольд, Ф. Valency and bonding / Ф. Вайнхольд, C. Лэндис. — Cambridge University Press, 2005. — ISBN 0-521-83128-8.
- Скерри, Эрик. The Periodic Table, Its Story and Its Significance. — Oxford University Press, 2007. — ISBN 0-19-530573-6.
Ссылки
В другом языковом разделе есть более полная статья Noble gas (англ.). |