Фавипиравир
| Фавипиравир | |
|---|---|
 | |
| Химическое соединение | |
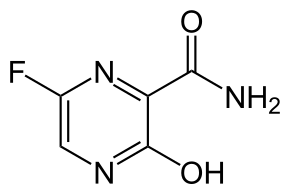
| ИЮПАК | 6-фторо-3-гидроксипиразин-2-карбоксамид |
| Брутто-формула | C5H4FN3O2 |
| Молярная масса | 157,104 г/моль |
| CAS | 259793-96-9 |
| PubChem | 492405 |
| DrugBank | DB12466 |
| Состав | |
| Классификация | |
| АТХ | J05AX27 |
| Способы введения | |
| перорально | |
| Другие названия | |
| Фавилавир, Авифавир, Авиган, Арепливир, Коронавир, T-705 | |
Фавипирави́р — противовирусный препарат, разработанный в Японии для лечения гриппа[1]. Обладает широким спектром активности против РНК-содержащих вирусов, включая вирусы гриппа, риновирус, респираторно-синцитиальный вирус, а также опасные для жизни вирусы. Не работает против ДНК-содержащих вирусов, в числе которых аденовирус, вирус простого герпеса первого типа и цитомегаловирус. Принцип действия основан на ингибировании вирусной РНК-зависимой РНК-полимеразы путём терминирования удлинения формирующейся цепи РНК[2], но касательно механизма действия есть и другие мнения.
Фавипиравир изучается как потенциальное средство для лечения ряда других вирусных инфекций, в том числе коронавирусной инфекции COVID-19. Как и экспериментальные противовирусные препараты Т-1105 и Т-1106, это производное противотуберкулёзного препарата пиразинкарбоксамида[1].
Препарат показал активность против многих вирусов в лабораторных условиях и эффективность в испытаниях на животных. Среди людей использовался против опасных для жизни вирусов лихорадок Эбола и Ласса, вирусов бешенства и тяжелой лихорадки с синдромом тромбоцитопении[англ.]. Пока отсутствуют штаммы, выработавшие устойчивость к препарату[2].
Торговые наименования: «Фавилавир», «Авиган», «Авифавир». До получения международного названия фавипиравир обозначался индексом разработчика T-705[2]. Первые публикации о препарате появились в 2002 году[3].
История
Изначально в разработавшей препарат компании Toyama Chemical надеялись, что фавипиравир станет новым лекарством от гриппа, которое может заменить осельтамивир, но эксперименты на животных показали, что он может негативно влиять на ДНК будущего ребёнка с риском повреждения плода, поэтому одобрение данного препарата Министерством здравоохранения, труда и социального обеспечения Японии было отложено на неопределённый срок[4].
В 2014 году фавипиравир был одобрен в Японии в качестве препарата против пандемии гриппа[5] — ограниченно разрешён для лечения гриппа A и B, вызванного резистентными к противовирусным препаратам штаммами[6], и не предназначен для лечения сезонного гриппа. По состоянию на 2020 год вероятность развития резистентности вируса гриппа к препарату остаётся низкой[7].
15 марта 2020 года препарат был разрешён к продаже в Китае для лечения гриппа[8]. 30 мая 2020 года фавипиравир, выпускаемый под торговым наименованием «Авифавир» на совместном предприятии «ХимРара» и РФПИ, зарегистрирован в России как лекарство от коронавирусной инфекции[9].
Механизм действия
О механизме действия фавипиравира есть разные мнения. Одни исследователи считают, что фавипиравир селективно ингибирует вирусную РНК-зависимую РНК-полимеразу[10]. Другие исследования показывают, что фавипиравир индуцирует летальные мутации РНК-трансверсии, производя нежизнеспособный вирусный фенотип[11].
Также есть мнение, что фавипиравир как в пероральной, так и внутривенной формах является пролекарством, которое метаболизируется до его активной формы, фавипиравир-рибофуранозил-5'-трифосфат (фавипиравир-RTP)[12][13]. Считается, что человеческая гипоксантин-гуанин-фосфорибозилтрансфераза (HGPRT) играет ключевую роль в процессе его активации[14].
Побочные эффекты
Существуют доказательства того, что употребление во время беременности может нанести вред ребёнку[7].
Эффективность и безопасность
Для фавипиравира нет клинических доказательств эффективности при лечении гриппа[15].
Фавипиравир нетоксичен для млекопитающих, поскольку не ингибирует синтез РНК или ДНК в их клетках[16].
Исследования
Фавипиравир изучался в качестве потенциального средства лечения COVID-19: в Китае в феврале 2020[17][18], в марте — в Японии[19]. До этого в декабре 2019 года было опубликовано китайское исследование, ограничением данного исследования было то, что оно не было рандомизированно двойным слепым и плацебо-контролируемым[20][21]. В марте 2020 года начались испытания в Италии[22]. Итальянское фармацевтическое агентство, однако, напомнило общественности, что имеющиеся доказательства в поддержку этого препарата скудны и предварительны[23]. 21 мая 2020 года Минздрав России одобрил финальный этап (n=330[24]) испытаний лекарства «Авифавир», так как по итогам первого десятидневного этапа клинических исследований препарат продемонстрировал безопасность и не было выявлено никаких новых побочных эффектов[25][26]; 29 мая того же года препарат был зарегистрирован для использования в условиях стационара[27].
В 2014 году некоторые исследователи высказывали предположение о потенциале фавипиравира для лечения геморрагической лихорадки Эболы[28][29]. Но проведённое впоследствии клиническое исследование в Гвинее имеет серьёзные недостатки методики и ничего не доказывает[30].
In vitro и на животных также была замечена некоторая эффективность фавипиравира против вируса бешенства[31], однако, будучи однажды экспериментально применён у человека, он не спас пациента от смерти[32].
Примечания
- ↑ 1 2 Yin‐Xiao Du, Xiao‐Ping Chen. Favipiravir: pharmacokinetics and concerns about clinical trials for 2019-nCoV infection (англ.) // Clinical pharmacology and therapeutics[англ.]. — 2020. — 4 April. — doi:10.1002/cpt.1844. — PMID 32246834.
- ↑ 1 2 3 Kimiyasu Shiraki, Tohru Daikoku. Favipiravir, an anti-influenza drug against life-threatening RNA virus infections (англ.) // Pharmacology & Therapeutics. — 2020. — May (vol. 209). — P. 107512. — ISSN 0163-7258. — doi:10.1016/j.pharmthera.2020.107512. — PMID 32097670.
- ↑ Furuta, Y. In Vitro and In Vivo Activities of Anti-Influenza Virus Compound T-705 : [англ.] / Y. Furuta, K. Takahashi, Y. Fukuda … [et al.] // Antimicrobial Agents and Chemotherapy. — 2002. — Vol. 46, no. 4. — P. 977—981. — doi:10.1128/AAC.46.4.977-981.2002. — PMID 11897578. — PMC 127093.

- ↑ 条件付き承認で普及に足かせ 富山化学インフル薬の"無念" (яп.). diamond.jp. Дата обращения: 25 февраля 2014.
- ↑ Koons, Cynthia. Ebola Drug From Japan May Emerge Among Key Candidates : [англ.] // Bloomberg : [электр. ресурс]. — 2014. — 7 August.
- ↑ Hayden F. G., Shindo N. Influenza virus polymerase inhibitors in clinical development (англ.) // Current Opinion in Infectious Diseases[англ.]. — Lippincott Williams & Wilkins[англ.], 2019. — Vol. 32, no. 2. — P. 176—186. — doi:10.1097/QCO.0000000000000532. — PMID 30724789.

- ↑ 1 2 Kimiyasu Shiraki, Tohru Daikoku. Favipiravir, an anti-influenza drug against life-threatening RNA virus infections (англ.) // Pharmacology & therapeutics : journal. — 2020. — 22 February (vol. 209). — P. 107512. — doi:10.1016/j.pharmthera.2020.107512. — PMID 32097670.
- ↑ Zhang Yangfei. Potential coronavirus drug approved for marketing (англ.). China Daily. Дата обращения: 21 марта 2020.
- ↑ Константин Журавлёв. Минздрав одобрил препарат РФПИ и «ХимРара» от коронавируса. Газета.ру (30 мая 2020).
- ↑ Jin Z. et al. The ambiguous base-pairing and high substrate efficiency of T-705 (Favipiravir) Ribofuranosyl 5'-triphosphate towards influenza A virus polymerase (англ.) // PLOS One : journal. — Public Library of Science, 2013. — Vol. 8, no. 7. — P. e68347. — doi:10.1371/journal.pone.0068347. — . — PMID 23874596.
- ↑ Baranovich T. et al. T-705 (favipiravir) induces lethal mutagenesis in influenza A H1N1 viruses in vitro (англ.) // Journal of Virology[англ.] : journal. — 2013. — April (vol. 87, no. 7). — P. 3741—3751. — doi:10.1128/JVI.02346-12. — PMID 23325689.
- ↑ Guedj J. et al. Antiviral efficacy of favipiravir against Ebola virus: A translational study in cynomolgus macaques (англ.) // PLOS Medicine[англ.] : journal. — 2018. — March (vol. 15, no. 3). — P. e1002535. — doi:10.1371/journal.pmed.1002535. — PMID 29584730.
- ↑ Smee D. F. et al. Intracellular metabolism of favipiravir (T-705) in uninfected and influenza A (H5N1) virus-infected cells (англ.) // The Journal of Antimicrobial Chemotherapy[англ.] : journal. — 2009. — October (vol. 64, no. 4). — P. 741—746. — doi:10.1093/jac/dkp274. — PMID 19643775.
- ↑ Naesens L. et al. Role of human hypoxanthine guanine phosphoribosyltransferase in activation of the antiviral agent T-705 (favipiravir) (англ.) // Molecular Pharmacology[англ.] : journal. — 2013. — October (vol. 84, no. 4). — P. 615—629. — doi:10.1124/mol.113.087247. — PMID 23907213.
- ↑ Jeong-Joong Yoon et al. Orally Efficacious Broad-Spectrum Ribonucleoside Analog Inhibitor of Influenza and Respiratory Syncytial Viruses (англ.) // Antimicrobial Agents and Chemotherapy[англ.] : journal. — 2018. — August (vol. 62, no. 8). — P. e00766–18. — doi:10.1128/AAC.00766-18. — PMID 29891600.
- ↑ T-705 (favipiravir) and related compounds: Novel broad-spectrum inhibitors of RNA viral infections (англ.) // Antiviral Research[англ.] : journal. — 2009. — June (vol. 82, no. 3). — P. 95—102. — doi:10.1016/j.antiviral.2009.02.198. — PMID 19428599.
- ↑ Li G., De Clercq E. Therapeutic options for the 2019 novel coronavirus (2019-nCoV) (англ.) // Nature Reviews Drug Discovery. — 2020. — Vol. 19, iss. February. — P. 149—150. — doi:10.1038/d41573-020-00016-0.

- ↑ Brief -Corrected — Zhejiang Hisun Pharma gets approval for clinical trial to test flu drug Favipiravir for pneumonia caused by new coronavirus. Reuters Healthcare, February 16, 2020.
- ↑ Fujifilm Announces the Start of a Phase III Clinical Trial of Influenza Antiviral Drug Avigan (favipiravir) on COVID-19 in Japan and Commits to Increasing Production (англ.). Drugs.com. Дата обращения: 12 апреля 2020.
- ↑ Cai Q. et al. Experimental Treatment with Favipiravir for COVID-19: An Open-Label Control Study (англ.) // Engineering : journal. — 2020. — 18 March. — ISSN 2095-8099. — doi:10.1016/j.eng.2020.03.007.
- ↑ Liying Dong, Shasha Hu, Jianjun Gao. Discovering drugs to treat coronavirus disease 2019 (COVID-19) (англ.) // Drug Discoveries & Therapeutics : journal. — 2020. — Vol. 14, no. 1. — P. 58—60. — doi:10.5582/ddt.2020.01012. — PMID 32147628.
- ↑ Coronavirus, il Veneto sperimenta l'antivirale giapponese Favipiravir. Ma l'Aifa: "Ci sono scarse evidenze scientifiche su efficacia" (итал.). Il Fatto Quotidiano (22 марта 2020). Дата обращения: 23 марта 2020.
- ↑ AIFA precisa, uso favipiravir per COVID-19 non autorizzato in Europa e USA, scarse evidenze scientifiche sull’efficacia (итал.). AIFA. Дата обращения: 23 марта 2020.
- ↑ https://www.pnp.ru/politics/chto-izvestno-o-zaregistrirovannom-dlya-lecheniya-covid-19-preparate-avifavir.html
- ↑ Первый эффективный российский препарат от COVID-19 назвали «Авифавир», 22 мая 2020
- ↑ Препарат против коронавируса «Фавипиравир» в РФ будет называться «Авифавир», 22 мая 2020
- ↑ Регистрационное удостоверение на Авифавир (англ.). Государственный реестр лекарственных средств (29 мая 2020). Дата обращения: 31 мая 2020.
- ↑ Gatherer D. The 2014 Ebola virus disease outbreak in West Africa (англ.) // Journal of General Virology[англ.]. — Microbiology Society[англ.], 2014. — August (vol. 95, no. Pt 8). — P. 1619—1624. — doi:10.1099/vir.0.067199-0. — PMID 24795448.

- ↑ Smither S. J. et al. Post-exposure efficacy of oral T-705 (Favipiravir) against inhalational Ebola virus infection in a mouse model (англ.) // Antiviral Research[англ.]. — 2014. — April (vol. 104). — P. 153—155. — doi:10.1016/j.antiviral.2014.01.012. — PMID 24462697.
- ↑ Cohen J. Results from encouraging Ebola trial scrutinized : [англ.] // Science Insider : электр. ресурс. — 2015. — 26 February. — doi:10.1126/science.aaa7912.
- ↑ Yamada K. et al. Efficacy of Favipiravir (T-705) in Rabies Postexposure Prophylaxis (англ.) // The Journal of Infectious Diseases. — 2016. — April (vol. 213, no. 8). — P. 1253—1261. — doi:10.1093/infdis/jiv586. — PMID 26655300.
- ↑ Murphy J. et al. Human Rabies – Virginia, 2017 (англ.) // MMWR. Morbidity and Mortality Weekly Report?! : journal. — 2019. — January (vol. 67, no. 5152). — P. 1410—1414. — doi:10.15585/mmwr.mm675152a2. — PMID 30605446.
Ссылки
- Favipiravir. Drug Information Portal. U.S. National Library of Medicine.
- Авифавир. Справочник лекарственных препаратов Medum.ru. Медум.ру.