Ацетали

Ацета́ли — простые эфиры гем-диолов общей формулы R₂C(OR¹)(OR²), где R¹ и R² — углеводородные радикалы: CH3, C2H5 и др. Первоначально к ацеталям относили производные альдегидов RCH(OR¹)(OR²), а аналогичные производные кетонов именовались кеталями R—C(R¹)(OR²)(OR³), однако в настоящее время в номенклатуре IUPAC для обоих классов соединений рекомендуется название «ацетали».[1].
Если один из R¹ или R² представляет собой атом водорода, то такие соединения R₂C(OH)OR′ (R′ ≠ H) называют полуацеталями (полуацеталями)[2].
Свойства и реакционная способность
Низшие ацетали — жидкости приятного фруктового запаха, растворимые в органических растворителях и нерастворимые в воде.
Ацетали устойчивы в щелочных средах, однако в присутствии кислот легко гидролизуются водой с образованием альдегидов и спиртов, производными которых они являются. Полуацетали, как правило, ещё легче подвержены гидролизу и в растворах находятся в равновесии с исходным альдегидом и спиртом.
Такое поведение ацеталей и полуацеталей — как и их образование из карбонильных соединений — обусловлено общим механизмом кислотного катализа с образованием резонансно стабилизированного α-атомом кислорода карбокатиона:
Все эти реакции обратимы, и положение равновесия может быть сдвинуто удалением из реакционной смеси какого-либо компонента. Другим следствием обратимости реакций ацеталей в условиях кислотного катализа, идущих с образованием карбокатионов, являются реакции переацетализации:
Переацетализация происходит при взаимодействии ацеталей не только со спиртами, но и при реакции с тиолами и ведет в последнем случае к образованию дитиоацеталей R2C(SR)2.
В реакциях с азотистыми нуклеофилами ацетали выступают как функциональные аналоги исходных карбонильных соединений: так, в реакциях ацеталей с первичными аминами, гидразинами и гидроксиламином образуются имины, гидразоны и оксимы:
- R'' = Alk, Ar (имины), NR2 (гидразоны), OH (оксимы)
При взаимодействии вторичных аминов с ацеталями — функциональными аналогами енолизирующихся альдегидов и кетонов образуются енамины:
Синтез
Основным препаративным методом синтеза ацеталей является взаимодействие альдегидов и кетонов со спиртами либо ортоэфирами в условиях кислотного катализа:
В качестве эквивалента диола в таком синтезе ацеталей могут выступать эпоксиды:
Ацетали также могут быть синтезированы присоединением спиртов к виниловым эфирам и их гомологам:
Замещение галогена в алифатических гем-дагалогенидах и α-галогенэфирах алкоголятами и фенолятами также ведет к ацеталям:
такой метод синтеза — взимодействие этилидендибромида с этилатом натрия — был использован Вюрцем и Фраполли для доказательства строения диэтилацеталя уксусного альдегида, полученного в 1833 году Деберейнером при окисления этанола над платиновой чернью[3]
Биологическое значение
Образование полуацеталей и ацеталей имеет чрезвычайно важное значение в химии углеводов, являющихся полигидроксиальдегидами (альдозы) и полигидроксикетонами (кетозы).
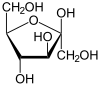
Такое сочетание гидроксильных и карбонильных функций в одной молекуле ведет к тому, что моносахариды могут существовать и в линейной форме, и, за счет внутримолекулярного образования полуацеталей, в циклической:
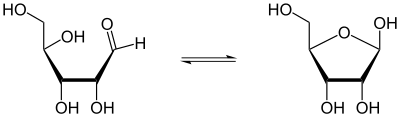
Линейная (оксо-) и циклическая полуацетальная (фуранозная) формы рибозы
В водных растворах линейные оксоформы и циклические полуацетальные формы моносахаридов, являющиеся динамическими структурными изомерами, находятся равновесии, то есть являются таутомерами. Таутомерия этого типа получила название цикло-оксо таутомерии.
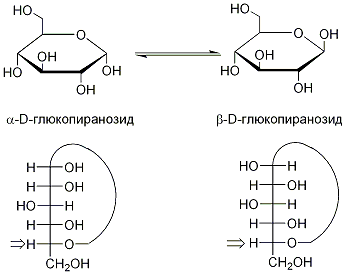
В свою очередь, циклические полуацетальные формы моносахаридов могут существовать в виде двух стереоизомерных аномерных форм, образующихся вследствие образования циклических полуацеталей при нуклеофильной атаки гидроксила с различных сторон карбонильной группы:
Циклические полуацетальные формы моноз способны образовывать полные ацетали с различными соединениями: так, образование смешанных ацеталей с другими монозами ведет к образованию сахаридов — обширного класса природных соединений, включающих как низкомолекулярные ди- и олигосахариды, так и высокомолекулярные полисахариды (целлюлоза, хитин и др.):
Примечания
- ↑ acetals // IUPAC Gold Book
- ↑ hemiacetals // IUPAC Gold Book
- ↑ Ацеталь // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.