Имиды карбоновых кислот

Ими́ды карбо́новых кисло́т — соединения, содержащие группу -CO-NR-CO-, диацилпроизводные аммиака (R = H) или аминов[1]. Ациклические имиды — производные монокарбоновых кислот также называют диациламидами, большое значение в синтетической химии имеют циклические имиды дикарбоновых кислот.
Реакционная способность и химические свойства
Свойства и реакционная способность имидов сходны со свойствами амидов карбоновых кислот. Индуктивный эффект двух ацильных заместителей при атоме азота обуславливает большую кислотность атома водорода NH-группы, снижает нуклеофильность атомов азота и карбонильного кислорода, а также повышает электрофильность карбонильных атомов углерода ацильных групп по сравнению с амидами.
Реакции NH-группы
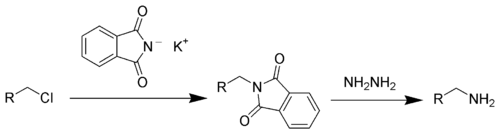
Имиды образуют соли с щелочными металлами, стабильные в спиртовых растворах, и которые легко алкилируются по атому азота алкилгалогенидами. Алкилирование калиевой соли фталимида алкилгалогенидами с последующим гидролизом образовавшегося N-алкилфталимида является классическим методом синтеза первичных аминов по Габриелю:
Имиды взаимодействуют с альдегидами и кетонами с образованием соответствующих аминокарбинолов:
- R'CONHCOR'' + R'''CHO R’CON(CHR'''OH)COR'
и в присутствии аминов вступают с ними в реакцию Манниха в качестве «кислотных» компонент:
- R’CONHCOR'' + CH2O + (CH3)2NH R'CON(CH2N(CH3)2)COR'
Имиды, подобно амидам, взаимодействуют с галогенами или гипогалогенитами с образованием N-галогенимидов, более стабильных, чем N-галогенамиды. Наиболее стабильны циклические N-галогенимиды, некоторые из которых (например, N-бромсукцинимид) используются в органическом синтезе в качестве источников галогена. N-галогенимиды под действием оснований претерпевают перегруппировку Гофмана с образованием изоцианатов. Так, реакция фталимида с гипохлоритом в щелочной среде ведёт к образованию антраниловой кислоты.
Реакции по карбонильной группе
Органические имиды широко применяют в синтезе гетероциклических соединений, аминов, аминокислот, пептидов.