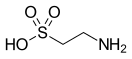
Таурин
| Таурин | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
2-Аминоэтансульфоновая кислота | ||
| Хим. формула | C2H7NO3S | ||
| Физические свойства | |||
| Молярная масса | 125,14 г/моль | ||
| Плотность | 1,734 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 305,0 °C | ||
| Классификация | |||
| Рег. номер CAS | 107-35-7 | ||
| PubChem | 1123 и 4068592 | ||
| Рег. номер EINECS | 203-483-8 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 15891 и 507393 | ||
| ChemSpider | 1091 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Таурин — серосодержащая аминокислота, образующаяся в организме из цистеина[1]. В небольших количествах присутствует в тканях и жёлчи животных, в том числе человека. Используется как пищевая добавка и в качестве лекарственного средства.
Название происходит от лат. taurus (бык), так как впервые был получен из бычьей жёлчи немецкими учёными Фридрихом Тидеманом и Леопольдом Гмелином в 1827 году[2].
Физические и химические свойства
Белый кристаллический порошок, плавится с разложением. Хорошо растворим в воде, плохо — в большинстве органических растворителей. Молекула таурина содержит кислую сульфогруппу SO3H (pK 1.5) и основную аминогруппу NH2 (pK 8.74), изоэлектрическая точка в водных растворах составляет 5.12[3]. В физиологических условиях (pH 7.4) степень ионизации сульфогруппы составляет 100 %, аминогруппы — 96,3 %, то есть таурин в таких условиях практически полностью существует в виде цвиттер-иона[4].
Биологическая роль
Таурин часто называют серосодержащей аминокислотой, хотя это не вполне верно с точки зрения современной химии, так как в молекуле отсутствует карбоксильная группа.
Таурин образуется в организме при ферментативном окислении сульфгидрильной группы SH цистеина с участием цистеиндеоксигеназы до цистеинсульфиновой кислоты:
- HSCH2CH(NH2)COOH HO2SCH2CH(NH2)COOH
последующим декарбоксилированием цистеинсульфиновой кислоты в гипотаурин:
- HO2SCH2CH(NH2)COOH HO2SCH2CH2NH2
и окислением гипотаурина в таурин:
- HO2SCH2CH2NH2 HO3SCH2CH2NH2
Таурин образует в печени конъюгаты с желчными кислотами (ацилируясь ими по аминогруппе), образовавшиеся конъюгаты (например, таурохолевая и тауродезоксихолевая кислоты) входят в состав желчи, и, будучи поверхностно-активными веществами, способствуют эмульгированию жиров в кишечнике.
В последнее время установлено, что в мозге таурин играет роль нейромедиаторной аминокислоты, тормозящей синаптическую передачу, обладает противосудорожной активностью, оказывает также кардиотропное действие. Таурин способствует улучшению энергетических процессов, стимулирует репаративные процессы при дистрофических заболеваниях и процессах, сопровождающихся значительным нарушением метаболизма тканей глаза.
Большинство млекопитающих способны к биосинтезу таурина, однако у кошек низка активность ферментативной системы, декарбоксилирующей цистеинсульфиновую кислоту и для них таурин является незаменимой аминокислотой, дефицит которой приводит к дегенерации сетчатки и кардиомиопатии[5].
Получение
В промышленном синтезе таурина исходным веществом является этаноламин — продукт крупнотоннажного органического синтеза.
На первой стадии этаноламин этерифицируется серной кислотой:
HOCH2CH2NH2 + H2SO4 HO3SOCH2CH2NH2
Затем под действием едкого натра этаноламинсульфат образует азиридин:
HO3SOCH2CH2NH2 + NaOH (CH2)2NH
На последней стадии проводится присоединение к азиридину сернистой кислоты под действием сульфита натрия в кислой среде:
(CH2)2NH + H2SO3 HO3SCH2CH2NH2
Основные мощности по производству таурина в настоящее время (2006 г.) находятся в Юго-Восточной Азии, уровень цен колеблется от 3 (Китай) до 5-12 долларов США за кг (Европа).
Применение
Используется в медицине и пищевой промышленности. В последние годы стал обычным компонентом «энергетических напитков» и продуктов спортивного питания.
В медицине
Таурин принимает участие в обмене липидов, улучшает энергетические и обменные процессы, входит в состав жёлчных кислот (таурохолиевой, тауродезоксихолевой), способствующих эмульгированию жиров в кишечнике. В центральной нервной системе выполняет функцию тормозящего нейромедиатора, обладает некоторой противосудорожной активностью. Способствует нормализации обменных процессов в тканях глаза при заболеваниях дистрофического характера.
В виде глазных капель таурин применяется при дистрофических поражениях сетчатки глаза, в том числе при наследственной тапеторетинальной дегенерации, при дистрофии роговицы, при старческой, диабетической, травматической и лучевой катаракте, при травмах роговицы.
Внутрь применяют при сердечно-сосудистой недостаточности, при отравлении сердечными гликозидами и при сахарном диабете первого и второго типа.
Таурин часто вводят в состав комплексных лекарственных препаратов. Основным действующим веществом он является в препаратах «Дибикор», «Тауфон», «Эрготекс».
Пищевая добавка
Используется, как одна из составляющих БАД, к пищевым продуктам (соки, также энергетические напитки), а также к кормам для животных. Для кошек является незаменимой аминокислотой и обязательно входит в состав кошачьих кормов, изготовленных из бедных таурином компонентов.
Таурин входит в состав сухих молочных смесей для вскармливания детей от 0 месяцев.
Примечания
- ↑ 1 2 Таурин (Taurine): инструкция, применение и формула. Энциклопедия лекарств и товаров аптечного ассортимента.
- ↑ F. Tiedemann, L. Gmelin (1827). "Einige neue Bestandtheile der Galle des Ochsen". Annalen der Physik. 85 (2): 326—37. doi:10.1002/andp.18270850214.
- ↑ Jacobsen, J.; Smith, L.; Biochemistry and Physiology of Taurine and Taurine Derviatives. Phys. Rev. 48; 1968
- ↑ Della Corte, L.; Taurine 4 : Taurine and Excitable Tissues; Advances in Experimental Medicine and Biology 483; Plenum Press; New York, 2000
- ↑ John Hilton. The Biosynthesis, Function and Deficiency Signs of Taurine in Cats. Can Vet J. 1988 July; 29(7): 598—599, 601.
- ↑ "Государственный реестр лекарственных средств. Том II. Часть 2. Типовые клинико-фармакологические статьи" (по состоянию на 1 апреля 2009 года) М., Издательство "Медицинский совет", 2009".
{{cite journal}}: Cite journal требует|journal=(справка)