Сульфурилхлорид
| Сульфурилхлорид | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Хлористый сульфурил |
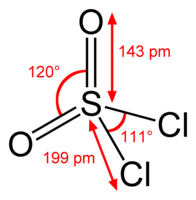
| Хим. формула | SO2Cl2 |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 134.965 г/моль |
| Плотность | 1.665 г/см³ |
| Поверхностное натяжение | 28,78 ± 0,01 мН/м[1] |
| Энергия ионизации | 12,05 эВ[2] |
| Термические свойства | |
| Температура | |
| • плавления | −54,7 °C |
| • кипения | 69,2 °C |
| Энтальпия | |
| • образования | −391,2 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | гидролизуется |
| Структура | |
| Дипольный момент | 6,0E−30 Кл·м[2] |
| Классификация | |
| Рег. номер CAS | [7791-25-5] |
| PubChem | 24648 |
| Рег. номер EINECS | 232-245-6 |
| SMILES | |
| InChI | |
| ChEBI | 29291 |
| ChemSpider | 23050 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Сульфурилхлорид (хлористый сульфурил) SO2Cl2 — хлорангидрид серной кислоты.
Свойства
Бесцветная, резко пахнущая жидкость, хорошо растворимая в хлороформе и уксусной кислоте, в избытке воды растворяется с частично протекающим гидролизом. Дымит на воздухе, гидролизуется по реакции:
Гидролиз идёт слабо в холодной воде, в горячей воде протекает быстро.
При хранении желтеет, поскольку распадается на SO2 и зеленовато-жёлтый хлор.
Получение
Получают взаимодействием SO2 с Cl2 в присутствии катализаторов (активированный уголь, камфора).
Применение
Сульфурилхлорид используется как растворитель для ряда органических и неорганических соединений.
Применяют в синтезе органических веществ (с ним активно проходит хлорирование[3]), вступает в реакции сульфохлорирования тиофенов, через образование комплекса с ДМФА[4].
Примечания
- ↑ CRC Handbook of Chemistry and Physics (англ.) / David R. Lide, Jr. — 78 — United States of America: CRC Press, 1997. — P. 6—135. — ISBN 978-0-8493-0478-1
- ↑ 1 2 David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ Реми, Генрих. Курс неорганической химии. Том 1. /Пер. с нем. XI изд. под ред. акад. А. В. Новосёловой. Москва: Мир, 1972. —с. 700—701.
- ↑ Tyo Sone. The use of N,N-dimethylformamide-sulfonyl chloride complex for the preparation of thiophenesulfonyl chlorides (англ.) // Bull. Chem. Soc. Jpn.. — 1985. — Т. 58. — С. 1063-1064.
2. Tyo Sone et all. The use of N,N-dimethylformamide-sulfonyl chloride complex for the preparation of thiophenesulfonyl chlorides - Bull. Chem. Soc. Jpn. 1985, 58, P. 1063-1064
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.




