Mad2
Необходимо проверить качество перевода, исправить содержательные и стилистические ошибки. |

Mad2 (митотический дефицитный блокатор 2) является важным белком контрольной точки веретена деления. Система контрольной точки веретена деления является системой регулирования, сдерживающей прогрессирование перехода от метафазы к анафазе. Ген Mad2 был впервые выявлен в дрожжах S. cerevisiae в скриннинге для генов, мутированных для придания им чувствительности к ядам микротрубочек[1]. Человеческие ортологи Mad2 (MAD2L1 и MAD2L2 были впервые выделены в поисках человеческих кДНК, которые спасают микротрубочки ядочувствительного штамма дрожжей, в котором отсутствовал белок, связывающий кинетохор[2]. Было показано, что белок был представлен в одиноких кинетохорах и исследование ингибирования антител показало, что он имеет важное значение для выполнения блока перехода от метафазы к анафазе в ответ на отравление микротрубочек нокодазолом[2]. После выделения ортолога Xenopus Laevis , подобного человеческим последовательностям, появилась возможность охарактеризовать митотическую контрольную точку в экстрактах яиц[3].
Переход от метафазы к анафазе
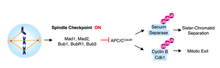
Прогрессирование от метафазы к анафазе отмечается разделением сестринских хроматид. Механизм слежения клеточного цикла, который предотвращает разделение сестринских хроматид и переход в анафазу называется контрольной точкой веретена деления. В качестве меры против ошибок хромосом, контрольная точка сборки веретена деления (SАС) задерживает анафазу, пока все пары сестринских хроматид не будут биполярно приложены.
После того, как микротрубочки присоединены к кинетохорам, хромосомы выравниваются на метафазной пластине и достигается биориентации, механизм остановки SAC удаляется. Вход в анафазу опосредуется активацией APCCdc20. APCCdc20 является убиквитинпротеинлигазой, которая метит белок, секурин для уничтожения. Уничтожение секурина освобождает и активирует сепаразу. Сепараза, связанная с секурином остается блокированной; однако, когда ингибирование освобождено, активированная сепараза расщепляет комплекс кохезина, который связывает сестринские хроматиды вместе[5].
Без Cdc20, комплекс стимуляции анафазы (APC) не может активироваться и анафаза не наступает. Mad2, как было показано, ингибируют активность APC путём прямого физического взаимодействия[6] в тройном комплексе с Cdc20[7]. Кинетохоры, к которым остаются привязаны микротрубочки, катализируют секвестр Cdc20 с помощью Mad2. В самом деле, когда в метафазе клетки млекопитающих обрабатывают агент, деполимеризующий веретено деления, нокодазол, белки MAD2 становятся локализованными на кинетохорах всеми парами сестринских хроматид[5].
Конформеры Mad2
![[4]](/upwiki/wikipedia/commons/0/0b/Mad2conformers.png)
Mad2 способен образовывать мультимеры и принимает по меньшей мере две структурных конформации. Открытый Mad2 отличается от закрытого Mad2 в позиционировании 50 остатков С-концевого[англ.] сегмента. Этот «ремень безопасности» плотно прижимался к правой стороне белка в открытой конформации. После ослабления, ремень безопасности может быть повторно установлен партнером связывания. В закрытой конформации, ремень безопасности обтекает связанный лиганд и взаимодействует с другой областью Mad2. Связывающими партнерами Mad2 могут быть либо Cdc20 либо Mad1. Mad1 и Cdc20 связывают Mad2 идентичным образом. Mad2 использует один и тот же сайт для связывания либо Mad1 либо Cdc20 и, таким образом, может связывать только один из двух белков одновременно[5].
Активация Mad2 в контрольной точке сборки веретена деления
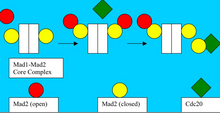
Так как одинокие кинетохоры установливют и поддерживают SAC, Mad2 рекрутируется для предотвращения от разделения этих неупорядоченных сестринских хроматид. Когда процесс торможения контрольных точек активирован, Mad2 связывает Mad1, формируя замкнутый Mad2-Mad1 комплекс. Учитывая, что Mad1:Mad2 — устойчивый комплекс и CDC20 и MAD1 связывает Mad2 в том же самом сайте связывания, то крайне маловероятно, что закрытый Mad2 освободит Mad1 для связывания с Cdc20.
Модель, объясняющая конформацию Mad2, способную связываться с Cdc20, опирается на первичность формирование основного комплекса Mad1-Mad2. В этой модели, внешний открытый Mad2 рекрутируется в матрицу Mad1: Mad2. Это Mad2: Mad2 взаимодействие необходимо, чтобы разрешить конформационные изменения, которые позволяют периферии, связанной с открытым Mad2, взаимодействовать с Cdc20. Cdc20: Mad2 тогда распадается и Mad1:Mad2 может снова связывать свободный цитозольный Mad2[8].
Предполагается, что когда-то образованные Cdc20:Mad2 комплексы могут усиливать сигнал ожидания анафазы, стимулируя дальнейшее преобразование цитозольного открытого Mad2 и свободного Cdc20 в Cdc20: закрытый Mad2 комплекс. Эта диффузии распространения сигнала от кинетохорных комплексов может объяснить, как вакансия только одного крошечного сайта кинетохора может полностью закрыть переход от метафазы к анафазе[9].
Будущие цели исследований
Многое ещё предстоит объяснить о сигнализации контрольной точки веретена деления и вклад других сборочных белков контрольной точки веретена деления, таких как Bub1, BubR1 и Bub3. BubR1 и Bub3 также могут образовывать комплексы с Cdc20, но это ещё предстоит увидеть, если этим белкам облегчить связывания Cdc20 с открытым Mad2[9].
Также весьма неясно, как p31comet противодействует контрольной точке и способствует диссоциации Mad2-Cdc20. Де Антони и др. предполагают, что в сочетании с «матрицей Mad2», p31comet конкурирует с открытым Mad2 за связывание с закрытым Mad2: Mad1. Тестирование ведется для того, чтобы осветить, как p31comet может заставить замолчать контрольные точки веретена деления[10].
Примечания
- ↑ Li R, Murray AW (1991). "Feedback control of mitosis in budding yeast". Cell. 66 (3): 519—31. doi:10.1016/0092-8674(81)90015-5. PMID 1651172.
- ↑ 1 2 Li Y, Benezra R (1996). "Identification of a human mitotic checkpoint gene: hsMAD2". Science. 274 (5285): 246—8. doi:10.1126/science.274.5285.246. PMID 8824189.
- ↑ Chen RH, Waters JC, Salmon ED, Murray AW (October 1996). "Association of spindle assembly checkpoint component XMAD2 with unattached kinetochores". Science. 274 (5285): 242—6. doi:10.1126/science.274.5285.242. PMID 8824188.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ 1 2 Yu H (April 2006). "Structural activation of Mad2 in the mitotic spindle checkpoint: the two-state Mad2 model versus the Mad2 template model". J. Cell Biol. 173 (2): 153—7. doi:10.1083/jcb.200601172. PMC 2063805. PMID 16636141.
- ↑ 1 2 3 Morgan DL. The cell cycle: principles of control. — London : Published by New Science Press in association with Oxford University Press, 2007. — ISBN 0-87893-508-8.
- ↑ Li Y, Gorbea C, Mahaffey D, Rechsteiner M, Benezra R (November 1997). "MAD2 associates with the cyclosome/anaphase-promoting complex and inhibits its activity". Proc. Natl. Acad. Sci. U.S.A. 94 (23): 12431—6. doi:10.1073/pnas.94.23.12431. PMC 24983. PMID 9356466.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Wassmann K, Benezra R (September 1998). "Mad2 transiently associates with an APC/p55Cdc complex during mitosis". Proc. Natl. Acad. Sci. U.S.A. 95 (19): 11193—8. doi:10.1073/pnas.95.19.11193. PMC 21618. PMID 9736712.
- ↑ Hardwick KG (February 2005). "Checkpoint signalling: Mad2 conformers and signal propagation". Curr. Biol. 15 (4): R122—4. doi:10.1016/j.cub.2005.02.008. PMID 15723780.
- ↑ 1 2 Nasmyth K (March 2005). "How do so few control so many?". Cell. 120 (6): 739—46. doi:10.1016/j.cell.2005.03.006. PMID 15797376.
- ↑ De Antoni A, Pearson CG, Cimini D, Canman JC, Sala V, Nezi L, Mapelli M, Sironi L, Faretta M, Salmon ED, Musacchio A (February 2005). "The Mad1/Mad2 complex as a template for Mad2 activation in the spindle assembly checkpoint". Curr. Biol. 15 (3): 214—25. doi:10.1016/j.cub.2005.01.038. PMID 15694304.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка)