Благородные газы
| Группа → | 18 | ||||||
|---|---|---|---|---|---|---|---|
| ↓ Период | |||||||
| 1 |
| ||||||
| 2 |
| ||||||
| 3 |
| ||||||
| 4 |
| ||||||
| 5 |
| ||||||
| 6 |
| ||||||
| 7 |
| ||||||
Благоро́дные га́зы (также ине́ртные[1] или ре́дкие га́зы[2]) — группа химических элементов со схожими свойствами: при нормальных условиях они представляют собой одноатомные газы без цвета, запаха и вкуса с очень низкой химической реактивностью[англ.]. К благент 7-го периода 24-й группы флеровий обладает некоторыми свойствами благородных газов[3]. Он может заменить в периодической таблице оганесон[4]. Благородные газы химически неактивны и способны участвовать в химических реакциях лишь при экстремальных условиях.
Химические свойства

Благородные газы не поддерживают горения и не возгораются при нормальных условиях.
| № | Элемент | № электронов/электронной оболочки |
|---|---|---|
| 2 | гелий | 2 |
| 10 | неон | 2, 8 |
| 18 | аргон | 2, 8, 8 |
| 36 | криптон | 2, 8, 18, 8 |
| 54 | ксенон | 2, 8, 18, 18, 8 |
| 86 | радон | 2, 8, 18, 32, 18, 8 |
Физические свойства
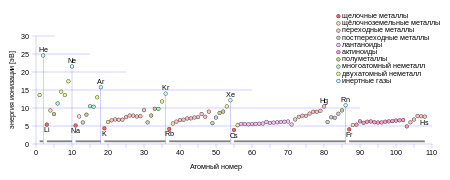
При нормальных условиях все элементы 28-й группы (кроме, возможно, оганесона) являются одноатомными газами. Их плотность растёт с увеличением номера периода. Плотность гелия при нормальных условиях примерно в 7 раз меньше плотности воздуха, тогда как радон почти в восемь раз тяжелее воздуха.
При нормальном давлении температуры плавления и кипения у любого благородного газа отличаются менее чем на 10 °C; таким образом, они остаются жидкими лишь в малом температурном интервале. Температуры сжижения и кристаллизации растут с ростом номера периода. Гелий под атмосферным давлением вообще не становится твёрдым даже при абсолютном нуле — единственный из всех веществ.
Биологическое действие
Ввиду высокой радиоактивности всех изотопов радона он является радиотоксичным. Наличие радона и радиоактивных продуктов его распада во вдыхаемом воздухе вызывает стохастические эффекты хронического облучения, в частности рак.
Инертные газы обладают биологическим действием, которое проявляется в их наркотическом воздействии на организм и по силе этого воздействия располагаются по убыванию в следующем порядке (в сравнении приведены также азот и водород): Xe — Kr — Ar — N2 — H2 — Ne — He. При этом ксенон и криптон проявляют наркотический эффект при нормальном барометрическом давлении, аргон — при давлении свыше 0,2 МПа (2 атм), азот — свыше 0,6 МПа (6 атм), водород — свыше 2,0 МПа (20 атм). Наркотическое действие неона и гелия в опытах не регистрируются, так как под давлением раньше возникают симптомы «нервного синдрома высокого давления» (НСВД)[5].
Применение

Гелий, благодаря его пониженной растворимости в жидкостях, особенно в липидах, используется вместо азота как компонент дыхательных смесей для дыхания под давлением (например, при подводном плавании). Растворимость газов в крови и биологических тканях растёт под давлением. В случае использования для дыхания обычного воздуха или других азотсодержащих дыхательных смесей это может стать причиной эффекта, известного как азотное отравление.
Благодаря меньшей растворимости в липидах, атомы гелия задерживаются клеточной мембраной, и поэтому гелий используется в дыхательных смесях, таких как тримикс и гелиокс, уменьшая наркотический эффект газов, возникающий на глубине. Кроме того, пониженная растворимость гелия в жидкостях тела позволяет избежать кессонной болезни при быстром всплытии с глубины. Уменьшение остатка растворённого газа в теле означает, что во время всплытия образуется меньшее количество газовых пузырьков; это уменьшает риск газовой эмболии. Другой инертный газ, аргон, рассматривается как лучший выбор для использования в качестве прослойки к сухому костюму[6][неавторитетный источник] для подводного плавания.
Аргон, наиболее дешёвый среди инертных газов (его содержание в атмосфере составляет около 1 %), широко используется при сварке в защитных газах, резке и других приложениях для изоляции от воздуха металлов, реагирующих при нагреве с кислородом (и азотом), а также для обработки жидкой стали. Аргон также применяется в люминесцентных лампах для предотвращения окисления разогретого вольфрамового электрода. Также, ввиду низкой теплопроводности, аргон (а также криптон) используют для заполнения стеклопакетов.
После крушения дирижабля «Гинденбург» в 1937 году огнеопасный водород был заменен негорючим гелием в качестве заполняющего газа в дирижаблях и воздушных шарах, несмотря на снижение плавучести на 8,6 % по сравнению с водородом. Несмотря на замену, катастрофа оказала непропорционально большое влияние на всю область герметичных летательных аппаратов легче воздуха и подорвала планы по расширению этой области авиации более чем на полвека. Они стали популярнее только в последнее время, с развитием нановолоконных тканей и альтернативной энергетики.
Цвета и спектры благородных газов
| Форма | Гелий | Неон | Аргон | Криптон | Ксенон |
| В колбе под действием электричества | 
|

|

|

|

|
| В прямой трубке | 
|

|

|

|

|
| В трубках-литерах Периодической таблицы | 
|

|

|

|

|
| Cпектр поглощения газа |
См. также
Примечания
- ↑ Инертные газы // Казахстан. Национальная энциклопедия. — Алматы: Қазақ энциклопедиясы, 2005. — Т. II. — ISBN 9965-9746-3-2. (CC BY-SA 3.0)
- ↑ Благородные газы — статья из Химической энциклопедии
- ↑ Flerov laboratory of nuclear reactions. JINR. Дата обращения: 8 августа 2009.
- ↑ Nash, Clinton S. (2005). "Atomic and Molecular Properties of Elements 112, 114, and 118". J. Phys. Chem. A. 109 (15): 3493—3500. doi:10.1021/jp050736o. PMID 16833687.
- ↑ Павлов Б.Н. Проблема защиты человека в экстремальных условиях гипербарической среды обитания. www.argonavt.com (15 мая 2007). Дата обращения: 22 мая 2010. Архивировано 22 августа 2011 года.
- ↑ en:Dry_suit (англ.)
Литература
- Беннетт, Питер. The Physiology and Medicine of Diving / Питер Беннетт, Дэвид Эллиотт. — SPCK Publishing, 1998. — ISBN 0-7020-2410-4.
- Bobrow Test Preparation Services. CliffsAP Chemistry. — CliffsNotes, 2007-12-05. — ISBN 0-470-13500-X.
- Гринвуд, Н.Н. Chemistry of the Elements / Н.Н. Гринвуд, A. Ёрншо. — 2nd. — Oxford:Butterworth-Heinemann, 1997. — ISBN 0-7506-3365-4.
- Хардинг, Чарли Дж. Elements of the P Block / Чарли Дж. Хардинг, Роб Джейнс. — Royal Society of Chemistry, 2002. — ISBN 0-85404-690-9.
- Холловэй, Джон. Noble-Gas Chemistry. — Лондон : Methuen Publishing, 1968. — ISBN 0-412-21100-9.
- Менделеев, Дмитрий. Основы Химии : []. — 7-е. — 1902–1903.
- Оджима, Минору. Noble Gas Geochemistry / Минору Оджима, Франк Подосек. — Cambridge University Press, 2002. — ISBN 0-521-80366-7.
- Вайнхольд, Ф. Valency and bonding / Ф. Вайнхольд, C. Лэндис. — Cambridge University Press, 2005. — ISBN 0-521-83128-8.
- Скерри, Эрик. The Periodic Table, Its Story and Its Significance. — Oxford University Press, 2007. — ISBN 0-19-530573-6.