Мерлин (белок)
Мерлин (нейрофибромин 2 или шванномин) — белок цитоскелета. У людей это опухолевый супрессорный белок, вовлеченный в нейрофиброматоз 2-го типа. Его аминокислотная последовательность демонстрирует сходство с белками семейства ERM.
Название «мерлин» — это акроним слов «Моэзин-Эзрин-Радиксин-подобный белок» (Moesin-Ezrin-Radixin-Like Protein).
Гены
[править | править код]Человеческий мерлин закодирован в гене NF2 в 22-й хромосоме. У мышей ген мерлина расположен в 11-й хромосоме, а у крыс в 17-й. У дрозофилы этот ген находится в первой хромосоме и на 58 % соответствует человеческому аналогу. Другие «мерлиноподобные» гены известны у большого количества животных. Считается, что образование мерлина произошло у ранних многоклеточных. Мерлин — член семейства ERM, включающего также эзрин, моэзин и радиксин и входящего в надсемейство белков 4.1. Мерлин также известен как шванномин (название, образованное от шванномы — наиболее частой опухоли у пациентов с фенотипом NF2).
Структура
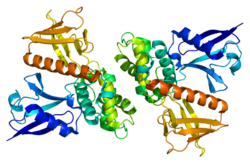
[править | править код]Мерлин у позвоночных — это белок весом 70 КДа. Известно 10 изоформ молекул человеческого мерлина (полная молекула состоит из 595 аминокислот). Две самые похожие изоформы, найденные также у мышей, названы тип 1 и тип 2. Они различаются отсутствием или наличием экзона 16 или 17, соответственно. Все известные варианты имеют сохраненный N-конец, состоящий из FERM-домена (домен, обнаруживаемый у большинства белков, образующих мембранный цитоскелет). За FERM-доменом следует альфа-спиральный домен и гидрофильный «хвост». Мерлин димеризуется, образуя гомодимеры, и гетеродимеризуется с другими белками ERM-семейства.
Функции
[править | править код]Мерлин — белок, являющийся «строительными лесами» мембранного цитоскелета, то есть соединяющий актиновые филаменты с клеточной мембраной или с мембранными гликопротеинами. Человеческий мерлин в основном обнаруживается в нервных тканях, но также и в некоторых зародышевых тканях, и в основном он сосредоточен в адгезивных контактах. Его свойства как опухолевого супрессора связаны с контактным торможением. Мерлин дрозофилы выделяется в эмбриональной кишке, слюнных железах и в имагинальных дисках и играет несколько другую роль, чем у позвоночных. Известно, что фосфорилирование серина в позиции 518 приводит к изменению функционального состояния мерлина. Предполагается, что сигнальный путь мерлина включает различные молекулы, в их числе eIF3c, CD44, протеинкиназа A и p21 активированные киназы, контролирующие рост клеток. Мутации гена NF2 вызывают у людей аутосомно-доминантное заболевание, называемое нейрофиброматозом 2-го типа. Оно характеризуется развитием опухолей нервной системы, чаще всего двусторонних вестибулярных шванном (также называемых акустическими невромами). NF2 принадлежит к группе генов — опухолевых супрессоров.
Взаимодействие
[править | править код]Известно, что мерлин взаимодействует с HGS, CUL4A, VIL2, SDCBP, VPRBP, RIT1, SPTBN1, MED28 и DDB1.
Литература
[править | править код]- Rouleau GA, Merel P, Lutchman M, Sanson M, Zucman J, Marineau C, Hoang-Xuan K, Demczuk S, Desmaze C, Plougastel B (1993). «Alteration in a new gene encoding a putative membrane-organizing protein causes neuro-fibromatosis type 2». Nature 363 (6429): 515-21. doi:10.1038/363515a0. PMID 8379998.
- Golovnina K, Blinov A, Akhmametyeva EM, Omelyanchuk LV, Chang LS (2005). «Evolution and origin of merlin, the product of the Neurofibromatosis type 2 (NF2) tumor-suppressor gene». BMC Evol. Biol. 5: 69. doi:10.1186/1471-2148-5-69. PMID 16324214.
- Haase VH, Trofatter JA, MacCollin M, Tarttelin E, Gusella JF, Ramesh V (1994). «The murine NF2 homologue encodes a highly conserved merlin protein with alternative forms». Hum. Mol. Genet. 3 (3): 407-11. doi:10.1093/hmg/3.3.407. PMID 8012352.
- Shimizu T, Seto A, Maita N, Hamada K, Tsukita S, Tsukita S, Hakoshima T (2002). «Structural basis for neurofibromatosis type 2. Crystal structure of the merlin FERM domain». J. Biol. Chem. 277 (12): 10332-6. doi:10.1074/jbc.M109979200. PMID 11756419.
- McClatchey AI, Giovannini M (2005). «Membrane organization and tumorigenesis--the NF2 tumor suppressor, Merlin». Genes Dev. 19 (19): 2265-77. doi:10.1101/gad.1335605. PMID 16204178.
- den Bakker MA, Vissers KJ, Molijn AC, Kros JM, Zwarthoff EC, van der Kwast TH (1999). «Expression of the neurofibromatosis type 2 gene in human tissues». J. Histochem. Cytochem. 47 (11): 1471-80. PMID 10544220. https://web.archive.org/web/20080518194148/http://www.jhc.org/cgi/content/abstract/47/11/1471.
- LaJeunesse DR, McCartney BM, Fehon RG (1998). «Structural analysis of Drosophila merlin reveals functional domains important for growth control and subcellular localization». J. Cell Biol. 141 (7): 1589-99. doi:10.1083/jcb.141.7.1589. PMID 9647651.
- Alfthan K, Heiska L, Grönholm M, Renkema GH, Carpén O (2004). «Cyclic AMP-dependent protein kinase phosphorylates merlin at serine 518 independently of p21-activated kinase and promotes merlin-ezrin heterodimerization». J. Biol. Chem. 279 (18): 18559-66. doi:10.1074/jbc.M313916200. PMID 14981079.
- Scoles DR, Yong WH, Qin Y, Wawrowsky K, Pulst SM (2006). «Schwannomin inhibits tumorigenesis through direct interaction with the eukaryotic initiation factor subunit c (eIF3c)». Hum. Mol. Genet. 15 (7): 1059-70. doi:10.1093/hmg/ddl021. PMID 16497727.
- Gutmann, D H; Haipek C A, Burke S P, Sun C X, Scoles D R, Pulst S M (Apr. 2001). «The NF2 interactor, hepatocyte growth factor-regulated tyrosine kinase substrate (HRS), associates with merlin in the „open“ conformation and suppresses cell growth and motility». Hum. Mol. Genet. (England) 10 (8): 825-34. ISSN 0964-6906. PMID 11285248.
- Scoles, D R; Huynh D P, Chen M S, Burke S P, Gutmann D H, Pulst S M (Jul. 2000). «The neurofibromatosis 2 tumor suppressor protein interacts with hepatocyte growth factor-regulated tyrosine kinase substrate». Hum. Mol. Genet. (ENGLAND) 9 (11): 1567-74. ISSN 0964-6906. PMID 10861283.
- Huang, J; Chen J (Jul. 2008). «VprBP targets Merlin to the Roc1-Cul4A-DDB1 E3 ligase complex for degradation». Oncogene (England) 27 (29): 4056-64. doi:10.1038/onc.2008.44. PMID 18332868.
- Grönholm, M; Sainio M, Zhao F, Heiska L, Vaheri A, Carpén O (Mar. 1999). «Homotypic and heterotypic interaction of the neurofibromatosis 2 tumor suppressor protein merlin and the ERM protein ezrin». J. Cell. Sci. (ENGLAND) 112 (Pt 6): 895—904. ISSN 0021-9533. PMID 10036239.
- Jannatipour, M; Dion P, Khan S, Jindal H, Fan X, Laganière J, Chishti A H, Rouleau G A (Aug. 2001). «Schwannomin isoform-1 interacts with syntenin via PDZ domains». J. Biol. Chem. (United States) 276 (35): 33093-100. doi:10.1074/jbc.M105792200. ISSN 0021-9258. PMID 11432873.
- Neill, G W; Crompton M R (Sep. 2001). «Binding of the merlin-I product of the neurofibromatosis type 2 tumour suppressor gene to a novel site in beta-fodrin is regulated by association between merlin domains». Biochem. J. (England) 358 (Pt 3): 727-35. ISSN 0264-6021. PMID 11535133.
- Wiederhold, Thorsten; Lee Ming-Fen, James Marianne, Neujahr Ralph, Smith Nicole, Murthy Anita, Hartwig John, Gusella James F, Ramesh Vijaya (Nov. 2004). «Magicin, a novel cytoskeletal protein associates with the NF2 tumor suppressor merlin and Grb2». Oncogene (England) 23 (54): 8815-25. doi:10.1038/sj.onc.1208110. ISSN 0950-9232. PMID 15467741.
Для улучшения этой статьи желательно:
|