Дитиосульфатоаурат(I) натрия
| Дитиосульфатоаурат(I) натрия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
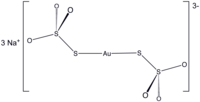
Дитиосульфатоаурат(I) натрия |
| Хим. формула | Na3Au(S2O3)2 |
| Рац. формула | Na3AuS4O6 |
| Физические свойства | |
| Состояние | красно-коричневый порошок (гидрат) |
| Молярная масса | 490,16 г/моль |
| Классификация | |
| Рег. номер CAS | 18497-75-1 |
| PubChem | 170028 |
| SMILES | |
| InChI | |
| ChemSpider | 148687 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Дитиосульфатоаурат(I) натрия — неорганическое соединение, соль металлов натрия и золота и тиосерной кислоты, формулой Na3Au(S2O3)2. При нормальных условиях представляет собой красно-коричневое твёрдое вещество. Известен гидрат состава Na3Au(S2O3)2·2H2O.
Получение
[править | править код]- Взаимодействие димера хлорида золота(III) c солями Ме[AuCl2] и Ме[AuCl4], где Ме=щелочной металл, c тиосульфатом натрия:
Физические свойства
[править | править код]Дитиосульфатоаурат(I) натрия образует красно-коричневое твёрдое вещество. При нагревании сначала дегидратируется (теряет воду), а потом разлагается.
Химические свойства
[править | править код]- Реакция дегидратации:
- При сильном нагревании на воздухе полностью разлагается:
- Взаимодействует с дигидратом хлорида бария в присутствии спирта или ацетона:
- Галогеноводороды, серная и щавелевая кислоты также реагируют с дитиосульфатоауратом(I) натрия. В ходе реакции образуется сульфид золота(III) Au2S3. Известна калийная соль состава K3Au(S2O3)2
Литература
[править | править код]- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.

![{\displaystyle {\mathsf {Me[AuCl_{4}]+4Na_{2}S_{2}O_{3}\ {\xrightarrow {}}\ Na_{3}Au(S_{2}O_{3})_{2}+Na_{2}S_{4}O_{6}+3NaCl+MeCl}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/6fb749a83219a960ebe9bf94de7b8fe0579db123)
![{\displaystyle {\mathsf {Cs[AuCl_{4}]+4Na_{2}S_{2}O_{3}\ {\xrightarrow {}}\ Na_{3}Au(S_{2}O_{3})_{2}+Na_{2}S_{4}O_{6}+3NaCl+CsCl}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/d2c479df8a176aa647b9922d144cf571d12e7acd)
![{\displaystyle {\mathsf {Me[AuCl_{2}]+2Na_{2}S_{2}O_{3}\ {\xrightarrow {}}\ Na_{3}Au(S_{2}O_{3})_{2}+2MeCl}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/0de64ff0386cd3038ddb28085d08a7639c716b92)
![{\displaystyle {\mathsf {Na[AuCl_{2}]+2Na_{2}S_{2}O_{3}\ {\xrightarrow {}}\ Na_{3}Au(S_{2}O_{3})_{2}+2NaCl}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/816365aeea7d1f7d766f8f778fa1f3c01c669966)


![{\displaystyle {\mathsf {2Na_{3}Au(S_{2}O_{3})_{2}+3BaCl_{2}\cdot 2H_{2}O\ {\xrightarrow {C_{2}H_{5}OH}}\ Ba_{3}[Au(S_{2}O_{3})_{2}]_{2}\cdot 6H_{2}O+6NaCl}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/6b1d58d961b11e7c3a3c7e9bb68b4f417c27e77f)