四碘化碲:修订间差异
外观
删除的内容 添加的内容
Cat-a-lot:分类间复制:从Category:卤化碲到Category:四价碲化合物 |
|||
| 第47行: | 第47行: | ||
[[category:碘化物]] |
[[category:碘化物]] |
||
[[Category:卤化碲]] |
[[Category:卤化碲]] |
||
[[Category:四价碲化合物]] |
|||
2022年10月24日 (一) 12:52的最新版本
| 四碘化碲 | |
|---|---|
| |
| 别名 | 碘化碲(IV) |
| 识别 | |
| CAS号 | 7790-48-9 |
| PubChem | 82255 |
| SMILES |
|
| InChI |
|
| EINECS | 232-210-5 |
| 性质 | |
| 化学式 | TeI4 |
| 摩尔质量 | 635.218 g/mol g·mol⁻¹ |
| 外观 | 黑色晶体 |
| 密度 | 5.05 g/cm³(固) |
| 熔点 | 280 °C(553 K) |
| 结构 | |
| 晶体结构 | orthorhombic |
| 危险性 | |
| 欧盟分类 | 未列出 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
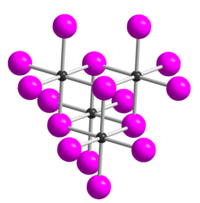
四碘化碲(化学式:TeI4)是一种无机化合物,具有和TeCl4和TeBr4的四聚体固体形式不同的四聚体结构。[1]在TeI4中,Te原子的配位结构为八面体,八面体的顶点被共用。[1]
TeI4可以由单质制备,或者通过碲和碘甲烷的反应得到。[1]在气态TeI4中会发生解离:[2]
- TeI4 → TeI2 + I2
TeI4熔化时是一个导体,这是由于解离出的TeI3+和I−。有配位能力的溶剂,如乙腈,在溶解该物质时,溶液具有导电能力:[2]
- TeI4 + 2 CH3CN → (CH3CN)2TeI3+ + I−
参考文献
[编辑]- ^ 1.0 1.1 1.2 Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ 2.0 2.1 Inorganic Chemistry,Egon Wiberg, Arnold Frederick Holleman Elsevier 2001 ISBN 0-12-352651-5
