TEV蛋白酶
| {{{Name}}} | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
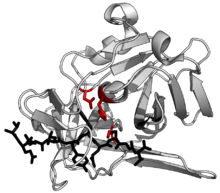
| TEV蛋白酶(白色)与肽底物(黑色)与活性位点三联体残基(红色)复合。 (PDB 1lvb) | |||||||
| |||||||
| 识别码 | |||||||
| EC編號 | 3.4.22.44 | ||||||
| CAS号 | 139946-51-3 | ||||||
| 数据库 | |||||||
| IntEnz | IntEnz浏览 | ||||||
| BRENDA | BRENDA入口 | ||||||
| ExPASy | NiceZyme浏览 | ||||||
| KEGG | KEGG入口 | ||||||
| MetaCyc | 代谢路径 | ||||||
| PRIAM | 概述 | ||||||
| PDB | RCSB PDB PDBj PDBe PDBsum | ||||||
| |||||||
烟草蚀刻病毒蛋白酶(EC 3.4.22.44),简称TEV蛋白酶,是来自烟草蚀刻病毒的高度序列特异性半胱氨酸蛋白酶。[1]它是胰凝乳蛋白酶样蛋白酶PA家族的成员。[2]由于其高序列特异性,它经常用于体外和体内融合蛋白的受控切割。[3]
来源
烟草蚀刻病毒将其整个基因组编码为单一的大量多聚蛋白(350kDa)。这被三种蛋白酶切割成功能单元:P1蛋白酶(1个切割位点)、辅助组分蛋白酶(1个切割位点)和TEV蛋白酶(7个切割位点)。[1]天然TEV蛋白酶还包含一个内部自切割位点。该位点被缓慢切割以使酶失活(其生理原因尚不清楚)。
Structure and function

TEV蛋白酶的结构已通过X射线晶体学解析。[4]它由两个β桶和一个灵活的C末端尾部组成,并显示出与蛋白酶的糜蛋白酶超家族(PA 族,MEROPS 分类的 C4 家族)的结构同源性。[2]尽管与细胞丝氨酸蛋白酶(如胰蛋白酶、弹性蛋白酶、凝血酶等)同源,但TEV蛋白酶使用半胱氨酸作为其催化亲核试剂[5](与许多其他病毒蛋白酶一样)。
用Asp-His-Cys三联体进行共价催化,在两个桶之间分开(β1上的Asp与β2上的His和Cys)。[6]底物保持为β折叠,与桶之间的裂缝形成反平行相互作用,并与C端形成平行相互作用。[7]因此,酶在底物周围形成结合隧道,侧链相互作用控制特异性。[4]
特异性

优选的天然切割序列首先通过检查天然多蛋白底物中的切割位点的重复序列来鉴定。这些天然切割位点的共识是ENLYFQ\S,其中“\”表示切割的肽键。[8]底物的残留物在切割位点之前标记为P6到P1,在切割位点之后标记为P1'。早期的工作还测量了一系列相似底物的切割,以表征蛋白酶对天然序列的特异性。[9][10]
随后的研究使用从随机序列池中切割底物的测序来确定偏好模式。[11][12]尽管ENLYFQ\S是最佳序列,但蛋白酶在一系列底物上或多或少都有活性(即显示出一些底物混杂)。最高切割是最接近共有EXLYΦQ\φ的序列,其中X是任何残基,Φ是任何大或中等疏水基,φ是任何小的疏水或极性残基。虽然这个序列是最优的,但如果序列的其余部分是最优的,那么在某些位置具有不利残基的序列仍然可以被切割。[10][12]
酶和底物之间的大接触面积赋予了特异性。由于只有一个或两个口袋结合底物侧链的浅结合裂口,蛋白酶(如胰蛋白酶)对断裂键前后的一个残基具有特异性。相反,病毒蛋白酶(如TEV蛋白酶)有一个长的C端,它完全覆盖底物以形成结合隧道。该隧道包含一组紧密的结合口袋,这样底物肽的每个侧链(P6到P1')都结合在一个互补位点(S6到S1')。[4]
特别是,肽侧链P6-Glu接触三个氢键网络;P5-Asn指向溶剂,没有特定的相互作用(因此在这个位置没有底物共识);P4-Leu被埋在疏水袋中; P3-Tyr位于末端带有短氢键的疏水袋中;P2-Phe也被疏水物包围,包括三联体组氨酸的表面;P1-Gln形成四个氢键;并且P1'-Ser仅部分封闭在浅疏水凹槽中。[4]
作为生化工具
这种蛋白质的主要用途之一是从纯化的重组融合蛋白中去除亲和标签。使用TEV蛋白酶作为生化工具的原因是其高序列特异性。当偏好序列插入柔性环时,这种特异性允许蛋白质的受控切割。它还使其在体内相对无毒,因为识别的序列几乎不存在于蛋白质中。[13]
尽管合理设计在改变蛋白酶特异性方面的成功有限,但定向进化已被用于在切割位点之前[14]或之后[15][16]改变首选残基。
然而,TEV蛋白酶作为生化工具确实有局限性。它很容易通过自切割(自溶)失活,尽管这可以通过内部切割位点的单个S219V突变来消除。[17]单独表达的蛋白酶的溶解性也很差,但是已经进行了几次尝试以通过定向进化和计算设计来提高其溶解度。还表明,可以通过与麦芽糖结合蛋白融合来改善表达,该蛋白充当溶解度增强伙伴。
据报道,TEV蛋白酶在4°C时活性降低10倍。[18]TEV蛋白酶在34°C以上的温度下会失去活性。[19]
这种酶的分子量在25和27 kDa之间变化,具体取决于所使用的特定构建体。
参考文献
- ^ 1.0 1.1 UniProt: TEV polyprotein: P04517.
- ^ 2.0 2.1 Rawlings ND, Barrett AJ, Bateman A. MEROPS: the database of proteolytic enzymes, their substrates and inhibitors. Nucleic Acids Res. January 2012, 40 (Database issue): D343–50. PMC 3245014
 . PMID 22086950. doi:10.1093/nar/gkr987.
. PMID 22086950. doi:10.1093/nar/gkr987.
- ^ Kapust RB, Waugh DS. Controlled intracellular processing of fusion proteins by TEV protease. Protein Expr. Purif. July 2000, 19 (2): 312–8. PMID 10873547. doi:10.1006/prep.2000.1251.
- ^ 4.0 4.1 4.2 4.3 Phan J, Zdanov A, Evdokimov AG, Tropea JE, Peters HK, Kapust RB, Li M, Wlodawer A, Waugh DS. Structural basis for the substrate specificity of tobacco etch virus protease. J. Biol. Chem. December 2002, 277 (52): 50564–72. PMID 12377789. doi:10.1074/jbc.M207224200
 .
.
- ^ Bazan JF, Fletterick RJ. Viral cysteine proteases are homologous to the trypsin-like family of serine proteases: structural and functional implications. Proc. Natl. Acad. Sci. U.S.A. November 1988, 85 (21): 7872–6. Bibcode:1988PNAS...85.7872B. PMC 282299
 . PMID 3186696. doi:10.1073/pnas.85.21.7872
. PMID 3186696. doi:10.1073/pnas.85.21.7872  .
.
- ^ Dougherty WG, Parks TD, Cary SM, Bazan JF, Fletterick RJ. Characterization of the catalytic residues of the tobacco etch virus 49-kDa proteinase. Virology. September 1989, 172 (1): 302–10. PMID 2475971. doi:10.1016/0042-6822(89)90132-3.
- ^ Tyndall JD, Nall T, Fairlie DP. Proteases universally recognize beta strands in their active sites. Chem. Rev. March 2005, 105 (3): 973–99. PMID 15755082. doi:10.1021/cr040669e.
- ^ Carrington JC, Dougherty WG. A viral cleavage site cassette: identification of amino acid sequences required for tobacco etch virus polyprotein processing. Proc. Natl. Acad. Sci. U.S.A. May 1988, 85 (10): 3391–5. Bibcode:1988PNAS...85.3391C. PMC 280215
 . PMID 3285343. doi:10.1073/pnas.85.10.3391
. PMID 3285343. doi:10.1073/pnas.85.10.3391  .
.
- ^ Dougherty WG, Cary SM, Parks TD. Molecular genetic analysis of a plant virus polyprotein cleavage site: a model. Virology. August 1989, 171 (2): 356–64. PMID 2669323. doi:10.1016/0042-6822(89)90603-X.
- ^ 10.0 10.1 Kapust, Rachel B.; Tözsér, József; Copeland, Terry D.; Waugh, David S. The P1' specificity of tobacco etch virus protease. Biochemical and Biophysical Research Communications. 2002-06-28, 294 (5): 949–955. CiteSeerX 10.1.1.375.4271
 . ISSN 0006-291X. PMID 12074568. doi:10.1016/S0006-291X(02)00574-0.
. ISSN 0006-291X. PMID 12074568. doi:10.1016/S0006-291X(02)00574-0.
- ^ Boulware KT, Jabaiah A, Daugherty PS. Evolutionary optimization of peptide substrates for proteases that exhibit rapid hydrolysis kinetics. Biotechnol. Bioeng. June 2010, 106 (3): 339–46. PMID 20148412. S2CID 205499859. doi:10.1002/bit.22693.
- ^ 12.0 12.1 Kostallas G, Löfdahl PÅ, Samuelson P. Substrate profiling of tobacco etch virus protease using a novel fluorescence-assisted whole-cell assay. PLOS ONE. 2011, 6 (1): e16136. Bibcode:2011PLoSO...616136K. PMC 3022733
 . PMID 21267463. doi:10.1371/journal.pone.0016136
. PMID 21267463. doi:10.1371/journal.pone.0016136  .
.
- ^ Parks TD, Leuther KK, Howard ED, Johnston SA, Dougherty WG. Release of proteins and peptides from fusion proteins using a recombinant plant virus proteinase. Anal. Biochem. February 1994, 216 (2): 413–7. PMID 8179197. doi:10.1006/abio.1994.1060.
- ^ Yi L, Gebhard MC, Li Q, Taft JM, Georgiou G, Iverson BL. Engineering of TEV protease variants by yeast ER sequestration screening (YESS) of combinatorial libraries. Proc. Natl. Acad. Sci. U.S.A. April 2013, 110 (18): 7229–34. Bibcode:2013PNAS..110.7229Y. PMC 3645551
 . PMID 23589865. doi:10.1073/pnas.1215994110
. PMID 23589865. doi:10.1073/pnas.1215994110  .
.
- ^ Renicke C, Spadaccini R, Taxis C. A tobacco etch virus protease with increased substrate tolerance at the P1' position. PLOS ONE. 2013, 8 (6): e67915. Bibcode:2013PLoSO...867915R. PMC 3691164
 . PMID 23826349. doi:10.1371/journal.pone.0067915
. PMID 23826349. doi:10.1371/journal.pone.0067915  .
.
- ^ Verhoeven KD, Altstadt OC, Savinov SN. Intracellular detection and evolution of site-specific proteases using a genetic selection system. Appl. Biochem. Biotechnol. March 2012, 166 (5): 1340–54. PMID 22270548. S2CID 36583382. doi:10.1007/s12010-011-9522-6.
- ^ Kapust RB, Tözsér J, Fox JD, Anderson DE, Cherry S, Copeland TD, Waugh DS. Tobacco etch virus protease: mechanism of autolysis and rational design of stable mutants with wild-type catalytic proficiency. Protein Eng. December 2001, 14 (12): 993–1000. PMID 11809930. doi:10.1093/protein/14.12.993
 .
.
- ^ Raran-Kurussi S, Tözsér J, Cherry S, Tropea JE, Waugh DS. Differential temperature dependence of tobacco etch virus and rhinovirus 3C proteases. Analytical Biochemistry. 15 May 2013, 436 (2): 142–144. PMC 4196241
 . PMID 23395976. doi:10.1016/j.ab.2013.01.031.
. PMID 23395976. doi:10.1016/j.ab.2013.01.031.
- ^ Nallamsetty S, Kapust RB, Tözsér J, Cherry S, Tropea JE, Copeland TD, Waugh DS. Efficient site-specific processing of fusion proteins by tobacco vein mottling virus protease in vivo and in vitro. Protein Expr. Purif. November 2004, 38 (1): 108–115. PMID 15477088. doi:10.1016/j.pep.2004.08.016.
