碳正离子

碳正离子,又称作碳阳离子,是一个带有正电的碳原子,其中最简单的形式为甲基碳正离子CH3+,跟乙基碳阳离子C2H5+。有些碳正离子基会带有两个或更多的正电,正电可能会在同一个或是不同的碳上,如乙烯双阳离子基C2H42+。
直到1970年代早期,碳阳离子都被视为碳离子。在近代的化学中,带正电的碳原子就视作一个碳阳离子。根据碳原子的价数可以分成两大类:三价的碳离子(质子化的碳烯),或五到六价的碳离子(质子化的烷类),而命名法为乔治·安德鲁·欧拉(George A. Olah)所发表,碳正离子能借由分散或离域正电荷来达到稳定。
历史
[编辑]碳阳离子的历史可追溯到1891年,G. Merling说他将溴加到环庚三烯(cycloheptatriene)上,然后加热结晶化产物取得水溶性物质C7H7Br,产生一个他无法解释的结构。然而, Doering 跟Knox预测是符合Hückel's 规则的溴化环庚三烯的芳香族来解释这个现象。
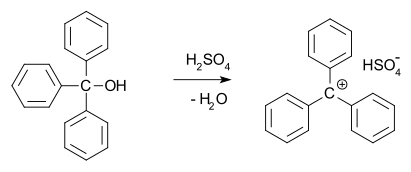
1902年,Norris 跟Kehrman分别发现无色的三苯基甲醇(triphenylmethanol)在浓硫酸中会变成深黄色。相似地,三苯基氯甲烷(Triphenylmethyl chloride)会跟铝、锡氯化物形成有机复合物。同年,阿道夫·冯·拜尔 (Adolf von Baeyer)认为其化合物形成一个类似盐类的构造。阿道夫猜测颜色跟盐类结构之间的关系就好比孔雀石绿(malachite green)。
碳阳离子在许多有机反应中扮演中间物的角色。其概念最早由Julius Stieglitz于1899年发表,Hans Meerweiny在他于1922做的研究Wagner-Meerwein rearrangement(重组)对其概念有更深的发展。且碳正离子在SN1,E1及重组反应(如Whitmore 1,2 转移)中被发现有参与反应进行。很长的一段时间,美国的化学家不愿意去接受一个新的化学概念,在文章中也不去提到碳正离子此概念。
第一个溶液中稳定的碳正离子的NMR图谱在1958由Doering等人所发表。其为七甲基苯离子(heptamethylbenzenium ion),由六甲基苯加上氯化铝、氯甲烷所制成。Story等人于1960制备出稳定的7-norbornadienyl 阳离子,借由norbornadienyl chloride与-80℃下溶于液态二氧化硫的四氟硼酸银(Silver tetrafluoroborate)反应产生。此NMR图谱显示出一个非传统的中间物(第一个发现的非传统稳定离子)
1962年,Olah借由核磁共振直接发现三级丁基碳阳离子跟溶于魔酸(magic acid)里的三级丁基氟一样稳定。Norbornyl阳离子的NMR图谱最先由 Schleyer等人发表,而Saunders等人则显示出屏障间质子抢夺的过程。
结构与特性
[编辑]碳阳离子中带有电荷的碳原子为六价态(sixtet),即外层电子只有六颗,而非符合八隅体的八颗。因此碳阳离子反应性高,以转变成有八颗电子的碳原子。其轨域为sp2混成轨域跟一个空的p轨域,而非sp3杂化,其中一个带有正电。分子模型为平面三角形。简单的例子如CH3+ 。而碳正离子常作为亲电体,像氢氧离子、卤素离子的结合对象。
碳正离子通常会进行重组反应,以反应常数超过109 /秒的速度从较不稳定的结构转变到较稳定的结构。此现象让许多化合物的合成过程变得复杂。例如:将3-戊醇跟HCl水溶液共热产生3-戊基碳正离子,会因重组反应产生3-戊基跟2-戊基的混和物。再跟氯离子进行反应得到的产物会有约1/3的3-氯戊烷跟2/3的2-氯戊烷。
碳正离子能借由与相邻的碳-碳双键共振来达到稳定。像是烯丙基阳离子(allyl cation)跟苄基阳离子(benzylic cation)就相较于其他碳正离子更加稳定。能够形成烯丙基或苯基碳正离子的分子其反应性就会较佳。经由与碳正离子空的p轨域与邻近的π键重叠,C+能够有额外的稳定性。轨域的重叠能够让复数的原子分享电荷,同时稳定碳阳离子。另一个稳定碳阳离子的因素是超共轭(Hyperconjugation),空的p轨域接受邻近碳上的电子对来将正电转给对方。
参考资料
[编辑]- Hansjörg Grützmacher, Christina M. Marchand (1997), "Heteroatom stabilized carbenium ions", Coordination Chemistry Reviews, volume 163, pages 287-344
- George A. Olah (1972), "Stable carbocations. CXVIII. General concept and structure of carbocations based on differentiation of trivalent (classical) carbenium ions from three-center bound penta- of tetracoordinated (nonclassical) carbonium ions. Role of carbocations in electrophilic reactions." Journal of the American Chemical Society, volume 94, issue 3, pages 808–820
- Organic chemistry 5th Ed. John McMurry ISBN 0-534-37617-7
- Organic Chemistry, Fourth Edition Paula Yurkanis Bruice ISBN 0-13-140748-1
- Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (1st ed.). Oxford University Press. ISBN 978-0-19-850346-0.
- Organic Chemistry by Marye Anne Fox and James K. Whitesell ISBN 0-7637-0413-X
- The Cycloheptatrienylium (Tropylium) Ion W. Von E. Doering and L. H. Knox J. Am. Chem. Soc.; 1954; 76(12) pp 3203 - 3206
- On the Constitution of the Salts of Imido-Ethers and other Carbimide Derivatives; Am. Chem. J. 21, 101
- Rzepa, H. S.; Allan, C. S. M. (2010). "Racemization of Isobornyl Chloride via Carbocations: A Nonclassical Look at a Classic Mechanism". Journal of Chemical Education 87 (2)
- The 1,1,2,3,4,5,6-heptamethylbenzenonium ion W. von E. Doering and M. Saunders H. G. Boyton, H. W. Earhart, E. F. Wadley and W. R. Edwards G. Laber Tetrahedron Volume 4, Issues 1-2 , 1958, Pages 178-185
- The 7-norbornadienyl carbonium ion Paul R. Story and Martin Saunders J. Am. Chem. Soc.; 1960; 82(23) pp 6199 - 6199
- George A. Olah - Nobel Lecture
- Stable Carbonium Ions. XVII.1a Cyclopropyl Carbonium Ions and Protonated Cyclopropyl Ketones Charles U. Pittman Jr., George A. Olah J. Am. Chem. Soc., 1965, 87 (22), pp 5123–5132
参见
[编辑]
