氫鍵催化
外觀

氫鍵催化是有機催化反應,以氫鍵相互作用加速和控制有機反應。在生物系統,氫鍵在許多酶促反應中起關鍵作用,包括調整受質方向和降低反應門檻。[1]然而,化學家最近才開始用氫鍵的力量來催化反應,與路易士酸催化研究相比,該領域不太發達。[2]
供氫鍵體可以多種機制促成反應。反應時,氫鍵可穩定陰離子中間體和過渡態,或結合小陰離子形成活躍親電陽離子;更酸的供體可充當通用酸或特定酸,以質子啟動親電試劑。「雙官能催化」中,親核試劑和親電試劑反應雙方同時啟動,是有效的方法。氫鍵催化中,催化劑份子與受質緊密結合,是促成選擇對映體的有效方法。
氫鍵催化劑通常易製,相對穩定,且可以合成高對映純度。氫鍵催化反應發表越發頻密,如羥醛加成、地-阿環加成和曼氏反應等可用於合成的常見有機反應之不對稱變體。[3]
然而,氫鍵催化發揮全部合成效用潛力前必須克服幾樣挑戰。目前已知的反應只限於某些受質,加速率和周轉率亦頗低,需高催化劑負載。催化劑常以覆試發現和微調,而化學家對催化劑結構和反應活度關係知之甚少。此外,領域仍未了解遠超一般機理的新發現反應。隨著未來更詳細的結構和機理研究,氫鍵催化有巨大潛力,有用於不對稱合成的前景,可用於高效的新型選定反應。
催化方式
[編輯]穩定四面體中間體
[編輯]


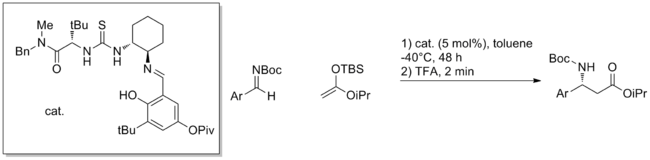
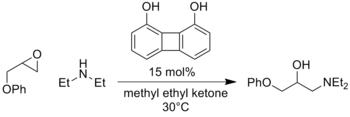
穩定陰離子部份
[編輯]
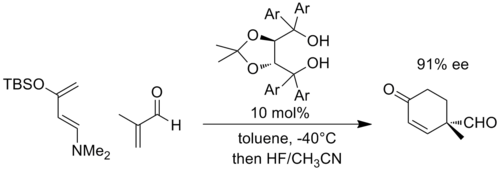
陰離子結合
[編輯]


質子結合
[編輯]
多功能策略
[編輯]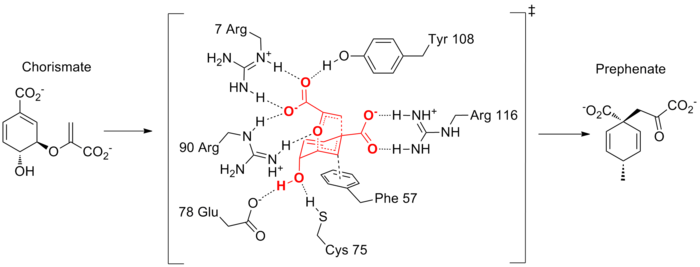



參見
[編輯]延伸閱讀
[編輯]- ^ Jacobsen, E. N.; Knowles, R. R. Attractive noncovalent interactions in asymmetric catalysis: Links between enzymes and small molecule catalysts (PDF). Proc. Natl. Acad. Sci. September 2010, 107 (48): 20678–20685 [2022-11-19]. Bibcode:2010PNAS..10720678K. PMC 2996434
 . PMID 20956302. doi:10.1073/pnas.1006402107
. PMID 20956302. doi:10.1073/pnas.1006402107  . (原始內容存檔 (PDF)於2023-01-06).
. (原始內容存檔 (PDF)於2023-01-06).
- ^ Jacobsen, E. N.; Taylor, M. S. Asymmetric catalysis by chiral hydrogen-bond donors. Angew. Chem. Int. Ed. February 2006, 45 (10): 1521–1539. PMID 16491487. doi:10.1002/anie.200503132.
- ^ Doyle, Abigail G.; Jacobsen, E. N. Small-molecule H-bond donors in asymmetric catalysis. Chem. Rev. December 2007, 107 (12): 5713–5743. PMID 18072808. doi:10.1021/cr068373r.
