Microbiota uterina
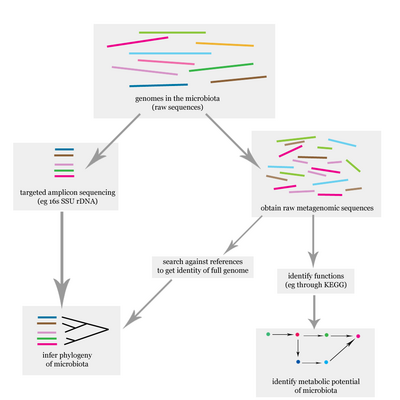
La microbiota uterina son las bacterias comensales, no patógenas, virus, levaduras/hongos presentes en un útero sano, líquido amniótico y endometrio y el entorno específico en el que habitan. Recientemente se confirmó que el útero y sus tejidos no son estériles.[1] Debido a la mejora de las técnicas de secuenciación del gen 16S ARNr, la detección de las bacterias que están presentes en números bajos es posible.[2] Usando este procedimiento que permite la detección de bacterias que no pueden cultivarse fuera del cuerpo, se espera que aumenten los estudios de microbiota presentes en el útero.[3]
Microbiota uterina y fertilidad
[editar]La evidencia muestra que la presencia de 16S rRNA uterino no es solo el resultado de errores de muestreo o análisis y merece ser reconocido. El concepto del endometrio estéril, y el compartimento uterino en general, está pasado de moda, aunque el verdadero microbiota uterino central aún debe evaluarse. Se necesitan estudios funcionales para dilucidar la importancia fisiológica del microbiota en la fertilidad. El desafío de estudiar la inmunología reproductiva y la microbiota involucrada es que la investigación sobre todos los diferentes aspectos aún está en su infancia; el microbioma, la inmunidad, la endocrinología en el embarazo y el desarrollo placentario y fetal deben estudiarse juntos para obtener una visión más completa.[4]
Características
[editar]Las bacterias, los virus y un género de levaduras son una parte normal del útero antes y durante el embarazo.[5] Se ha descubierto que el útero posee su propio microbiota característico que difiere significativamente del microbiota vaginal. A pesar de su estrecha conexión espacial con la vagina, el microbioma del útero se parece más a las bacterias comensales que se encuentran en la cavidad oral. Además, el sistema inmunitario puede diferenciar entre las bacterias que normalmente se encuentran en el útero y las que son patógenas. Los cambios hormonales tienen un efecto sobre la microbiota del útero.[6]
Taxones
[editar]
Comensales
[editar]

Los organismos enumerados a continuación se han identificado como comensales en el útero sano. Algunos también tienen el potencial de crecer hasta el punto de causar enfermedades:
Organismo Comensal Transitorio Potencial
patógenoRef. Escherichia coli x x [6] Escherichia spp. x x [6] Ureaplasma parvum x x [6] Fusobacterium nucleatum x [7] Prevotella tannerae x [5] Bacteroides spp. x [5] Streptomyces avermitilis x [6] Mycoplasma spp. x x [5] Neisseria lactamica x [6] Neisseria polysaccharea x [6] Virus de Epstein-Barr x x [5] Virus sincitial respiratorio x x [5] Adenovirus x x [5] Candida spp. x x [5]
Patógenos
[editar]Otros taxones pueden estar presentes, sin causar enfermedad o una respuesta inmune. Su presencia está asociada con resultados negativos de nacimiento.[5][6]
Organismo Patógeno Mayor riesgo de Ref. Ureaplasma urealyticum ruptura prematura de membranastrabajo prematuro cesárea
inflamación placentaria
neumonía congénita
bacteriemia
meningitis
lesión pulmonar fetal
muerte del infante
[5][8][9] Haemophilus influenzae ruptura prematura de membranastrabajo prematuro parto prematuro
[5] Ureaplasma parvum [5] Fusobacterium nucleatum [5] Prevotella tannerae [5] Bacteroides spp. Streptomyces avermitilis [5] Mycoplasma hominis neumonía congénitabacteriemia meningitis
enfermedad inflamatoria pélvica
fiebre posparto y postabortal
[5][8] Neisseria lactamica [5] Neisseria polysaccharea [5] Virus de Epstein-Barr [5] Virus sincitial respiratorio [5] Adenovirus [5] Candida spp.. [5]
Significación clínica
[editar]Se han inyectado antibióticos profilácticos en el útero para tratar la infertilidad. Esto se hizo antes de la transferencia de embriones con la intención de mejorar las tasas de implantación. No existe asociación entre la implantación exitosa y el tratamiento con antibióticos.[10] Los tratamientos de infertilidad a menudo progresan hasta el punto en que se realiza un análisis microbiológico de la microbiota uterina. El parto prematuro se asocia con ciertas especies de bacterias que normalmente no forman parte del microbioma uterino sano.[5]
Respuesta inmune
[editar]La respuesta inmune se vuelve más pronunciada cuando se encuentran bacterias que no son comensales.[5]
Historia
[editar]Las investigaciones sobre microbiomas asociados a la reproducción comenzaron alrededor de 1885 por Theodor Escherich . Escribió que el meconio del recién nacido estaba libre de bacterias. Hubo un consenso general en ese momento e incluso recientemente que el útero era estéril y esto se conoció como el paradigma del útero estéril. Otras investigaciones utilizaron pañales estériles para la recolección de meconio. No se pudieron cultivar bacterias a partir de las muestras. Otros estudios mostraron que se detectaron bacterias y fueron directamente proporcionales al tiempo entre el nacimiento y el paso del meconio.[1]
Investigación
[editar]Las investigaciones sobre el papel del microbioma uterino en el desarrollo del microbioma infantil están en curso.[1]
Dos estudios que relacionan el parto por césarea y desarrollo cognitivo en niños y niñas entre los 4 y 9 años, determinaron la existencia de un impacto negativo significativo.[11] Polidano et al. (2017) de la Universidad de Melbourne sugieren que se debe a las diferente composición de la microbiota intestinal entre los niños y niñas nacidos por parto vaginal y los nacidos por cesárea.[12][13]
Véase también
[editar]- Microbioma humano
- Proyecto de microbioma humano
- Viroma humano
- Lista de péptidos antimicrobianos en el aparato reproductor femenino.
- Anexo:Microbiota de la vaginosis bacteriana
- Microbiota placentaria
- Epitelio vaginal
- Flora vaginal en el embarazo
Referencias y notas
[editar]- ↑ a b c Perez-Muñoz, Maria Elisa; Arrieta, Marie-Claire; Ramer-Tait, Amanda E.; Walter, Jens (2017). «A critical assessment of the “sterile womb” and “in utero colonization” hypotheses: implications for research on the pioneer infant microbiome». Microbiome 5 (1). ISSN 2049-2618. PMC 5410102. PMID 28454555. doi:10.1186/s40168-017-0268-4.
- ↑ Verstraelen, Hans; Vilchez-Vargas, Ramiro; Desimpel, Fabian; Jauregui, Ruy; Vankeirsbilck, Nele; Weyers, Steven; Verhelst, Rita; De Sutter, Petra et al. (2016). «Characterisation of the human uterine microbiome in non-pregnant women through deep sequencing of the V1-2 region of the 16S rRNA gene». PeerJ 4: e1602. ISSN 2167-8359. PMC 4730988. PMID 26823997. doi:10.7717/peerj.1602.
- ↑ Wassenaar, T.M.; Panigrahi, P. (2014). «Is a foetus developing in a sterile environment?». Letters in Applied Microbiology 59 (6): 572-579. ISSN 0266-8254. PMID 25273890. doi:10.1111/lam.12334.
- ↑ Moreno, I.; Franasiak, J. (2017). «Endometrial microbiota—new player in town». Fertility and Sterility 108 (1): 32-39.
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u v w Payne, Matthew S.; Bayatibojakhi, Sara (2014). «Exploring Preterm Birth as a Polymicrobial Disease: An Overview of the Uterine Microbiome». Frontiers in Immunology 5: 595. ISSN 1664-3224. PMC 4245917. PMID 25505898. doi:10.3389/fimmu.2014.00595.
- ↑ a b c d e f g h Yarbrough, V. L.; Winkle, S.; Herbst-Kralovetz, M. M. (2014). «Antimicrobial peptides in the female reproductive tract: a critical component of the mucosal immune barrier with physiological and clinical implications». Human Reproduction Update 21 (3): 353-377. ISSN 1355-4786. PMID 25547201. doi:10.1093/humupd/dmu065.
- ↑ Prince, Amanda L.; Antony, Kathleen M.; Chu, Derrick M.; Aagaard, Kjersti M. (2014). «The microbiome, parturition, and timing of birth: more questions than answers». Journal of ReproductiveImmunology. 104–105: 12-19. ISSN 0165-0378. PMC 4157949. PMID 24793619. doi:10.1016/j.jri.2014.03.006.
- ↑ a b Ureaplasma Infection: Background, Pathophysiology, Epidemiology. 17 de noviembre de 2017. Consultado el 7 de diciembre de 2017 – via eMedicine.
- ↑ Pryhuber, Gloria S. (2015). «Postnatal Infections and Immunology Affecting Chronic Lung Disease of Prematurity». Clinics in Perinatology 42 (4): 697-718. ISSN 0095-5108. PMC 4660246. PMID 26593074. doi:10.1016/j.clp.2015.08.002.
- ↑ Franasiak, Jason M.; Scott, Richard T. (2015). «Reproductive tract microbiome in assisted reproductive technologies». Fertility and Sterility 104 (6): 1364-1371. ISSN 0015-0282. PMID 26597628. doi:10.1016/j.fertnstert.2015.10.012.
- ↑ Nassar, Natasha; Morris, Jonathan M.; Martin, Andrew J.; Bowen, Jenny R.; Roberts, Christine L.; Bentley, Jason P. (1 de diciembre de 2016). «Planned Birth Before 39 Weeks and Child Development: A Population-Based Study». Pediatrics (en inglés) 138 (6): e20162002. ISSN 0031-4005. PMID 27940704. doi:10.1542/peds.2016-2002. Consultado el 8 de marzo de 2019.
- ↑ Bornstein, Joel C.; Zhu, Anna; Polidano, Cain (13 de septiembre de 2017). «The relation between cesarean birth and child cognitive development». Scientific Reports (en inglés) 7 (1): 11483. ISSN 2045-2322. doi:10.1038/s41598-017-10831-y. Consultado el 8 de marzo de 2019.
- ↑ JM Cézares-Méndez; JF Cadena-León; Montijo-Barrios, E.; Zárate-Mondragón, F.; Cervantes-Bustamante, R.; EM Toro-Monjaraz; JA Ramírez-Mayans; VP Zamudio-Vázquez (15 de marzo de 2017). [http://www.medigraphic.com/cgi-bin/new/resumen.cgi?IDARTICULO=70964 «Importancia de la microbiota gastrointestinal en pediatr�a»]. Acta Pediátrica de México (en español) 38 (1): 49-62. Consultado el 8 de marzo de 2019.
