Ацетали: различия между версиями
| [отпатрулированная версия] | [непроверенная версия] |
Kurgus (обсуждение | вклад) |
Elenheru (обсуждение | вклад) Нет описания правки |
||
| (не показано 38 промежуточных версий 23 участников) | |||
| Строка 1: | Строка 1: | ||
[[Файл: |
[[Файл:Ketal-2D-skeletal.png|мини|Общее строение ацеталей]] |
||
{{Не путать|Полиацеталь|соответствующим полимером}} |
|||
'''Ацета́ли''' |
'''Ацета́ли''' — [[простые эфиры]] ''[[Геминальный|гем]]''-[[Диолы|диолов]] общей формулы R₂C(OR¹)(OR²), где R¹ и R² — [[Углеводородный радикал|углеводородные радикалы]]: [[метил|CH<sub>3</sub>]], [[этил|C<sub>2</sub>H<sub>5</sub>]] и др. Первоначально к ацеталям относили производные [[Альдегиды|альдегидов]] RCH(OR¹)(OR²), а аналогичные производные [[Кетоны|кетонов]] именовались [[Кетали|кеталями]] R—C(R¹)(OR²)(OR³), однако в настоящее время в номенклатуре IUPAC для обоих классов соединений рекомендуется название «ацетали».<ref>{{Cite web |url=http://goldbook.iupac.org/A00062.html |title=acetals // IUPAC Gold Book |access-date=2011-09-24 |archive-date=2011-07-07 |archive-url=https://web.archive.org/web/20110707185511/http://goldbook.iupac.org/A00062.html |deadlink=no }}</ref>. |
||
Если один из R¹ или R² представляет собой атом [[ |
Если один из R¹ или R² представляет собой атом [[водород]]а, то такие соединения R₂C(OH)OR′ ({{nobr|R′ ≠ H}}) называют [[Полуацетали|полуацеталями]]<ref>{{Cite web |url=http://goldbook.iupac.org/H02774.html |title=hemiacetals // IUPAC Gold Book |access-date=2011-09-24 |archive-date=2011-08-20 |archive-url=https://web.archive.org/web/20110820031407/http://goldbook.iupac.org/H02774.html |deadlink=no }}</ref>. |
||
== Свойства и реакционная способность == |
== Свойства и реакционная способность == |
||
Низшие ацетали — жидкости приятного фруктового запаха, растворимые в органических растворителях и нерастворимые в воде. |
|||
| ⚫ | |||
| ⚫ | Ацетали устойчивы в щелочных средах, однако в присутствии [[Кислота|кислот]] легко [[гидролиз]]уются водой с образованием [[альдегиды|альдегидов]] и [[спирты|спиртов]], производными которых они являются. Полуацетали, как правило, ещё легче подвержены [[гидролиз]]у и в растворах находятся в [[Химическое равновесие|равновесии]] с исходным альдегидом и спиртом. |
||
Такое поведение ацеталей и полуацеталей — как и их образование из карбонильных соединений — обусловлено общим механизмом кислотного катализа с образованием [[Химический резонанс|резонансно стабилизированного]] α-атомом кислорода [[карбокатион]]а: |
|||
:: <math>\mathsf{R\text{-}CHO + H^+ \rightleftarrows R\text{-}CH^+\text{-}OH \rightleftarrows R\text{-}CH\text{=}O^+H}</math> |
|||
:: <math>\mathsf{R\text{-}CH^+\text{-}OH + R'OH \rightleftarrows R\text{-}CH(OR')OH + H^+}</math> |
|||
:: <math>\mathsf{R\text{-}CH(OR')OH + R'OH \rightarrow R\text{-}CH(OR')_2 + H_2O}</math> |
|||
Все эти реакции обратимы, и положение равновесия может быть сдвинуто удалением из реакционной смеси какого-либо компонента. Другим следствием обратимости реакций ацеталей в условиях кислотного катализа, идущих с образованием карбокатионов, являются реакции переацетализации: |
|||
:: <math>\mathsf{R\text{-}CH(OR')_2 + R''XS \rightarrow R\text{-}CH(OR_1)OR'' + H_2X, \ \ \ X=O, S}</math> |
|||
Переацетализация происходит при взаимодействии ацеталей не только со спиртами, но и при реакции с тиолами и ведет в последнем случае к образованию [[Тиоацетали|дитиоацеталей]] R<sub>2</sub>C(SR)<sub>2</sub>. |
|||
В реакциях с азотистыми нуклеофилами ацетали выступают как функциональные аналоги исходных карбонильных соединений: так, в реакциях ацеталей с первичными [[Амины|аминами]], [[гидразины|гидразинами]] и [[гидроксиламин]]ом образуются [[имины]], [[гидразоны]] и [[оксимы]]: |
|||
:: <math>\mathsf{R_2C(OR')_2 + R''NH_2 \rightarrow R_2C\text{=}NR'' + 2R'OH}</math> |
|||
: R<nowiki>''</nowiki> = Alk, Ar (имины), NR<sub>2</sub> (гидразоны), OH (оксимы) |
|||
При взаимодействии вторичных аминов с ацеталями — функциональными аналогами енолизирующихся альдегидов и кетонов образуются [[енамины]]: |
|||
:: <math>\mathsf{R'_2CHCR''(OR)_2 + R'''NH \rightarrow R'_2C\text{=}CR''NR'''}</math> |
|||
== Синтез == |
== Синтез == |
||
Основным препаративным методом синтеза ацеталей является взаимодействие альдегидов |
Основным препаративным методом синтеза ацеталей является взаимодействие альдегидов и кетонов со спиртами либо [[Ортоэфиры|ортоэфирами]] в условиях кислотного катализа: |
||
: [[Файл:Acetal Synthesis V.1.svg|400px]] |
: [[Файл:Acetal Synthesis V.1.svg|400px]] |
||
В качестве эквивалента диола в таком синтезе ацеталей могут выступать эпоксиды: |
|||
: [[Файл:1,3-dioxalane synthesis 3.png|400 px]] |
|||
Ацетали также могут быть синтезированы присоединением спиртов к виниловым эфирам и их гомологам: |
Ацетали также могут быть синтезированы присоединением спиртов к виниловым эфирам и их гомологам: |
||
:: <math>\mathsf{CH_2\text{=}CHOR + R'OH \rightarrow CH_3CH(OR)OR'}</math> |
|||
: СН<sub>2</sub>=СНОR + R<sup>1</sup>ОН <math>\to</math> СН<sub>3</sub>СН(ОR)(OR<sup>1</sup>) |
|||
Замещение галогена в алифатических ''гем''-дагалогенидах и α-галогенэфирах алкоголятами и фенолятами также ведет к ацеталям: |
Замещение галогена в алифатических ''гем''-дагалогенидах и α-галогенэфирах алкоголятами и фенолятами также ведет к ацеталям: |
||
: |
:: <math>\mathsf{RCH(X)Hal + RO^- \rightarrow RCH(OR)_2 + X^-, \ X = OR, Hal}</math> |
||
: X = OR, Hal, |
|||
| ⚫ | такой метод синтеза |
||
| ⚫ | такой метод синтеза — взаимодействие этилидендибромида с этилатом натрия — был использован [[Вюрц, Шарль Адольф|Вюрцем]] и Фраполли для доказательства строения диэтилацеталя уксусного альдегида, полученного в 1833 году [[Дёберейнер, Иоганн Вольфганг|Деберейнером]] при окисления [[этанол]]а над [[Платиновая чернь|платиновой чернью]]<ref>{{ВТ-ЭСБЕ|Ацеталь}}</ref>. |
||
| ⚫ | |||
<references/> |
|||
== Биологическое значение == |
|||
{{orgchem-stub}} |
|||
Образование полуацеталей и ацеталей имеет чрезвычайно важное значение в химии [[Углеводы|углеводов]], являющихся полигидроксиальдегидами ([[альдозы]]) и полигидроксикетонами ([[кетозы]]). |
|||
Такое сочетание гидроксильных и карбонильных функций в одной молекуле ведет к тому, что [[моносахариды]] могут существовать и в линейной форме, и, за счет внутримолекулярного образования полуацеталей, в циклической: |
|||
: [[Файл:Oxy-Cyclo-Tautomerie Ribose.svg|400 px]] |
|||
: <code>Линейная (оксо-) и циклическая полуацетальная ([[Фуранозы|фуранозная]]) формы [[Рибоза|рибозы]]</code> |
|||
В водных растворах линейные оксоформы и циклические полуацетальные формы моносахаридов, являющиеся динамическими структурными изомерами, находятся равновесии, то есть являются [[Таутомерия|таутомерами]]. Таутомерия этого типа получила название ''цикло-оксо таутомерии''. |
|||
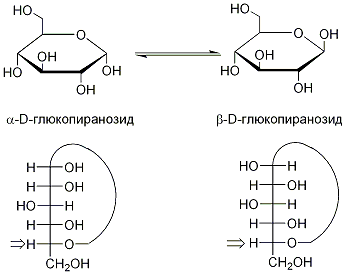
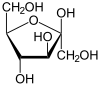
В свою очередь, циклические полуацетальные формы моносахаридов могут существовать в виде двух стереоизомерных [[Аномеры|аномерных]] форм, образующихся вследствие образования циклических полуацеталей при нуклеофильной атаки гидроксила с различных сторон карбонильной группы: |
|||
: [[Файл:Anomers.gif|Anomers.gif]] |
|||
: <code>Пиранозидные аномеры глюкозы, различающиеся конфигурацией хирального полуацетального центра</code> |
|||
Циклические полуацетальные формы [[Моносахариды|моноз]] способны образовывать полные ацетали с различными соединениями: так, образование смешанных ацеталей с другими монозами ведет к образованию [[Сахариды|сахаридов]] — обширного класса природных соединений, включающих как низкомолекулярные ди- и олигосахариды, так и высокомолекулярные полисахариды ([[целлюлоза]], [[хитин]] и др.): |
|||
: {| |
|||
|- |
|||
| [[Файл:Alpha-D-Glucopyranose.svg|100 px|Пиранозная форма глюкозы]] |
|||
|| + [[Файл:Beta-D-Fructofuranose.svg|100 px|Фуранозная форма фруктозы]] |
|||
|| → [[Файл:Sucrose structure formula inkscape.svg|240 px]] |
|||
|| + H<sub>2</sub>O |
|||
|- align="center" |
|||
| <code>Глюкоза</code> |
|||
|| <code>Фруктоза</code> |
|||
|| <code>Сахароза</code> |
|||
|| |
|||
|} |
|||
<!-- |
|||
так и высокомолекулярные полисахариды (целлюлоха, крахмал и др.) |
|||
: [[Файл:Cellulose Sessel.svg|Целлюлоза]] |
|||
и гликозиды: |
|||
: [[Файл:Salicin-perspective-2D-skeletal.png|200 px]] |
|||
--> |
|||
== См.также == |
|||
* [[2-Азидо-1,1-диметоксиэтан]] |
|||
* [[(3-Бромпропил)этилацеталь ацетальдегида]] |
|||
| ⚫ | |||
{{примечания}} |
|||
[[Категория:Ацетали|*|*]] |
[[Категория:Ацетали|*|*]] |
||
[[Категория:Простые эфиры]] |
[[Категория:Простые эфиры]] |
||
[[Категория:Терминология IUPAC]] |
|||
[[ar:أسيتال]] |
|||
[[ca:Acetal]] |
|||
[[de:Acetale]] |
|||
[[en:Acetal]] |
|||
[[es:Acetal]] |
|||
[[et:Atsetaalid]] |
|||
[[fa:استال]] |
|||
[[fr:Acétal et cétal]] |
|||
[[it:Acetali]] |
|||
[[ja:アセタール]] |
|||
[[mk:Ацетал]] |
|||
[[nl:Acetaal]] |
|||
[[nn:Acetal]] |
|||
[[no:Acetal]] |
|||
[[pl:Acetale]] |
|||
[[pt:Acetal]] |
|||
[[sv:Acetal]] |
|||
[[uk:Ацеталі]] |
|||
[[zh:缩醛]] |
|||
Версия от 22:54, 15 апреля 2024

Ацета́ли — простые эфиры гем-диолов общей формулы R₂C(OR¹)(OR²), где R¹ и R² — углеводородные радикалы: CH3, C2H5 и др. Первоначально к ацеталям относили производные альдегидов RCH(OR¹)(OR²), а аналогичные производные кетонов именовались кеталями R—C(R¹)(OR²)(OR³), однако в настоящее время в номенклатуре IUPAC для обоих классов соединений рекомендуется название «ацетали».[1].
Если один из R¹ или R² представляет собой атом водорода, то такие соединения R₂C(OH)OR′ (R′ ≠ H) называют полуацеталями[2].
Свойства и реакционная способность
Низшие ацетали — жидкости приятного фруктового запаха, растворимые в органических растворителях и нерастворимые в воде.
Ацетали устойчивы в щелочных средах, однако в присутствии кислот легко гидролизуются водой с образованием альдегидов и спиртов, производными которых они являются. Полуацетали, как правило, ещё легче подвержены гидролизу и в растворах находятся в равновесии с исходным альдегидом и спиртом.
Такое поведение ацеталей и полуацеталей — как и их образование из карбонильных соединений — обусловлено общим механизмом кислотного катализа с образованием резонансно стабилизированного α-атомом кислорода карбокатиона:
Все эти реакции обратимы, и положение равновесия может быть сдвинуто удалением из реакционной смеси какого-либо компонента. Другим следствием обратимости реакций ацеталей в условиях кислотного катализа, идущих с образованием карбокатионов, являются реакции переацетализации:
Переацетализация происходит при взаимодействии ацеталей не только со спиртами, но и при реакции с тиолами и ведет в последнем случае к образованию дитиоацеталей R2C(SR)2.
В реакциях с азотистыми нуклеофилами ацетали выступают как функциональные аналоги исходных карбонильных соединений: так, в реакциях ацеталей с первичными аминами, гидразинами и гидроксиламином образуются имины, гидразоны и оксимы:
- R'' = Alk, Ar (имины), NR2 (гидразоны), OH (оксимы)
При взаимодействии вторичных аминов с ацеталями — функциональными аналогами енолизирующихся альдегидов и кетонов образуются енамины:
Синтез
Основным препаративным методом синтеза ацеталей является взаимодействие альдегидов и кетонов со спиртами либо ортоэфирами в условиях кислотного катализа:
В качестве эквивалента диола в таком синтезе ацеталей могут выступать эпоксиды:
Ацетали также могут быть синтезированы присоединением спиртов к виниловым эфирам и их гомологам:
Замещение галогена в алифатических гем-дагалогенидах и α-галогенэфирах алкоголятами и фенолятами также ведет к ацеталям:
такой метод синтеза — взаимодействие этилидендибромида с этилатом натрия — был использован Вюрцем и Фраполли для доказательства строения диэтилацеталя уксусного альдегида, полученного в 1833 году Деберейнером при окисления этанола над платиновой чернью[3].
Биологическое значение
Образование полуацеталей и ацеталей имеет чрезвычайно важное значение в химии углеводов, являющихся полигидроксиальдегидами (альдозы) и полигидроксикетонами (кетозы).
Такое сочетание гидроксильных и карбонильных функций в одной молекуле ведет к тому, что моносахариды могут существовать и в линейной форме, и, за счет внутримолекулярного образования полуацеталей, в циклической:
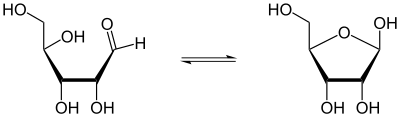
Линейная (оксо-) и циклическая полуацетальная (фуранозная) формы рибозы
В водных растворах линейные оксоформы и циклические полуацетальные формы моносахаридов, являющиеся динамическими структурными изомерами, находятся равновесии, то есть являются таутомерами. Таутомерия этого типа получила название цикло-оксо таутомерии.
В свою очередь, циклические полуацетальные формы моносахаридов могут существовать в виде двух стереоизомерных аномерных форм, образующихся вследствие образования циклических полуацеталей при нуклеофильной атаки гидроксила с различных сторон карбонильной группы:
Циклические полуацетальные формы моноз способны образовывать полные ацетали с различными соединениями: так, образование смешанных ацеталей с другими монозами ведет к образованию сахаридов — обширного класса природных соединений, включающих как низкомолекулярные ди- и олигосахариды, так и высокомолекулярные полисахариды (целлюлоза, хитин и др.):
См.также
Примечания
- ↑ acetals // IUPAC Gold Book. Дата обращения: 24 сентября 2011. Архивировано 7 июля 2011 года.
- ↑ hemiacetals // IUPAC Gold Book. Дата обращения: 24 сентября 2011. Архивировано 20 августа 2011 года.
- ↑ Ацеталь // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.