Нитрат уранила: различия между версиями
| [непроверенная версия] | [непроверенная версия] |
Нет описания правки Метки: через визуальный редактор с мобильного устройства из мобильной версии |
реакция для хим. свойства |
||
| Строка 117: | Строка 117: | ||
== Химические свойства == |
== Химические свойства == |
||
При нагревании кристаллы плавятся и выделяют [[Азотная кислота|азотную кислоту]] и воду. |
При нагревании кристаллы плавятся и выделяют [[Азотная кислота|азотную кислоту]] и воду. Кристаллогидрат легко выветривается на воздухе. |
||
Кристаллогидрат легко выветривается на воздухе. |
|||
Характерная реакция — при действии [[аммиак]]а образуется жёлтый осадок урановокислого [[Аммоний|аммония]] |
Характерная реакция — при действии [[аммиак]]а образуется жёлтый осадок урановокислого [[Аммоний|аммония]]: |
||
: <math>\mathsf{2UO_2(NO_3)_2 + 6NH_3*H_2O \xrightarrow{} (NH_4)_2U_2O_7\downarrow + 4NH_4NO_3 + 3H_2O}</math> |
|||
Обладает свойством [[дубление|дубить]] [[желатин]]. Ядовит. |
Обладает свойством [[дубление|дубить]] [[желатин]]. Ядовит. |
||
| Строка 133: | Строка 134: | ||
Реакции протекают по уравнениям: |
Реакции протекают по уравнениям: |
||
: <math>\mathsf{4Ag + 4K_3[Fe(CN)_6] |
: <math>\mathsf{4Ag + 4K_3[Fe(CN)_6] \xrightarrow{} 3K_4[Fe(CN)_6] + Ag_4[Fe(CN)_6]}</math> |
||
: <math>\mathsf{Ag_4[Fe(CN)_6] + 2UO_2(NO_3)_2 |
: <math>\mathsf{Ag_4[Fe(CN)_6] + 2UO_2(NO_3)_2 \xrightarrow{} 4AgNO_3 + (UO_2)_2[Fe(CN)_6]}</math> |
||
Азотнокислый уранил входит в состав промышленно выпускаемых усилителей, применяемых в фотопечати, в частности, ОРВО 604. |
Азотнокислый уранил входит в состав промышленно выпускаемых усилителей, применяемых в фотопечати, в частности, ОРВО 604. |
||
Версия от 20:41, 14 декабря 2022
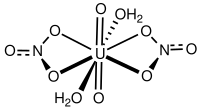
| Нитрат уранила | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Уранила нитрат |
| Традиционные названия | Азотнокислый уранил |
| Хим. формула | UO8N2 |
| Рац. формула | UO2(NO3)2 |
| Физические свойства | |
| Состояние | твёрдое, кристаллическое |
| Молярная масса | 394,04(безводн.); 502,13(гексагидрат) г/моль |
| Плотность | 3,35 г/см3 (дигидрат) |
| Термические свойства | |
| Температура | |
| • разложения | 100°C |
| Энтальпия | |
| • образования | 1987 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде, 20°C | 119 г/100 мл |
| • в воде, 30°C | 138 г/100 мл |
| • в ацетоне | растворим |
| • в этаноле | растворим |
| Классификация | |
| Рег. номер CAS | 10102-06-4 |
| PubChem | 24933 и 25199613 |
| Рег. номер EINECS | 233-266-3 |
| SMILES | |
| InChI | |
| Безопасность | |
| Токсичность | Высокотоксичен, радиоактивен |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Урани́л азотноки́слый — неорганическое соединение, азотнокислая окись урана. Имеет формулу UO2(NO3)2 (безводный); UO2(NO3)2·6H2O (кристаллогидрат).
Роль металла в этой соли исполняет катион уранила [UO2]2+.
Физические свойства
Кристаллы жёлтого цвета с зеленоватым отблеском, легко растворимые в воде. Водный раствор имеет кислую реакцию. Также растворим в этаноле, ацетоне и эфире, нерастворим в бензоле, толуоле и хлороформе. Молекулярный вес безводной формы 394,04; кристаллогидрата 502,13.
Химические свойства
При нагревании кристаллы плавятся и выделяют азотную кислоту и воду. Кристаллогидрат легко выветривается на воздухе.
Характерная реакция — при действии аммиака образуется жёлтый осадок урановокислого аммония:
Обладает свойством дубить желатин. Ядовит.
Получение
Получают растворением трехокиси урана в азотной кислоте[1]:
Применение
В фотографии на основе солей серебра применяется как усилитель негативов и для тонирования готовых отпечатков (рецепт на основе азотнокислого уранила окрашивает фотоснимок в красно-коричневые тона). При этом часть серебра в изображении заменяется на железосинеродистый уранил (UO2)2[Fe(CN)6].
Реакции протекают по уравнениям:
Азотнокислый уранил входит в состав промышленно выпускаемых усилителей, применяемых в фотопечати, в частности, ОРВО 604.
Примечания
- ↑ Карякин, 1974, с. 366.
Литература
- Волгин А. Г. Фотография. 1000 рецептов. — М.: Химия, 1993.
- Карякин Ю. В., Ангелов И. И. Чистые химические вещества. — М.: Химия, 1974. — 408 с.
- Мархилевич К. И. , Яштолд-Говорко В. А. Фотографическая химия. — М.: Искусство, 1956.


![{\displaystyle {\mathsf {4Ag+4K_{3}[Fe(CN)_{6}]\xrightarrow {} 3K_{4}[Fe(CN)_{6}]+Ag_{4}[Fe(CN)_{6}]}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/72e16e475b45a4079b75c813697111c1593c9e96)
![{\displaystyle {\mathsf {Ag_{4}[Fe(CN)_{6}]+2UO_{2}(NO_{3})_{2}\xrightarrow {} 4AgNO_{3}+(UO_{2})_{2}[Fe(CN)_{6}]}}}](https://wikimedia.org/ruwiki/api/rest_v1/media/math/render/svg/298497f5389307dc1deea0fc1b7bd59572c3dce4)