Дитиотреитол
| Дитиотреитол | |
|---|---|
 | |
| Общие | |
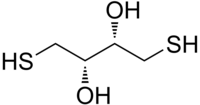
| Систематическое наименование |
(2S,3S)-1,4-бис(сульфанил)бутан-2,3-диол |
| Хим. формула | С4H10O2S2 |
| Физические свойства | |
| Состояние | белое твердое вещество |
| Молярная масса | 154,253 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 42–43 °C |
| • кипения | 125–130 °C |
| Классификация | |
| Рег. номер CAS | 3483-12-3 |
| PubChem | 446094 |
| Рег. номер EINECS | 222-468-7 |
| SMILES | |
| InChI | |
| ChEBI | 42170 |
| ChemSpider | 393541 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Дитиотреитол (дитиотреит, ДТТ, англ. DTT) — низкомолекулярный восстанавливающий агент, известный также как реагент Клеланда. Название молекулы происходит от четырехуглеродного сахара — треозы.
Восстанавливающий агент
[править | править код]Дитиотреитол — очень сильный восстанавливающий агент, способный формировать шестичленное кольцо путём образования внутримолекулярной дисульфидной связи. При рН 7 имеет восстановительный потенциал −0,33 В. Восстановление дисульфидных связей осуществляется путём двух последовательных тиол-дисульфидных обменов (см. ниже). Интермедиат нестабилен, так как вторая тиоловая группа имеет склонность к закрытию кольца и образованию окисленного ДТТ, при этом образуются две восстановленные дисульфидные связи. ДТТ проявляет восстанавливающую активность только при рН около 7, так как только отрицательно заряженный тиолят может образовывать активный -S-, в то время как протонированная тиоловая форма -SH неактивна. Константа кислотности тиоловой группы лежит между значениями рН от 9,2 до 10,1.

Применение
[править | править код]Дитиотреитол используют для «снятия защиты» с тиолированной ДНК. Концевой атом тиолированной ДНК в растворе имеет склонность к формированию димеров, особенно в присутствии кислорода. Димеризация значительно снижает эффективность последующих реакций соединения, например в случае иммобилизации ДНК на золоте в биосенсорах. Обычно ДТТ смешивают с раствором ДНК и дают время для реагирования, затем удаляют ДТТ фильтрацией или хроматографией. Удаление ДТТ называют обессаливанием.
Дитиотреитол в биохимии часто используют для восстановления дисульфидных связей в молекулах белков, и особенно внутримолекулярных и межмолекулярных связей между остатками цистеина. Однако, ДТТ не может восстанавливать дисульфидные связи, находящиеся глубоко в структуре белка (не находящиеся в контакте с растворителем), поэтому часто восстановление S-S связей производят в денатурирующих условиях (например, при нагревании, либо в присутствии сильного денатурирующего агента 6 M гуанидин гидрохлорида, 8 M мочевины, или 1 % додецилсульфата натрия). И, соответственно, присутствие дисульфидных связей на поверхности белка может быть исследовано их восстановлением в присутствии ДТТ.
ДТТ применяют также как окислитель. Преимуществом ДТТ является то, что он не образует смешанных дисульфидных связей, чем отличается от глутатиона. В очень редких случаях ДТТ может образовывать аддукты, например, два атома серы могут образовать дисульфидные связи с другими атомами серы; в подобных случаях ДТТ не может циклизоваться.
Свойства
[править | править код]ДТТ легко окисляется кислородом воздуха и поэтому является относительно нестабильным химическим соединением. Так как протонированные атомы серы имеют меньшую нуклеофильность, ДТТ является более слабым восстановителем при кислых pH.
Литература
[править | править код]- Cleland, W.W. Dithiothreitol, A New Protective Reagent for SH Groups (англ.) // Biochemistry : journal. — 1964. — April (vol. 3). — P. 480—482. — doi:10.1021/bi00892a002. — PMID 14192894.
- Ruegg, UT; Rudinger, J. Reductive cleavage of cystine disulfides with tributylphosphine (англ.) // Methods Enzymol : journal. — 1977. — Vol. 47. — P. 111—116. — doi:10.1016/0076-6879(77)47012-5. — PMID 927167.
Это заготовка статьи по биохимии. Помогите Википедии, дополнив её. |